Undersøg sonder, hvordan nanopartikler binder sig til blodproteiner ved grænseflader
Små partikler på kun en milliontedel af en millimeter på tværs kaldet nanopartikler er rigelige i det tøj, vi har på, og endda den mad, vi spiser. Ny forskning offentliggjort i PCCP indikerer, at nanopartikler er i stand til at ændre deres binding på overflader til proteiner, der er rigelige i blodet, afhængigt af om proteinet er bundet til fedtmolekyler på det tidspunkt. Resultaterne angiver, hvordan nanopartikler interagerer med blodproteiner i kroppen ved at påvirke effektiviteten af nanopartikeltransporten til overflader.
Arbejdet ligger til grund for mange aspekter af protein-nanopartikeladhæsion. For eksempel, usikkerhed omkring sikkerheden ved nanopartikler i køretøjsdampe og en række dagligvarer. Toksikologer er bekymrede over, at eksponering kan føre til, at nanopartikler kommer ind i blodbanen og samler sig i leveren, hindrer organets funktion. Imidlertid, der er også stor interesse for at bruge nanopartikler i medicin til at levere lægemidler til bestemte subcellulære regioner, såsom kernen.
I ny forskning, forskere fra Australian National University og Institut Laue-Langevin (ILL) testede en mulig mekanisme for nanopartikelbinding, kendt som 'protein corona' -hypotesen. Denne teori antyder, at nanopartikler er i stand til at komme ind i celler, fordi de binder sig til og bliver indkapslet af proteiner, forklædning af dem fra receptorer. En vigtig usikkerhed var, om denne corona -struktur også var udbredt på overflader, eller om der var forskellig adfærd.
I modsætning til mange eksperimenter med proteinkrystaller, disse forsøg blev udført i miljøer, der mere efterlignede menneskeligt blod. De brugte silica nanopartikler kun 20 nanometer i diameter, ligner dem, der findes i industrien, i vandige bufferopløsninger, der involverer salte på fysiologiske niveauer for at se, hvordan de interagerer med det mest rigelige protein i vores blod, humant serumalbumin (HSA). HSA's primære rolle er at binde sig til fedtmolekyler i blodet og transportere dem til forskellige dele af kroppen, og denne binding får proteinet til at ændre form. Begge typer HSA - med og uden fedt - blev undersøgt i denne forskning for at undersøge, om de interagerede med nanopartiklerne på overflader forskelligt.
To komplementære eksperimenter blev udført på buffer-protein-nanopartikel-blandingen for at analysere forskellige aspekter af processen.
- Neutronreflektometri på FIGARO -instrumentet ved ILL blev brugt til at studere, hvordan proteiner transporterede nanopartiklerne til luft/vand -grænsefladen. Intense neutronstråler blev affyret på filmens overflade, og afhængigheden af vinklen og bølgelængden af de reflekterede stråler gav information om strukturen og sammensætningen af de forskellige molekyler ved grænsefladen, og især forholdet mellem protein og nanopartikler i filmen.
- Røntgenreflektometri blev brugt til at bestemme overfladelagets fine struktur, og især fordelingen af proteinmolekyler, der dekorerer silica -nanopartiklerne ved grænsefladen.
Resultaterne viste, at flere faktorer er vigtige i bindingen. For det første, ladningen på silica nanopartiklen bestemmer, hvordan den interagerer med protein på overflader. Silica -partiklerne, der blev brugt i undersøgelsen, havde en lille negativ ladning og blev tiltrukket af de positivt ladede domæner for HSA, selvom den også har en negativ negativ ladning. Alligevel har proteinets fedtede form sin ladning ændret af fedtet selv, og i så fald var kun overfladeinteraktionerne uafhængige af protein:nanopartikelforholdet i opløsningen. For det andet, den fedtede form af proteinet er mere stabil og mindre tilbøjelig til at udfolde sig. Som resultat, proteinet er mindre i stand til at transportere nanopartikler til grænsefladen for at vedtage optimale konformationer ved grænsefladen, når den effektive nanopartikelkoncentration ændres. Disse resultater tyder på, at overfladedesign kan være vigtigt for at minimere toksiske virkninger af nanopartikler og også maksimere det terapeutiske potentiale af sådanne partikler.
Professor John White, Professor i fysisk og teoretisk kemi, Research School of Chemistry, Australian National University, siger, "Da giftige resultater er blevet korreleret med lille størrelse og problemerne med partikelakkumulering, er eksperimenterne blevet udført på industrielt producerede små silica-nanopartikler, der er almindeligt tilgængelige. De peger på stabil protein-nanopartikelklynge ved grænseflader, der er følsomme over for meget subtile egenskaber ved vedhæftningen protein. "
Dr. Richard Campbell, FIGARO instrumentforsker, SYG, siger, "En kritisk del af forskningen var at kunne udføre målinger på proteinmolekyler under forhold tæt på deres fysiologiske miljø. Strukturelle undersøgelser af proteiner kræver ofte, at molekylet er i en unaturlig krystallinsk form, men det kraftige FIGARO -reflektometer ved ILL tillod os for at studere HSA, der interagerer med nanopartikler på den frie overflade af en bufferopløsning, der mere efterlignede blodet. "
Eksperimentelle metoder
Mængden af deuterium - 'tungt brint' - i bufferopløsningen blev ændret for at udnytte en egenskab kaldet isotopisk kontrastvariation. Neutroner spredes forskelligt af hydrogen- og deuteriumatomer og ved at ændre forholdet mellem H2O og D2O i bufferen kan refleksionssignalet fra de pågældende molekyler forbedres i forhold til spredningen fra opløsningen. Dette tillader erhvervelse af unik struktur- og sammensætningsinformation, der ikke kan bestemmes ved nogen anden eksperimentel teknik.
 Varme artikler
Varme artikler
-
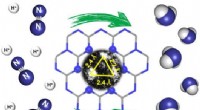 Forskere foreslår nano-indeslutningsstrategi for at danne sub-nanometer-reaktorerTEM billede af et tredobbelt atom aktivt center og den skematiske illustration af en sub-nanometer reaktor, der er vært for det til katalysering af NRR. Kredit:LIANG Ji Single-atom katalysatorer (
Forskere foreslår nano-indeslutningsstrategi for at danne sub-nanometer-reaktorerTEM billede af et tredobbelt atom aktivt center og den skematiske illustration af en sub-nanometer reaktor, der er vært for det til katalysering af NRR. Kredit:LIANG Ji Single-atom katalysatorer ( -
 Præcisionskontrol af komplekse elektrokemiske grænseflader til separationerKredit:CC0 Public Domain Forskere, der arbejder inden for Pacific Northwest National Laboratorys (PNNLs) Separations Science-program lykkedes med at koble en meget kontrolleret måde at modificere
Præcisionskontrol af komplekse elektrokemiske grænseflader til separationerKredit:CC0 Public Domain Forskere, der arbejder inden for Pacific Northwest National Laboratorys (PNNLs) Separations Science-program lykkedes med at koble en meget kontrolleret måde at modificere -
 Betydningen af internationale standarder for grafensamfundetKredit:Pixabay/CC0 Public Domain NPL, i samarbejde med internationale partnere, har udviklet en ISO/IEC standard, ISO/TS 21356-1:2021, til måling af de strukturelle egenskaber af grafen, sælges ty
Betydningen af internationale standarder for grafensamfundetKredit:Pixabay/CC0 Public Domain NPL, i samarbejde med internationale partnere, har udviklet en ISO/IEC standard, ISO/TS 21356-1:2021, til måling af de strukturelle egenskaber af grafen, sælges ty -
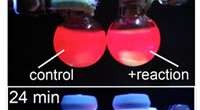 Kemikere tilføjer farve til kemiske reaktionerEn fototidslinje for reaktionsovervågning ved hjælp af perovskitfluorescens. Kredit:Syracuse University News Services Kemikere ved Syracuse University er kommet med en innovativ ny måde at visuali
Kemikere tilføjer farve til kemiske reaktionerEn fototidslinje for reaktionsovervågning ved hjælp af perovskitfluorescens. Kredit:Syracuse University News Services Kemikere ved Syracuse University er kommet med en innovativ ny måde at visuali
- Spionerer den nye dukke på dine børn?
- Stimulering af differentieringen af knogleprækursorer med organisk modificeret hydroxyapatit (orm…
- Chaufføradfærd påvirker trafikmønstre lige så meget som vejbanedesign, undersøgelsesrapporter
- Modulær platform til montering af biosensorer
- EPCOT var Walt Disneys radikale vision for en ny slags by
- Energetiske partikler kan bombardere exoplaneter


