Hitchhiking nanorør viser hvordan celler omrører sig selv
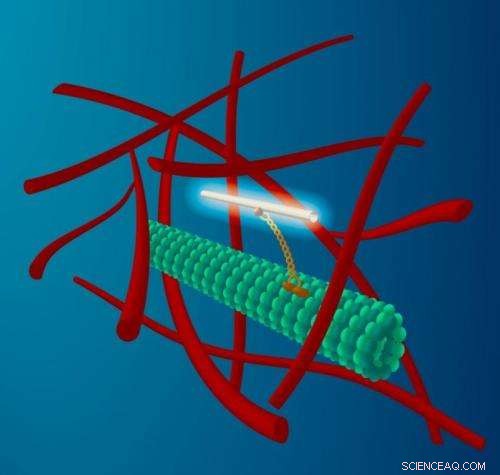
Et tyndt kulnanorør er fastgjort til en molekylær motor (gul), der bevæger sig langs mikrotubuli -filamenter (grøn), der danner transportnet af celler. Denne transport sker i det meget overfyldte miljø i cytoplasmaet, der omfatter et netværk af aktinfilamenter (rødt). Det fluorescerende nanorør fungerer som et fyrtårn for både transporten langs mikrotubuli, samt buffering af mikrotubuli ved den stærkt omrørte omgivende cytoplasma. Kredit:M. Leunissen, Hollandsk datadesign
(Phys.org) —Kemiske ingeniører fra Rice University og biofysikere fra Georg-August Universität Göttingen i Tyskland og VU University Amsterdam i Holland har med succes sporet enkeltmolekyler inde i levende celler med carbon nanorør.
Gennem denne nye metode, forskerne fandt ud af, at celler omrører deres interiør ved hjælp af de samme motoriske proteiner, der tjener til muskelsammentrækning.
Studiet, som kaster nyt lys over biologiske transportmekanismer i celler, vises i denne uge i Videnskab .
Teamet knyttet carbon nanorør til at transportere molekyler kendt som kinesin motorer for at visualisere og spore dem, da de bevægede sig gennem cytoplasma af levende celler.
"Jeg er overrasket over, hvor alsidige carbon nanorør er, "sagde medforfatter Matteo Pasquali, en Rice-professor i kemisk og biomolekylær teknik og i kemi. "Vi bruger dem til en bred vifte af applikationer, fra konstruktion af ledende fibre til billeddannelse i celler."
Carbon nanorør er hule cylindre af rent kulstof med et atom-tykke vægge. De fluorescerer naturligt med nær-infrarøde bølgelængder, når de udsættes for synligt lys, en ejendom opdaget ved Rice af professor Rick Smalley for et årti siden og derefter udnyttet af risprofessor Bruce Weisman til at afbilde kulstofnanorør. Når det er knyttet til et molekyle, blaffer nanorørene fungerer som små pejlemærker, der kan spores præcist over lange perioder for at undersøge små, tilfældige bevægelser inde i celler.
"Enhver sonde, der kan spænde cellens længde og bredde, groft det, slum det, kæmpe mod frygtelige odds, vinde igennem og stadig vide, hvor dets protein er, er helt klart en sonde at regne med, "sagde hovedforfatter Nikta Fakhri, parafrasere "The Hitchhiker's Guide to the Galaxy." Fakhri, som fik sin Rice-doktorgrad i Pasqualis laboratorium i 2011, er i øjeblikket en Human Frontier Science Program Fellow i Göttingen.
"Faktisk, den exceptionelle stabilitet af disse prober gjorde det muligt at observere intracellulære bevægelser fra tider så korte som millisekunder til så lange som timer, " hun sagde.
Til langdistancetransport, såsom langs nervecellernes lange axoner, celler anvender normalt motorproteiner bundet til lipidvesikler, cellens "lastcontainere". Denne proces involverer betydelig logistik:Last skal pakkes, fastgjort til motorerne og sendt af sted i den rigtige retning.
"Denne forskning har hjulpet med at afdække yderligere meget enklere mekanisme til transport i cellens indre, " sagde hovedefterforsker Christoph Schmidt, professor i fysik ved Göttingen. "Celler omrører sig kraftigt, meget på den måde, som en kemiker ville fremskynde en reaktion ved at ryste et reagensglas. Dette vil hjælpe dem med at flytte objekter rundt i det meget overfyldte mobilmiljø. "
Forskerne viste, at den samme type motorprotein, der bruges til muskelsammentrækning, er ansvarlig for omrøring. De nåede denne konklusion efter at have udsat cellerne for lægemidler, der undertrykte disse specifikke motoriske proteiner. Testene viste, at omrøringen også blev undertrykt.
Det mekaniske cytoskelet af celler består af netværk af proteinfilamenter, som actin. Inden i cellen, det motoriske protein myosin danner bundter, der aktivt kontraherer aktin-netværket i korte perioder. Forskerne fandt tilfældig klemning af det elastiske aktinnetværk af mange myosinbundter resulteret i den globale interne omrøring af cellen. Både actin og myosin spiller en lignende rolle i muskelsammentrækning.
De meget præcise målinger af interne udsving i cellerne blev forklaret i en teoretisk model udviklet af VU-medforfatter Fred MacKintosh, der brugte cytoskeletets elastiske egenskaber og motorernes kraftgenererende egenskaber.
"Den nye opdagelse fremmer ikke kun vores forståelse af celledynamik, men peger også på interessante muligheder for at designe 'aktive' tekniske materialer, "sagde Fakhri, som snart vil slutte sig til Massachusetts Institute of Technology fakultet som adjunkt i fysik. "Forestil dig en mikroskopisk biomedicinsk enhed, der blander bittesmå blodprøver med reagenser for at opdage sygdom eller smarte filtre, der adskiller squishy fra stive materialer."
 Varme artikler
Varme artikler
-
 Bedre katalysator for solcelledrevet brintproduktionKugle-og-stik-repræsentation af nanoskala-klynger i kobolt-baseret tynd film ved hjælp af boratelektrolyt (røde kugler er oxygen, blå kugler er kobolt) (Phys.org) — Hydrogen er et grønt brændstof,
Bedre katalysator for solcelledrevet brintproduktionKugle-og-stik-repræsentation af nanoskala-klynger i kobolt-baseret tynd film ved hjælp af boratelektrolyt (røde kugler er oxygen, blå kugler er kobolt) (Phys.org) — Hydrogen er et grønt brændstof, -
 Beregninger afslører, hvordan blandinger af forskellige grundstoffer kan kontrollere de termiske eg…Fononer (vibrationer) er typisk ansvarlige for at transportere varme langs en nanotråd. A*STAR-forskere har brugt en numerisk model til at beregne effekterne af kortrækkende bestilling på fononadfærd.
Beregninger afslører, hvordan blandinger af forskellige grundstoffer kan kontrollere de termiske eg…Fononer (vibrationer) er typisk ansvarlige for at transportere varme langs en nanotråd. A*STAR-forskere har brugt en numerisk model til at beregne effekterne af kortrækkende bestilling på fononadfærd. -
 Nanoteknologisk gennembrud muliggør konvertering af infrarødt lys til energiEt nærbillede af filmen, der kombinerer nanokrystaller og mikrolinser for at fange infrarødt lys og omdanne det til solenergi. Kredit:KTH Kgl. Teknologisk Institut Usynligt infrarødt lys står for
Nanoteknologisk gennembrud muliggør konvertering af infrarødt lys til energiEt nærbillede af filmen, der kombinerer nanokrystaller og mikrolinser for at fange infrarødt lys og omdanne det til solenergi. Kredit:KTH Kgl. Teknologisk Institut Usynligt infrarødt lys står for -
 Zebrafiskembryoner hjælper med at bevise, hvad der sker med nanopartikler i blodetFluorescensmærkede 70 nm SiO2 nanopartikler blev injiceret i blodbanen af 3 dage gamle transgene zebrafisk embryoner og live-billede 3 minutter efter injektionen. Indsætningerne viser skemaer for de
Zebrafiskembryoner hjælper med at bevise, hvad der sker med nanopartikler i blodetFluorescensmærkede 70 nm SiO2 nanopartikler blev injiceret i blodbanen af 3 dage gamle transgene zebrafisk embryoner og live-billede 3 minutter efter injektionen. Indsætningerne viser skemaer for de
- Endelig, 3D-printede graphene aerogeler til vandbehandling
- Typer af svejsemetaller
- Optogenetik – at kontrollere neuroner med lys – kan føre til helbredelse af PTSD, Alzheimers
- Billede:Hubble sporer en galakses yderområder
- Satellit ser Eastern Pacific Depression 10E form
- Sådan beregnes det isoelektriske punkt af peptider


