Forskers nanopartikelnøgle til ny malariavaccine
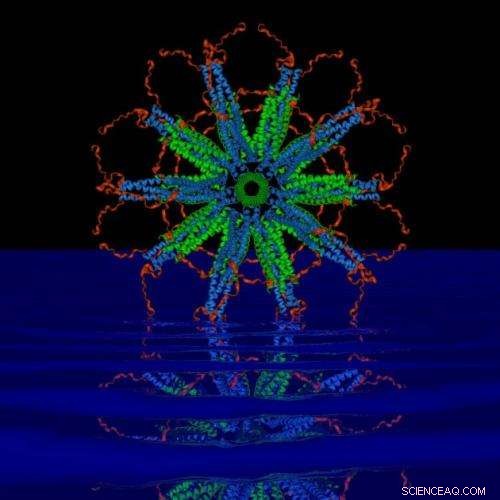
Denne selvsamlende protein-nanopartikel er afhængig af stive proteinstrukturer kaldet 'spiralspoler' (blå og grøn i billedet) for at skabe en stabil ramme, som forskere kan vedhæfte malariaparasitantigener på. Tidlige tests viser, at indsprøjtning af nanopartikler i kroppen som en vaccine initierer et stærkt immunsystemrespons, der ødelægger en malariaparasit, når den kommer ind i kroppen, og inden den når at sprede sig. Kredit:Peter Burkhard
En selvsamlende nanopartikel designet af en UConn-professor er nøglekomponenten i en potent ny malariavaccine, der viser lovende i tidlige tests.
Årevis, forskere, der forsøger at udvikle en malariavaccine, er blevet dæmpet af malariaparasitens evne til at transformere sig selv og "gemme sig" i leveren og røde blodlegemer hos en inficeret person for at undgå påvisning af immunsystemet.
Men en ny protein -nanopartikel udviklet af Peter Burkhard, professor i Institut for Molekylær &Cellebiologi, i samarbejde med David Lanar, en specialist i infektionssygdom ved Walter Reed Army Institute of Research, har vist sig at være effektiv til at få immunsystemet til at angribe de mest dødelige arter af malariaparasitter, Plasmodium falciparum, efter det kommer ind i kroppen, og før det har en chance for at skjule sig og aggressivt sprede sig.
Nøglen til vaccinens succes ligger i nanopartikelens perfekte icosahedral symmetri (tænk på mønsteret på en fodbold) og evnen til at bære op til 60 kopier af parasitens protein på overfladen. Proteinerne er arrangeret i en tæt, omhyggeligt konstrueret klynge, som immunsystemet opfatter som en trussel, får det til at frigive store mængder antistoffer, der kan angribe og dræbe parasitten.
I test med mus, vaccinen var 90-100 procent effektiv til at udrydde Plasmodium falciparum-parasitten og opretholde langvarig immunitet over 15 måneder. Denne succesrate er betydeligt højere end den rapporterede succesrate for RTS, S, verdens mest avancerede malariavaccinkandidat, der i øjeblikket gennemgår fase 3 kliniske forsøg, som er den sidste fase af testen før licensering.
"Begge vacciner ligner hinanden, det er bare, at densiteten af RTS, S -proteindisplays er meget lavere end vores, "siger Burkhard." Homogeniteten af vores vaccine er meget højere, som producerer et stærkere immunsystemrespons. Derfor er vi overbeviste om, at vores vil blive en forbedring.
"Hver eneste proteinkæde, der danner vores partikel, viser et af patogenets proteinmolekyler, der genkendes af immunsystemet, "tilføjer Burkhard, en ekspert i strukturbiologi tilknyttet UConn's Institute of Materials Science. "Med RTS, S, kun omkring 14 procent af vaccinens protein er fra malariaparasitten. Vi er i stand til at opnå vores høje densitet på grund af designet af nanopartiklen, som vi kontrollerer. "
Undersøgelsen blev offentliggjort i Malaria Journal i 2013.
Søgningen efter en malariavaccine er et af de vigtigste forskningsprojekter inden for global folkesundhed. Sygdommen transporteres almindeligvis gennem bid af myg om natten. De smittede lider af svær feber, kuldegysninger, og en influenzalignende sygdom. I alvorlige tilfælde, malaria forårsager anfald, alvorlig anæmi, åndedrætsbesvær, og nyresvigt. Hvert år, mere end 200 millioner tilfælde af malaria er rapporteret på verdensplan. Verdenssundhedsorganisationen anslog, at 627, 000 mennesker døde af malaria i 2012, mange af dem børn, der bor i Afrika syd for Sahara.
Det tog forskerne mere end 10 år at afslutte den nøjagtige samling af nanopartiklen som den kritiske bærer af vaccinen og finde de rigtige dele af malariaproteinet til at udløse et effektivt immunrespons. Forskningen blev yderligere kompliceret af det faktum, at malariaparasitten, der påvirker mus, der bruges i laboratorietest, strukturelt er forskellig fra den, der inficerer mennesker.
Forskerne brugte en kreativ tilgang til at komme uden om problemet.
"At teste vaccinens effektivitet var svært, fordi parasitten, der forårsager malaria hos mennesker, kun vokser hos mennesker, "Lanar siger." Men vi udviklede et lille trick. Vi tog en malariaparasit fra en mus og satte et stykke DNA fra den menneskelige malariaparasit i dens DNA, som vi ønskede, at vores vaccine skulle angribe. Det gav os mulighed for at foretage billige musestudier for at teste vaccinen, inden vi gik til dyre forsøg med mennesker. "
Parrets forskning er blevet støttet af et tilskud på $ 2 millioner fra National Institutes of Health og $ 2 millioner fra det amerikanske forskningsprogram for militær infektionssygdom. En anmodning om yderligere 7 millioner dollar i finansiering fra den amerikanske hær til at gennemføre den næste fase af vaccinens udvikling, herunder fremstilling og forsøg med mennesker afventer.
"Vi er på planen til at fremstille vaccinen til human brug tidligt næste år, "siger Lanar." Det vil tage omkring seks måneder at afslutte kvalitetskontrol og toksikologiske undersøgelser af det endelige produkt og få tilladelse fra FDA til at lave forsøg på mennesker. "
Lanar siger, at teamet håber at begynde tidlig testning på mennesker i 2016 og, hvis resultaterne er lovende, feltforsøg i endemiske malariaområder vil følge i 2017. Den krævede feltforsøgstest kan vare fem år eller mere, før vaccinen er tilgængelig til licens og offentlig brug, Siger Lanar.
Martin Edlund, CEO for Malaria No More, en New York-baseret nonprofit fokuseret på at bekæmpe dødsfald som følge af malaria, siger, "Denne forskning præsenterer en lovende ny tilgang til udvikling af en malariavaccine. Innovativt arbejde som f.eks. Hvad der udføres på University of Connecticut bringer os tættere på end vi nogensinde har været for at afslutte en af verdens ældste, dyreste, og dødeligste sygdomme. "
En virksomhed i Schweiz, Alpha-O-peptider, grundlagt af Burkhard, har patent på den selvsamlende nanopartikel, der bruges i malariavaccinen. Burkhard undersøger også andre potentielle anvendelser for nanopartiklen, herunder en vaccine, der vil bekæmpe dyreinfluenza og en, der vil hjælpe mennesker med nikotinafhængighed. Professor Mazhar Khan fra UConn's afdeling for patobiologi samarbejder med Burkhard om vaccinen mod influenza fra dyr.
 Varme artikler
Varme artikler
-
 Selvsamling af guld nanopartikler i små klyngerEt kryogenisk TEM-mikrografi af guldnanopartikler i DES-opløsningsmiddel. Sputteringsvarighed 300 s. Røde cirkler viser de forskellige domæner af selvsamlede Au-NPer. Indsatsen viser et forstørret bil
Selvsamling af guld nanopartikler i små klyngerEt kryogenisk TEM-mikrografi af guldnanopartikler i DES-opløsningsmiddel. Sputteringsvarighed 300 s. Røde cirkler viser de forskellige domæner af selvsamlede Au-NPer. Indsatsen viser et forstørret bil -
 Forskere producerer ensartede antimon-nanokrystaller til energilagringForskere fra Empa og ETH Zürich er for første gang lykkedes med at fremstille ensartede antimon-nanokrystaller. Testet som komponenter i laboratoriebatterier, disse er i stand til at opbevare et stort
Forskere producerer ensartede antimon-nanokrystaller til energilagringForskere fra Empa og ETH Zürich er for første gang lykkedes med at fremstille ensartede antimon-nanokrystaller. Testet som komponenter i laboratoriebatterier, disse er i stand til at opbevare et stort -
 Grafen dobbeltlag giver effektiv transport og kontrol af spinsIllustration af anisotrop spintransport i en tolags grafenflage mellem injektor- og detektorelektroder. Ud-af-plan-spindene overføres godt, mens in-plane-spindene henfalder hurtigt. Kredit:Talieh Ghia
Grafen dobbeltlag giver effektiv transport og kontrol af spinsIllustration af anisotrop spintransport i en tolags grafenflage mellem injektor- og detektorelektroder. Ud-af-plan-spindene overføres godt, mens in-plane-spindene henfalder hurtigt. Kredit:Talieh Ghia -
 Ny mikrostråleudsender har potentiale til at bringe lovende form for strålebehandling i klinisk br…Mikrostrålebehandling doserer området med tynde parallelle strålingsplaner, op til et par hundrede mikrometer i bredden, skabe et stribet mønster af bestråling på tværs af tumoren. (Phys.org) — Mi
Ny mikrostråleudsender har potentiale til at bringe lovende form for strålebehandling i klinisk br…Mikrostrålebehandling doserer området med tynde parallelle strålingsplaner, op til et par hundrede mikrometer i bredden, skabe et stribet mønster af bestråling på tværs af tumoren. (Phys.org) — Mi
- Styring af krystalstørrelsen af organiske halvledere
- Opstart af software på arbejdspladsen Slack vurderet til $7,1 mia. i ny finansiering
- Tiden er moden! En innovativ kontaktløs metode til rettidig høst af bløde frugter
- Opdagelse af ondsindede websider
- Forskere finder rekordvarmt vand i Antarktis, peger på årsag bag bekymrende gletsjersmeltning
- NASA kommer tæt på med Grønlands smeltende is


