Nanopartikler ved specifik temperatur stimulerer antitumorrespons
Søger en måde at stimulere antitumorresponser via immunsystemet, Steven Fiering, PhD, af Norris Cotton Cancer Center i Dartmouth, har identificeret den præcise temperatur, der resulterer i en distinkt kropsdækkende antitumor-immunrespons, der modstår metastatisk sygdom. Fierings team offentliggjorde forskningen i papiret "Local Hyperthermia Treatment of Tumors Induces CD8+ T Cell-Mediated Resistance Against Distale and Secondary Tumors, " som dukkede op i Nanomedicin:Nanoteknologi, Biologi og medicin .
"Mild hypertermi behandling af en identificeret tumor, før operation for at fjerne tumoren, viser fremragende løfte om at styrke antitumorresponset og hjælpe med at stoppe metastatisk sygdom, " forklarede Fiering.
Blandt de mange muligheder for kræftbehandling, som videnskaben forfølger, immunterapi er et nutidigt fokus. Immunsystemet genkender og eliminerer normalt små tumorer, men andre tumorer bliver til kliniske problemer og er kendt for at blokere antitumor-tendenserne med et naturligt system til immunsuppression. For nylig, forskere har arbejdet på at lære, hvordan man kan vende denne tumor-medierede immunsuppression. Ud over, fagocytter (nøgleaktører i immunsuppression og immunstimulering, og som hurtigt optager nanopartikler) har givet muligheder for nye strategier. Fierings undersøgelser blev udført i mus med en melanom tumormodel, og begyndte med at indsætte jernnanopartikler direkte i tumorerne, mens der blev påført et vekslende magnetfelt for at opvarme nanopartiklerne jævnt og ved præcise temperaturer.
"Selvom det er let at anvende nok varme til at ødelægge tumoren, den slags termisk ablation har ikke det resultat, vi ledte efter, som skulle stimulere et systemisk immunrespons for at eliminere metastatisk sygdom, " sagde Fiering. "Når man ser på temperaturvariabler, vi lærte, at ved præcis 43 grader celsius, det systemiske immunrespons træder i kraft. At gøre dette sikkert er en potent behandlingstilgang, der kan stimulere immunsystemet til at bekæmpe ubehandlede metastatiske tumorer."
Fiering brugte Dartmouths delte ressourcer inklusive den transgene muse-ressource til at udføre musemanipulationer. Kollega P. Jack Hoopes fra Dartmouths Thayer School of Engineering leverede det livsvigtige udstyr til alternerende magnetfelter. Dartmouth Shared Resources er åbne for eksterne efterforskere efter aftale.
Ved at bruge Norris Cotton Cancer Centers holdvidenskabelige tilgang, Fiering og Hoopes ser frem til fælles undersøgelser, der tester det systemiske immunrespons på nanopartikelbehandling hos hunde med melanom. Som hos mennesker, melanom er ofte metastaserende og dødelig for hunde. Hvis det systemiske immunrespons kan påvises at forhindre metastatisk sygdom hos hunde, det vil være klar til at udvikle til kliniske forsøg på mennesker.
 Varme artikler
Varme artikler
-
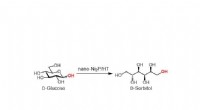 Nikkelphosphid nanopartikelkatalysator er den fulde pakkeFigur 1. Hydrogenering af D-glucose til D-sorbitol. Kredit:Osaka University De fleste katalysatorer, der fremmer omdannelsen af glucose til sorbitol, tilbyder visse egenskaber, mens de kræver ko
Nikkelphosphid nanopartikelkatalysator er den fulde pakkeFigur 1. Hydrogenering af D-glucose til D-sorbitol. Kredit:Osaka University De fleste katalysatorer, der fremmer omdannelsen af glucose til sorbitol, tilbyder visse egenskaber, mens de kræver ko -
 Belægning af nanorør med aluminiumoxid nedsætter risikoen for lungeskadeBillede af et flervægget kulstof nanorør. Billedkredit:Eric Wieser, via WikiMedia Commons. (Phys.org) — En ny undersøgelse fra North Carolina State University og National Institute of Environmenta
Belægning af nanorør med aluminiumoxid nedsætter risikoen for lungeskadeBillede af et flervægget kulstof nanorør. Billedkredit:Eric Wieser, via WikiMedia Commons. (Phys.org) — En ny undersøgelse fra North Carolina State University og National Institute of Environmenta -
 Grafenfotoniks gennembrud lover høj hastighed, lavpris kommunikation(Phys.org) —Swinburne-forskere har udviklet en højkvalitets kontinuerlig grafenoxid-tynd film, der viser potentiale for ultrahurtig telekommunikation. Lektor Baohua Jia ledede et team af forskere fra
Grafenfotoniks gennembrud lover høj hastighed, lavpris kommunikation(Phys.org) —Swinburne-forskere har udviklet en højkvalitets kontinuerlig grafenoxid-tynd film, der viser potentiale for ultrahurtig telekommunikation. Lektor Baohua Jia ledede et team af forskere fra -
 Graphenes Big Mac skaber næste generation af chipsKunstnerisk indtryk af grafenmolekyler. Kredit:University of Manchester Verdens tyndeste, stærkeste og mest ledende materiale, opdaget i 2004 ved University of Manchester af professor Andre Geim o
Graphenes Big Mac skaber næste generation af chipsKunstnerisk indtryk af grafenmolekyler. Kredit:University of Manchester Verdens tyndeste, stærkeste og mest ledende materiale, opdaget i 2004 ved University of Manchester af professor Andre Geim o
- Edinburgh Zoo:panda Tian Tian føder ikke i år
- Den nanomekaniske signatur af brystkræft
- Ny løsning på skadelig algeopblomstring giver håb om økonomiske og miljømæssige fordele
- Sådan fordeles eksponenter med forskellige baser
- Sexarbejderes rettigheder:Hysteri, overvågning og trusler mod grundlæggende frihedsrettigheder
- Opvarmning af vores klima skader vores økonomier:Undersøgelse afslører større omkostninger end f…


