Handel in vivo for in silico - en ny tilgang til vurdering af nanotoksicitet
Prof. Robert Rallo, koordinator for MODERN-projektet, diskuterer initiativets nye tilgang til vurdering af nanotoksicitet, som kunne hjælpe os i retning af en bredere anvendelse af in silico-metoder.
MODERN-projektet har sat sig for bedre at forstå, hvordan nanopartikler påvirker miljøet og menneskers sundhed. Deres nye tilgang, som er afhængig af nye beregningsmetoder til at karakterisere strukturen af nanopartikler og i silico-modeller til at vurdere deres virkninger, lover også at reducere behovet for in vivo test.
Historisk set, markedspres har ofte resulteret i, at videnskabelig innovation er blevet gjort tilgængelig for forbrugerne, selv før vi var fuldt ud klar over dens ins og outs. Dette var især tilfældet med asbest, og det samme scenarie kunne meget vel gentage sig med nanoteknologi, hvis der ikke udføres ordentlige sikkerhedsvurderingsundersøgelser, og politiske foranstaltninger træffes i overensstemmelse hermed:ifølge nogle af de seneste prognoser, markedet for nanoteknologi vil vokse til at nå 75,8 (EUR 65,8) milliarder i 2020. Og mens konstruerede nanopartikler (eNP'er) allerede er udbredt i kosmetik, maling og elektronik, vi ved stadig ikke meget om deres mulige langsigtede virkninger på biologiske systemer.
For at få en bedre forståelse, videnskabsmænd er stadig stærkt afhængige af dyreforsøg – på trods af indsatsen fra dyrebeskyttelsesaktivister, videnskabsmænd og politiske beslutningstagere til at sætte fokus på alternative testmetoder. I overensstemmelse med EU's bestræbelser på at implementere passende teststrategier og med henblik på at overvinde de nuværende hindringer for en bredere anvendelse af in silico-metoder, Prof. Robert Rallo, koordinator for MODERN, igangsatte det MODERNE projekt i januar 2013.
Et par måneder før projektets afslutning, han fortæller os om dets resultater og forventede indvirkning på eNP-toksicitetsvurderingsmetoder.
Vil du sige, der bliver gjort nok i Europa for at måle toksiciteten af eNP'er, før de kommer på markedet?
I de senere år har EU iværksat en betydelig indsats med det formål at definere de videnskabelige og metodiske principper for in vitro og in vivo test af nanomaterialer. Selvom der stadig mangler specifikke regler vedrørende brugen af nanoteknologi-aktiverede produkter, EU er på vej mod at skabe et grundlag for implementering af passende teststrategier, der vil understøtte risikovurdering og lovgivningsmæssig beslutningstagning.
Mangfoldigheden af nanomaterialer (f.eks. forskellige kombinationer af kemisk sammensætning, kerne-skal struktur, form, funktionalisering) gør den udtømmende test af nanomaterialer til en skræmmende opgave. I denne sammenhæng, udvikling og validering af high throughput screeningmetoder sammen med implementering af in silico værktøjer (som dem, der er udviklet i MODERN og i andre FP7 NMP modelleringsprojekter) vil i den nærmeste fremtid bidrage til at levere alternative testmetoder, der er egnede til evaluering af en stor antal nanomaterialer på en effektiv og omkostningseffektiv måde.
Hvorfor er eNP-toksicitetsvurdering så meget afhængig af dyreforsøg?
Hovedårsagen er, at nuværende in vitro-assays og in silico-værktøjer endnu ikke er accepteret som pålidelige modelsystemer for nanomaterialtoksicitet. Håndtering af "biologisk støj" (dvs. datavariabilitet) i in vitro high-throughput assays er en af de mest presserende udfordringer, der skal løses. Derudover er der et lige så påtrængende behov for at udvikle store databaser med eksperimentelle data af høj kvalitet til udvikling og validering af in silico-toksicitetsforudsigelsesværktøjer.
Hvordan har du tænkt dig at udfylde dette hul?
Hos MODERN udvikler vi i silico værktøjer til vurdering af nanotoksicitet ved at bruge forskellige typer information om nanopartikler. Projektet følger en integreret tilgang, der kombinerer forskellige typer information inden for rammerne af specifikke Adverse Outcome Pathways. Specifikt fokuserer vi på nanotoksicitetseffekter drevet af oxidative stressreaktioner. Vi har udviklet nye metoder til beregning af størrelsesafhængige nanodeskriptorer ved hjælp af kvantekemi og molekylære modelleringstilgange, samt nano-(Q)SAR baseret på deskriptorerne udviklet til en række økotoksicitets-endepunkter i forskellige arter, herunder protozoer, alger og bakterier.
En anden præstation er udviklingen af en ny normaliseringsmetodologi for omics-data, der er nyttig til at afsløre gen- og pathway-aktivitet ved lav koncentration (dvs. under realistiske miljøeksponeringsforhold). Modeller til forudsigelse af nanopartikelcelleinteraktioner baseret på sammensætningen af nanopartiklernes proteinkorona er også blevet udviklet og valideret. Endelig, vi forsøger at øge nøjagtigheden af nuværende modeller ved at identificere homogene kategorier af nanopartikler og udvikle nye lokale modeller for hver specifik kategori.
Lever de modeller, du har udviklet, op til dine oprindelige forventninger?
Vi har vist, at integrationen af forskellige typer information (f.eks. fysisk-kemiske egenskaber, strukturelle egenskaber og bioaktivitetsprofiler på forskellige niveauer af biologisk organisation) vedrørende nanopartiklers virkninger er grundlæggende for udviklingen af in silico-værktøjer, der er egnede til risikovurdering af nanomaterialer og beslutningstagning.
Da beregningsmodeller kan guide design af nye nanopartikler med kontrolleret toksicitet, in silico værktøjer kan også anvendes til sikre-by-design nanomaterialer. Der er dog stadig en betydelig mangel på (offentlig) information om nanopartiklers toksicitet, der gør det muligt for modeller at blive ordentligt vurderet og deres anvendelighedsdomæne udvidet. Som en konsekvens, nuværende modeller kan kun bruges som foreløbige screeningsværktøjer, der giver en indikation af de potentielle negative virkninger af et nanomateriale. Yderligere in vitro (og muligvis in vivo) test vil være nødvendigt for at bekræfte, hvorvidt en given nanopartikel har toksicitetsimplikationer.
Ville du være enig med forskere, der siger, at det er umuligt helt at stoppe med at bruge dyreforsøg, når det kommer til ENP-toksicitetsvurdering?
Lige nu er svaret ja. In vivo test vil være nødvendigt for at sikre sikkerheden af nanoteknologi-aktiverede produkter, især for de nanopartikler, der bruges i medicinske applikationer. Imidlertid, udviklingen af mere robuste in vitro-assays kombineret med in silico-forudsigelsesværktøjer vil have potentialet til at bidrage til en betydelig reduktion i antallet af dyr, der bruges til test.
I den nærmeste fremtid, med den kontinuerlige stigning i computerkraft og med forbedret forståelse af nano-bio-interaktionsmekanismerne, Jeg er overbevist om, at vi vil være i stand til at udføre nøjagtige simuleringer af interaktionerne mellem nanopartikler og biologiske systemer, som vil have potentialet til fuldstændig at erstatte dyreforsøg.
Hvad vil du sige er de vigtigste ting, du har lært af din forskning indtil videre?
Den første og vigtigste lektie er, at vores forståelse og modelleringskapacitet for nanotoksicitet stadig er langt fra, hvad vi har for kemisk toksicitet. Der er stadig en betydelig mangel på viden om nanotoksicitetsmekanismer og virkemåder. Også, mængden af tilgængelige data til modeludvikling – og endnu vigtigere, til modelvalidering - er meget begrænset sammenlignet med de tilgængelige data for kemikalier.
Der er stadig mange udfordringer, der hindrer udviklingen af in silico nanotoksicitetsscreeningsværktøjer, og den begrænsede mængde data er blot en af de begrænsende faktorer. Blandt andre, aktuelle vigtige behov omfatter udviklingen af en nomenklatur til at beskrive nanomaterialer utvetydigt; standardiserede protokoller til testning af nanotoksicitet; protokoller til high-throughput screeningsassays og deres tilknyttede dataforbehandlingsmetoder for at generere nok data til at berige og forbedre strømmen i silico-modeller; og metoder til farerangering, risikovurdering og beslutningstagning.
Hvad mangler du stadig at nå, inden projektet slutter i december?
Vi er i øjeblikket ved at evaluere den forudsigelige kapacitet af kvantekemien og molekylære modelleringsdeskriptorer for de metaloxidnanopartikler, vi har udviklet indtil videre. Beregningsmetoderne til at generere nanodeskriptorerne bliver også forfinet for at inkorporere strukturelle ændringer såsom metaldoping. Sideløbende bruger vi information opnået fra nanopartikelkategorisering til at udvikle ensemble nanotoksicitetsmodeller baseret på en samling af lokalt indstillede nano-QSAR'er. Oplysningerne fra disse modeller vil derefter blive brugt i en sidste fase til at levere farerangering og foreløbige risikovurderingsværktøjer for nanomaterialer.
Sidste artikelGadolinium-baserede partikler viser og behandler tumorer
Næste artikelGrafen flager som et ultrahurtigt stopur
 Varme artikler
Varme artikler
-
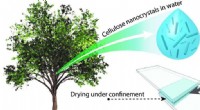 En kombination af plantebaserede partikler og vand danner en øko-limgrundlæggende demonstrationsgrafik. Kredit:Aalto University I en undersøgelse offentliggjort i Avancerede materialer , forskere ved Aalto University, universitetet i Tokyo, Sichuan University og
En kombination af plantebaserede partikler og vand danner en øko-limgrundlæggende demonstrationsgrafik. Kredit:Aalto University I en undersøgelse offentliggjort i Avancerede materialer , forskere ved Aalto University, universitetet i Tokyo, Sichuan University og -
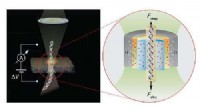 Forbedret afkodning af DNA til tilpassede medicinske behandlingerDen opto-elektriske effekt kan bruges til at kontrollere passagen af DNA-molekyler gennem nanopore-sensorer, hvilket fører til mere nøjagtig sansning og sekventering af individuelle DNA-molekyler.
Forbedret afkodning af DNA til tilpassede medicinske behandlingerDen opto-elektriske effekt kan bruges til at kontrollere passagen af DNA-molekyler gennem nanopore-sensorer, hvilket fører til mere nøjagtig sansning og sekventering af individuelle DNA-molekyler. -
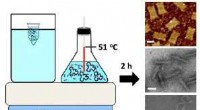 DNA origami innovation øger tilgængeligheden, sænker omkostningerneOhio State forskere har udviklet en ny tilgang til at fremstille DNA-origami ved hjælp af billigt og bredt tilgængeligt udstyr såsom varmeplader, vandbade og laboratoriebrændere. Kredit:Ohio State Uni
DNA origami innovation øger tilgængeligheden, sænker omkostningerneOhio State forskere har udviklet en ny tilgang til at fremstille DNA-origami ved hjælp af billigt og bredt tilgængeligt udstyr såsom varmeplader, vandbade og laboratoriebrændere. Kredit:Ohio State Uni -
 porøs, lagdelt materiale kan tjene som en grafenanalogSet fra oven (venstre) og set fra siden (højre), illustrerer den porøse og lagdelte struktur af et stærkt ledende pulver, forløber for en ny, indstillelig grafen analog. Kredit:Mircea Dincă, Massachus
porøs, lagdelt materiale kan tjene som en grafenanalogSet fra oven (venstre) og set fra siden (højre), illustrerer den porøse og lagdelte struktur af et stærkt ledende pulver, forløber for en ny, indstillelig grafen analog. Kredit:Mircea Dincă, Massachus
- Nanostrukturdesign gør det muligt for pixels at producere to forskellige farver
- Forsøger ikke at fnugle det:Håndtering af plastmikrofibre
- Team syntetiserer samtidigt dicarboxylsyrer og hydrogen fra dioler
- Pluto-bjergene er snedækkede, men ikke af de samme grunde som på Jorden
- Billede:Halvmåne Jupiter med den store røde plet
- Påvirker politisk overbevisning social distancering?


