Hvordan nanoteknologi kunne opdage og behandle kræft

Kredit:Christian Northeast
Et voksende felt kaldet nanoteknologi gør det muligt for forskere at manipulere molekyler og strukturer, der er meget mindre end en enkelt celle for at forbedre vores evne til at se, overvåge og ødelægge kræftceller i kroppen.
Besætningen på Proteus har en desperat chance for at redde en mands liv. Krympet til størrelsen af en stor bakterie, ubåden indeholder et hold af videnskabsmænd og læger, der ræser for at ødelægge en blodprop i hjernen på en sovjetisk afhopper. Gruppen rejser gennem kroppen, undgå gigantiske hvide blodlegemer og bittesmå antistoffer, mens de rejser gennem hjertet, det indre øre og hjernen for at nå og ødelægge blokeringen.
Selvom begivenheder i filmen Fantastisk rejse var langt ude, da den blev udgivet i 1966, de bliver nu realiseret hver dag i laboratorier rundt om i verden, især i kræftbehandling. Et voksende felt kaldet nanoteknologi gør det muligt for forskere at manipulere molekyler og strukturer, der er meget mindre end en enkelt celle for at forbedre vores evne til at se, overvåge og ødelægge kræftceller i kroppen.
Titusindvis af patienter har allerede modtaget kemoterapi medicin leveret af nanopartikler kaldet liposomer, og snesevis af andre tilgange er i øjeblikket i kliniske forsøg. Inden for de næste fem til 10 år, vores krops største forsvarsspillere kan være mindre end vi nogensinde kunne have forestillet os.
'Udsøgt følsomhed og præcision'
"Nanoteknologi tilbyder en udsøgt følsomhed og præcision, som er svær at matche med enhver anden teknologi, " sagde Sam Gambhir, MD, PhD, professor og formand for radiologi ved Medicinsk Institut. "Inden for det næste årti, nanomedicin vil ændre vejen for kræftdiagnose og behandling i dette land."
Feltet har nogle store bagmænd:National Cancer Institute bruger nu omkring 150 millioner dollars hvert år på nanoteknologisk forskning og træning for at bekæmpe sygdommen; andre institutter og centre ved National Institutes of Health bruger yderligere 300 millioner dollars på nanoteknologisk forskning for kræft og andre lidelser. Og en national alliance skabt af NCI i 2004 for at samle forskere fra biologi til datalogi til kemi til teknik bærer nu frugt – i form af snesevis af kliniske forsøg – på campusser og virksomheder over hele landet, inklusive Stanford.
"Vi kan nu påvise blot nogle få kræft-associerede molekyler eller cirkulerende tumorceller i kroppen i blot et par milliliter blod eller spyt, eller kortlægge grænserne for en hjernetumor inden for millimeter for at vurdere dens respons på terapi eller for at planlægge en operation, " sagde Gambhir. "Vi har specielt designet nanopartikler, der kan sende en massivt forstærket, voldsomt signal, når de binder sig til kræftceller i tyktarmen, og vi arbejder på måder at udløse selvsamling af nanopartikler, når de kommer ind i en kræftcelle. Feltet er gået gevaldigt frem i de sidste 10 til 15 år."
Gambhir, Virginia og D.K. Ludwig professor i klinisk undersøgelse i kræftforskning, medleder det NCI-finansierede Stanford Center for Cancer Nanotechnology and Excellence for Translational Diagnostics med Shan Wang, PhD, en professor i materialevidenskab og teknik og i elektroteknik.
Evnen til at diagnosticere de allertidligste tegn på problemer er afgørende for bestræbelserne på at stoppe sygdommen i dens spor, før symptomer eller komplikationer opstår - hvilket er en nøglekomponent i det, der er kendt som præcisionssundhed.
"Tidlig diagnose er absolut kritisk, og kræver en helt anden type tilgang og teknologi, end vi tidligere har stolet på, " sagde Gambhir. "Uden nanomedicin, vi ville ikke have en chance for at nå vores primære mål:at holde vores hospitaler tomme."
Et spørgsmål om skala
Så hvad er så specielt ved nanoteknologi? Som du måske kan gætte, det er et spørgsmål om skala. En nanometer er en milliarddel af en meter. Et menneskehår er omkring 100, 000 nanometer i diameter. En gennemsnitlig celle, omkring 10, 000. Proteus, i Den fantastiske rejse, var omkring 1, 000 nanometer lang, og antistofferne, der angreb dens passagerer, var omkring 10 nanometer store.
Nanopartikler til medicinsk brug defineres som molekyler eller strukturer, der ikke er større end omkring 100 nanometer - sammenlignelige i størrelse med de titusindvis af molekyler i kroppen, der glider ind og ud af intakte celler og vrikker uskadeligt gennem blodkarvæggene og ind i væv. Ligesom Proteus og dens besætning, de kan opsøge og interagere med individuelle celler og deres indhold. Men reglerne for engagement er ændret, ligesom den mulige størrelse af de besøgendes effekt.
Molekyler på nanometerskalaen opererer i en mørk underverden, hvor fysikkens love slingrer ved kanten af en kvantegalakse. Elektroner opfører sig mærkeligt på sådan en lille scene. Som resultat, nanopartiklernes væsentlige egenskaber, inklusive deres farve, smeltepunkter, fluorescens, ledningsevne og kemisk reaktivitet, kan variere afhængigt af deres størrelse.
Partikler i nanoskala har også enorme mængder overfladeareal sammenlignet med større partikler. En terning af guld med sider 1 centimeter lange har et samlet overfladeareal på 6 kvadratcentimeter. Men det samme volumen fyldt med guld nanosfærer med diametre på 1 nanometer har et overfladeareal større end en halv fodboldbane.
'Tuning' nanopartikler
Forskere som Gambhir og hans kolleger har lært, hvordan man kan udnytte mange af disse egenskaber i deres søgen efter at opsøge og ødelægge kræftceller i kroppen, eller for at indsamle dem fra en blodprøve til yderligere undersøgelse. Ved at ændre størrelsen af partiklerne, forskerne kan "tune" nanopartiklerne til at opføre sig på bestemte måder - fluorescerende forskellige farver til billeddannelsesformål, for eksempel, eller gribe fat i og derefter frigive kræftceller til undersøgelse. Nogle kan konstrueres til at absorbere lysenergi for at drive små akustiske vibrationer, der signalerer tilstedeværelsen af en tumor eller til at frigive varme for at dræbe cellerne indefra.
Forskere udnytter også partiklernes enorme overfladeareal, belægning dem med antistoffer eller proteiner, der er hjemsted for kræftceller, eller med signalmolekyler, der frigives i titusindvis, når en kræftcelle lokaliseres.
Gambhir mener, at nanoteknologi vil være særlig nyttig i tidlig diagnose og behandling. "Det er ikke, at vores terapier er dårlige - det er, at vi anvender dem for sent, " sagde han. "Nanoteknologi har potentialet til at opdage og endda dræbe tidlige kræftceller, der er til stede i hundreder eller tusinder versus de milliarder, der allerede er til stede i aktuelt diagnosticerbare tumorer."
Han og hans kolleger forestiller sig en dag i en ikke alt for fjern fremtid, hvor nanosensorer implanteres i vores kroppe, eller endda i husholdningsapparater som toilettet, kan advare os om de første tegn på problemer - ofte uden vores bevidste deltagelse. Han sammenligner tilgangen med at styre et jetfly.
"Et flys motor overvåges konstant, og information sendes til en global portal for at diagnosticere problemer i realtid, " sagde han. "Det mangler vi i sundhedsvæsenet i dag."
Men måske ikke så længe.
'Sluger lægen'
Konceptet med miniature medicinske håndlangere er ikke nyt. I 1959, bemærkede fysiker Richard Feynman, PhD, diskuterede muligheden for at "sluge lægen" i en tale på California Institute of Technology, og britiske forskere indså første gang liposomers potentiale til lægemiddellevering i 1961. Disse kugler kan konstrueres til at indeholde vandopløselige lægemidler i deres indre, mens du også egern væk hydrofob, eller uopløselige, lægemidler i deres fedtmembraner. Omhyggelig konstruktion kan resultere i liposombaserede strukturer, der leverer flere lægemidler i præcise forhold og i høje niveauer uden de toksiciteter, der kan opstå, når lægemidlerne leveres uden disse strukturer. De akkumuleres naturligt i tumorvæv, eller kan målrettes til specifikke celletyper ved tilsætning af antistoffer eller andre molekyler til deres overflade.
Teknikken blev først godkendt af U.S. Food and Drug Administration i 1995 til at levere kemoterapilægemidlet doxorubicin til patienter med AIDS-relateret Kaposis sarkom. Der er nu mere end et dusin liposomalt emballerede lægemidler på markedet, og forskere er begyndt at udforske måder at bruge andre typer nanopartikler til at levere ikke kun stoffer, but also small RNA molecules to block the expression of specific genes, or a payload of radioactivity to kill the cell.
"From a practical perspective, nano-based techniques aren't the wave of the future. This is the now, " said Heather Wakelee, MD, an associate professor of medicine at Stanford who focuses on the treatment of lung cancer patients. "And it's changing how we treat patients in the clinic."
Nanosensing technology
Researchers are working on technology for use outside the bodyto identify and characterize tumor cells present at minuscule levels in all manner of bodily fluids—tracking the course of a known disease or even pinpointing its inception long before symptoms arise.
Wakelee has worked with center co-director Wang to design a kind of "magnetic sifter" that quickly sorts cancer cells from normal blood, based on magnetic nanotags engineered to coat the cancer cells' surface. A key component of the technique is the ability to swiftly release the bound, living cells for further study. En anden tilgang, also launched in Wang's lab, involves a magneto-nanosensor—a silicon-based chip smaller than a dime that can detect and quantify magnetic nanotags on cancer cells or cancer-associated DNA or protein molecules based on changes in the chip's external magnetic field.
This approach is being tested in clinical trials by MagArray, a company based in Milpitas, Californien, for its ability to detect multiple lung and prostate cancer biomarkers in patients' blood. Like other nanotechnology, it is exquisitely sensitive.
'Toward a simple blood draw'
These techniques may allow researchers to not just count the circulating tumor cells in a patient, but also to sequence cells' genomes or assess the levels of expression of cancer-associated proteins on their surfaces. Wakelee is also working with colleagues to develop ways to capture and sequence tumor DNA that circulates freely in the blood of cancer patients.
"We're looking for specific gene mutations that could change therapy, " she said. "In this way, we're moving away from invasive biopsies for our patients and toward a simple blood draw to learn more about an individual's specific cancer."
Gambhir is working to design gold and silica nanoparticles for use inside the body to detect colon cancer. Partiklerne, which would be swallowed as pills, coat pockets of tumor cells that would normally be invisible during a colonoscopy, and can be visualized with a special endoscope designed by the team. The technique is under review by the FDA.
"Cancer is a very difficult disease to treat, and it's also difficult to diagnose early, " said Piotr Grodzinski, PhD, who directs the NCI's nanotechnology for cancer programs. "The alliance was created to bring together engineers and materials scientists, for eksempel, with biologists and oncologists to understand, først, how nanoparticles interact with biological systems and, sekund, how they interact with cancer cells and what they can do to the tumor."
"Stanford, in the heart of Silicon Valley, is a unique place for this kind of technology to develop, " said Gambhir. "The collaborative atmosphere brings together people to solve specific problems in cancer diagnosis and detection."
The crew on the Proteus managed to band together to save the defector—in the nick of time, of course—escaping through a tear duct after destroying the blood clot in his brain just before ballooning back to normal size. Nanomedicine for future patients will likely be less fraught with urgency, but the outcome will be more important. Trods alt, the patient could be you.
Sidste artikelMille-feuille-filter fjerner vira fra vand
Næste artikelKemikere tilføjer farve til kemiske reaktioner
 Varme artikler
Varme artikler
-
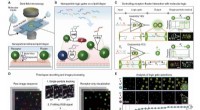 Nano-bio-computing lipid nanotabletEnkelt-nanopartikel logikberegning på LNTer. (A) Skema af LNT-platformen. To typer af DNA-modificerede nanopartikler, immobil receptor (R) og mobil flyder (F), er bundet til en SLB og overvåget af DFM
Nano-bio-computing lipid nanotabletEnkelt-nanopartikel logikberegning på LNTer. (A) Skema af LNT-platformen. To typer af DNA-modificerede nanopartikler, immobil receptor (R) og mobil flyder (F), er bundet til en SLB og overvåget af DFM -
 Forskeren undersøger kapselelasticitetKredit:Carnegie Mellon University Mechanical Engineering Carnegie Mellon Universitets Maskinteknik og Kemiteknik Professor Shelley Anna modtog for nylig et National Science Foundation -tilskud til
Forskeren undersøger kapselelasticitetKredit:Carnegie Mellon University Mechanical Engineering Carnegie Mellon Universitets Maskinteknik og Kemiteknik Professor Shelley Anna modtog for nylig et National Science Foundation -tilskud til -
 Uventede fund viser, at nanopartikler bevarer deres indre krystalstruktur, mens de bøjer som dråbe…Kredit:Yan Liang Et overraskende fænomen er blevet fundet i metal nanopartikler:De vises, udefra, at være flydende dråber, vaklende og let skiftende form, mens deres interiør bevarer en perfekt st
Uventede fund viser, at nanopartikler bevarer deres indre krystalstruktur, mens de bøjer som dråbe…Kredit:Yan Liang Et overraskende fænomen er blevet fundet i metal nanopartikler:De vises, udefra, at være flydende dråber, vaklende og let skiftende form, mens deres interiør bevarer en perfekt st -
 Fugtighed i åndedrættet gør bomuldsmasker mere effektive til at bremse spredningen af COVID-19Scanningselektronmikroskopbilleder af bomuldsflanel (venstre) og polyester (højre). Bomuldsfibre absorberer fugt fra åndedrættet, hvilket øger filtreringen. Hvert segment af billedskalaen er 50 mikrom
Fugtighed i åndedrættet gør bomuldsmasker mere effektive til at bremse spredningen af COVID-19Scanningselektronmikroskopbilleder af bomuldsflanel (venstre) og polyester (højre). Bomuldsfibre absorberer fugt fra åndedrættet, hvilket øger filtreringen. Hvert segment af billedskalaen er 50 mikrom
- Konspirationsteorier om oprindelsen af COVID-19 opvejer videnskabens indflydelse, siger forskere
- Ny global database vil hjælpe forskere med at spore søers rolle i Jordens økologi
- Solenergi bliver til biobrændsel uden solceller
- Forskellige neutronenergier øger asteroideafbøjningen
- NASA øjne tyfon Haishens 10 mile-brede øje
- WhatsApp -fejl lader spioner tage kontrol med opkald alene (opdatering)


