Selvsamlede nanostrukturer ramte deres mål
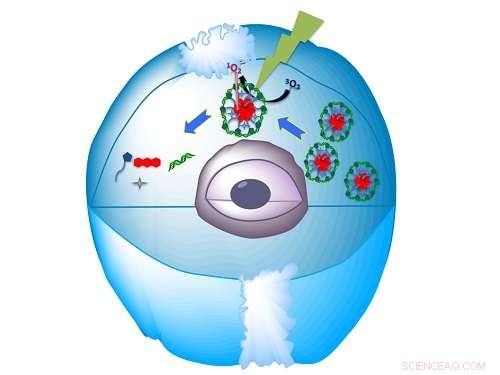
Det selvsamlede biokompatible nanomateriale leverer miRNA'et ind i cellen og frigiver det derefter, når det rammes af lys. Kredit:KAUST
Et lillebitte terapeutisk leveringssystem, der kan kontrollere kroppens evne til at fremstille proteiner, er blevet udviklet af Saudi-Arabiens King Abdullah University of Science and Technology (KAUST) forskere.
Gener indeholder instruktionerne til fremstilling af de proteiner, der udgør vores krop. Genetisk information omsættes til de proteiner, der er nødvendige for at bygge levende celler gennem en transkriptionsproces, hvor DNA's genetiske kode kopieres til et stort molekyle kendt som messenger RNA (mRNA).
Denne transkriptionsproces kan ændres ved at indføre korte dobbeltstrenge af RNA, kaldet lille interfererende RNA (siRNA), som binder til mRNA'et og hæmmer ekspressionen af bestemte gener. Det er vanskeligt at udnytte denne RNA-interferens til terapeutiske anvendelser og kræver et materiale, der kan beskytte siRNA'et, når det bevæger sig gennem blodbanen, hjælper den med at trænge ind i cellens ydre membran og levere den til dens målplacering.
"Levering af RNA er meget vanskelig, da det let kan fordøjes af celler. Bedre vehikler er nødvendige, så mere RNA kan leveres for at redigere gener, " siger Niveen Khashab fra KAUST Smart Hybrid Materials Laboratory.
Khashab og hendes kolleger har nu demonstreret biokompatible nanostrukturer til levering af siRNA og effektiv lyddæmpning af gener1. De kombinerede makromolekylet histidin-capped-9, 10-dialkoxy-anthracen (HDA) og siRNA i vand. De observerede selvsamlingen af sfæriske nanopartikler, når vandet var let surt, men ikke når den var pH-neutral.
Khashab forklarer, at disse nanosfærer er skabt af den elektrostatiske interaktion mellem det positivt ladede HDA og negativt ladede RNA, og så vikler de to lange arme af HDA supramolekylært sig omkring siRNA'et for at beskytte det.
"Vores organiske linker er i stand til at interagere med genetiske materialer ved hjælp af hydrogenbindinger og danne en leveringsbærer, " forklarer Khashab. "Tilgangen er skalerbar og skaber reproducerbare mængder af indkapslet RNA; det er også biokompatibelt og sikkert."
Nanopartiklerne kunne også aktiveres med synligt lys. Når det bestråles med grøn stråling, mens det er i nærværelse af en sur fluorescerende forbindelse, kendt som eosin, kuglen skiller sig ad og frigiver siRNA.
Holdet viste effektiviteten af nanopartikler til lægemiddellevering på B-celle lymfom 2, et mRNA-molekyle, der skaber proteiner til regulering af celledød. De viste, at deres nanostrukturer forbedrer gendæmpningseffektiviteten og førte til genet knockdown på mere end 90 procent efter eksponering for synligt lys.
"Det næste trin er at tilpasse designet til at levere andre lastmolekyler såsom protein og forbedre lysreaktionen på højere bølgelængder i det nære infrarøde, " siger Khashab.
 Varme artikler
Varme artikler
-
 Forskere identificerer den fysiske mekanisme, der kan dræbe bakterier med guld nanopartiklerI nærværelse af nanopartikler, bakteriens cellevæg ender med at brække tilsyneladende ved at strække sig, som en ballon, der pustes op fra forskellige punkter, indtil den eksploderede. Kredit:Universi
Forskere identificerer den fysiske mekanisme, der kan dræbe bakterier med guld nanopartiklerI nærværelse af nanopartikler, bakteriens cellevæg ender med at brække tilsyneladende ved at strække sig, som en ballon, der pustes op fra forskellige punkter, indtil den eksploderede. Kredit:Universi -
 Hurtigere, mere præcis kræftdetektion ved hjælp af nanopartiklerDenne illustration viser, hvordan humane brystkræftceller i en musemodel blev jagt med nye sjældne jordarters nanoskala-prober injiceret intravenøst. Når motivet er belyst, proberne lyser i et infrarø
Hurtigere, mere præcis kræftdetektion ved hjælp af nanopartiklerDenne illustration viser, hvordan humane brystkræftceller i en musemodel blev jagt med nye sjældne jordarters nanoskala-prober injiceret intravenøst. Når motivet er belyst, proberne lyser i et infrarø -
 Fremskridt inden for intens pulserende lyssintring åbner døren til forbedret elektronikproduktionUsintret, venstre, og sintrede nanopartikler. Kredit:Oregon State University Hurtigere produktion af avancerede, fleksibel elektronik er blandt de potentielle fordele ved en opdagelse af forskere
Fremskridt inden for intens pulserende lyssintring åbner døren til forbedret elektronikproduktionUsintret, venstre, og sintrede nanopartikler. Kredit:Oregon State University Hurtigere produktion af avancerede, fleksibel elektronik er blandt de potentielle fordele ved en opdagelse af forskere -
 Forskere skaber nye mikropartikler, der selv samler sig som atomer til molekylerForskere har skabt nye slags partikler, 1/100 af diameteren af et menneskehår, som spontant samler sig selv i strukturer, der ligner molekyler lavet af atomer. Kredit:Illustration udlånt af Yufeng W
Forskere skaber nye mikropartikler, der selv samler sig som atomer til molekylerForskere har skabt nye slags partikler, 1/100 af diameteren af et menneskehår, som spontant samler sig selv i strukturer, der ligner molekyler lavet af atomer. Kredit:Illustration udlånt af Yufeng W
- Forskere demonstrerer højeffektive kvanteprikkersolceller
- Hvordan COVID-19 polariserede australsk politik:#ISstandWithDan versus #DictatorDan
- At starte i mindre samfund kan være bedre for flygtninge på kort sigt
- Håndtryk eller kontrakter?
- Magnetisk flux: Hvad er det, ligning, enheder, densitet
- Var disse eksperimentresultater virkelig så forudsigelige? Disse forskere sigter efter at finde ud …


