Overvinde forhindringer i CRISPR-genredigering for at forbedre behandlingen
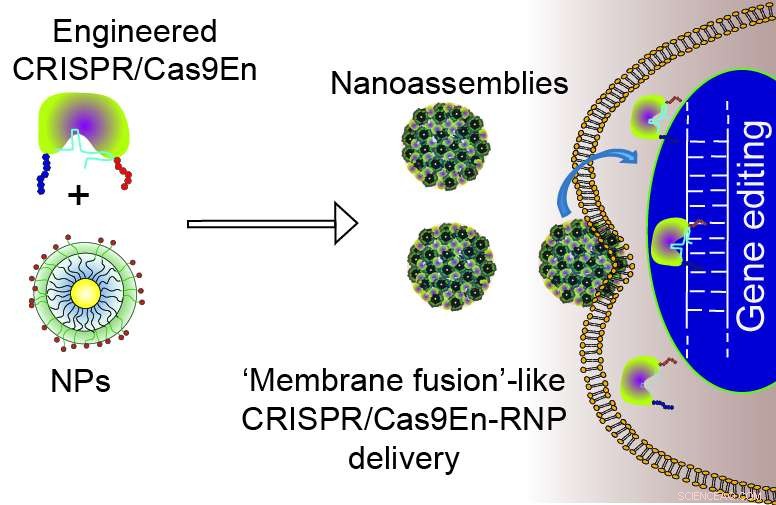
En tegneserie viser genredigering gennem manipuleret CRISPR/Cas9En-levering i Rotello-laboratoriet ved UMass Amherst. Forskerne har overvundet en hindring i teknologien ved at designe et leveringssystem, der bruger nanopartikler til at assistere CRISPR/Cas9 på tværs af cellemembranen og ind i kernen, mens de undgår at blive fanget af cellulært maskineri. Kredit:UMass Amherst
Flere og flere forskere bruger det kraftfulde nye genredigeringsværktøj kendt som CRISPR/Cas9, en teknologi isoleret fra bakterier, der lover ny behandling af sådanne genetiske sygdomme som cystisk fibrose, muskeldystrofi og hæmofili. Men for at fungere godt, det nye genklipningsværktøj skal leveres sikkert hen over cellemembranen og ind i dens kerne, en vanskelig proces, der kan udløse cellens forsvar og "fange" CRISPR/Cas9, reducerer dets behandlingspotentiale betydeligt.
Nu, forskere i nanokemi-ekspert Vincent Rotellos laboratorium ved University of Massachusetts Amherst har designet et leveringssystem, der bruger nanopartikler til at assistere CRISPR/Cas9 på tværs af membranen og ind i cellekernen, mens man undgår at blive fanget af cellemaskineri. Detaljerne findes i et nyligt nummer af tidsskriftet ACS Nano .
Laboratoriets eksperimentleder, Rubul Mout, siger, "CRISPR har to komponenter:et sakse-lignende protein kaldet Cas9, og et RNA-molekyle kaldet sgRNA, der leder Cas9 til dets målgen. Når Cas9-sgRNA-parret kommer til destinationsgenet i kernen, den kan udspørge sine genetiske fejl og rette dem ved hjælp af værtscellens reparationsmaskineri."
Han påpeger, at siden CRISPRs potentiale først blev opdaget i 2012, genredigering eller genomteknologi er hurtigt blevet et intenst forskningsemne inden for biologi og medicin. Målet er at behandle ellers uhelbredelige genetiske sygdomme ved at manipulere syge gener. "Imidlertid, for at opnå dette, biotek- og medicinalvirksomheder søger konstant efter mere effektive CRISPR-leveringsmetoder, " tilføjer han.
Den nye leveringsmetode Rotello, Mout og kolleger designet involverer konstruktion af Cas9-proteinet, ved navn Cas9En, og bærende nanopartikler. Rotello siger, "Ved at finjustere interaktionerne mellem konstrueret Cas9En-protein og nanopartikler, vi var i stand til at konstruere disse leveringsvektorer. Vektorerne, der bærer Cas9-proteinet og sgRNA, kommer i kontakt med cellemembranen, sikring, og frigive Cas9:sgRNA direkte ind i cellecytoplasmaet."
"Cas9-protein har også en nuklear vejledende sekvens, der fører komplekset ind i destinationskernen. Nøglen er at justere Cas9-proteinet, " tilføjer han. "Vi har leveret dette Cas9-protein og sgRNA-par ind i cellekernen uden at få det fanget på vej. Vi har set leveringsprocessen live i realtid ved hjælp af sofistikeret mikroskopi."
Mout og kolleger siger, at de nu kan levere Cas9-protein- og sgRNA-parret til omkring 90 procent af celler dyrket i en kulturskål med en redigeringseffektivitet på omkring 30 procent. "90 procent cytosolisk/nuklear levering er en enorm forbedring sammenlignet med andre metoder, " påpeger Mout.
Forskerne mener, at Cas9En også kan tjene som en platform for levering af en række andre materialer såsom polymerer, lipid nanopartikler eller selvsamlende peptider. Rotello siger, "Nu hvor vi har opnået effektiv genredigering i dyrkede celler, vi sigter mod at redigere gener i prækliniske dyremodeller. Vi er også interesserede i genredigering til adoptivterapier, hvor en syg celle er isoleret fra en patient, korrigeret af CRISPR i laboratoriet, og leveret tilbage til patienten."
Udover genredigering, den nye leveringsmetode kan have andre anvendelser. For eksempel, et andet vigtigt emne inden for biologi og medicin er sporing af DNA og RNA inde i celler. For nylig, CRISPR er blevet brugt til at hjælpe i denne forskning. Moumita Ray, en anden forsker i Rotello-laboratoriet, siger, "Vores metode tillader den præcise overvågning af Cas9-proteinbevægelse inde i en celle, åbner nye muligheder inden for genomforskning."
 Varme artikler
Varme artikler
-
 I solceller, justering af de mindste dele giver et stort spring i effektivitetElektrisk ingeniør Vladimir Mitin og hans kolleger har øget solcellernes elektriske effekt betydeligt ved at indlejre ladede kvanteprikker i dem. (PhysOrg.com) -- Ved at justere de mindste dele, e
I solceller, justering af de mindste dele giver et stort spring i effektivitetElektrisk ingeniør Vladimir Mitin og hans kolleger har øget solcellernes elektriske effekt betydeligt ved at indlejre ladede kvanteprikker i dem. (PhysOrg.com) -- Ved at justere de mindste dele, e -
 Nanopartikelmedicin kan gøre det nemmere for medicin at nå deres målNanoskala, tværbundne polymerstilladser kan hjælpe med at levere en overraskende høj mængde lægemidler med dårlig vandopløselighed til vandige mål. Kredit:Elsevier De enorme doser af lægemidler, d
Nanopartikelmedicin kan gøre det nemmere for medicin at nå deres målNanoskala, tværbundne polymerstilladser kan hjælpe med at levere en overraskende høj mængde lægemidler med dårlig vandopløselighed til vandige mål. Kredit:Elsevier De enorme doser af lægemidler, d -
 Forskere konstruerer et stabilt endimensionalt metallisk materialeKunstnerisk fremstilling af en af de indkapslede tellur -nanotrådtyper, som forskere forudsagde. Kredit:Paulo Medeiros Forskere har udviklet verdens tyndeste metalliske nanotråd, som kunne bruge
Forskere konstruerer et stabilt endimensionalt metallisk materialeKunstnerisk fremstilling af en af de indkapslede tellur -nanotrådtyper, som forskere forudsagde. Kredit:Paulo Medeiros Forskere har udviklet verdens tyndeste metalliske nanotråd, som kunne bruge -
 Graphene nanoflakes:Et nyt værktøj til præcisionsmedicinKredit:Swiss National Science Foundation Kemikere finansieret af SNSF har skabt en ny forbindelse til fleksibel lægemiddellevering, der specifikt er rettet mod prostatacancerceller. Inkorporerer f
Graphene nanoflakes:Et nyt værktøj til præcisionsmedicinKredit:Swiss National Science Foundation Kemikere finansieret af SNSF har skabt en ny forbindelse til fleksibel lægemiddellevering, der specifikt er rettet mod prostatacancerceller. Inkorporerer f
- Splashdown:Supersonisk kold metalbinding i 3D
- Intel præsenterer en 10-core 5,3 GHz processor
- Hvorfor Virgin Orbits nye præsident er ikke bekymret for en boble på det lille satellitmarked
- Astronomer opdager solcreme sne, der falder på varm exoplanet
- Hvad spiser Havkammuslinger Eat & Where lever de?
- Bullfinker holder sammen i årevis


