Ny tilgang til indfangning af tumor-afledte exosomer fra en prostatacancer cellelinje
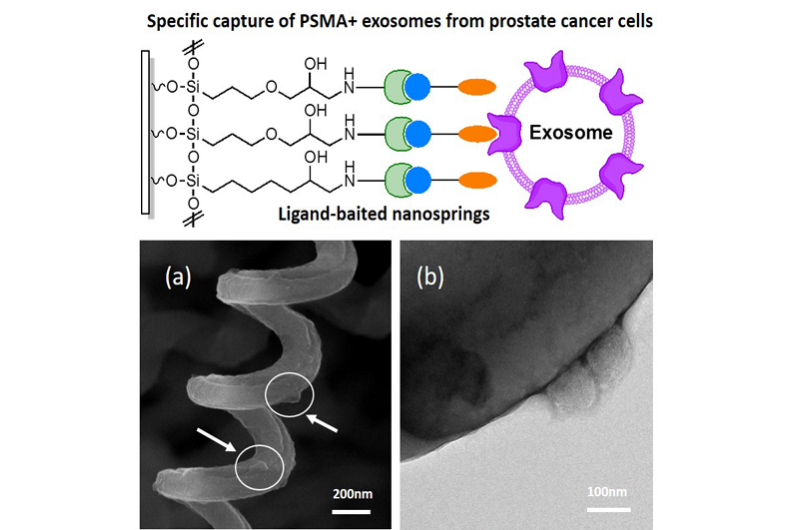
Figur a viser fangede exosomer på ligand-agnede nanospringe, exosomerne er angivet med pilene. Figur b viser et TEM -billede af fangede exosomer efter negativ farvning med phosphotungstinsyre (PTA) PH =7,1. Kredit:Springer Science+Business Media New York 2017
I et nyt papir i Springer's Journal of Materials Science , forskere ved Washington State University rapporterer om en ny tilgang til effektiv fangst af tumor-afledte exosomer fra en prostatacancer cellelinje. Exosomes er små udskillede vesikler, der spiller en central rolle i intercellulær kommunikation og kræftprogression.
Udvikling af effektiv selektiv indfangningsteknologi med høj gennemstrømning til exosomer, der bærer den prostata-specifikke membranantigen (PSMA) biomarkør, er afgørende for tidlig diagnostisk og prognostisk evaluering af prostatakræft og behandlingsplanlægning. Det vides, at prostata-tumorenzym-biomarkør PSMA er stærkt beriget i exosomer udskilt af PSMA+ prostatacancerceller. En ny biofunktionaliseret silica-nanostruktur blev designet til selektivitet at fange tumor-afledte exosomer gennem interaktionen mellem en kendt PSMA-ligand og PSMA på exosomerne.
Dette arbejde muliggør en ikke-invasiv tilgang til diagnose og prognose for prostatakræft. Det overvinder mange af begrænsningerne ved alternative tilgange, der ofte er ineffektive til at isolere tumorafledte exosomer fra dem, der stammer fra normalt væv på grund af de lave genopretningsudbytter og den tid, der kræves til processen.
Konceptet blev demonstreret ved hjælp af en enkelt kræftform (dvs. prostatakræft), men baseret på data præsenteret i denne undersøgelse, forfatterne forventer, at et bredt panel af biomarkørligander kan agnes på silica-nanostrukturer for selektivt at fange biomarkør-positive exosomer fra en række celletyper. Yderligere fordele ved den fremgangsmåde, der anvendes i denne undersøgelse, er evnen til at isolere en specifik subpopulation af exosomer, der er afhængige af ekspressionen af en specifik overflademarkør samt forbedret exosome -genopretningshastighed. I fremtiden, forfatterne forestiller sig en mikrofluidisk strømningsenhed, der giver mulighed for øget exosome indfangningseffektivitet og kliniske applikationer.
 Varme artikler
Varme artikler
-
 Undersøgelse viser, at grafen er i stand til at modstå en fartkugleRice University-forskere affyrede mikrokugler med supersoniske hastigheder i eksperimenter, der viser, at grafen er 10 gange bedre end stål til at absorbere energien fra et gennemtrængende projektil.
Undersøgelse viser, at grafen er i stand til at modstå en fartkugleRice University-forskere affyrede mikrokugler med supersoniske hastigheder i eksperimenter, der viser, at grafen er 10 gange bedre end stål til at absorbere energien fra et gennemtrængende projektil. -
 Selvlysende træ kan lyse op i fremtidens hjemNår de udsættes for UV-lys på ydersiden, et selvlysende træpanel (højre) lyser et indendørs rum op (set gennem vinduer; røde pile), hvorimod et ikke-luminescerende panel (venstre) ikke gør. Kredit:Til
Selvlysende træ kan lyse op i fremtidens hjemNår de udsættes for UV-lys på ydersiden, et selvlysende træpanel (højre) lyser et indendørs rum op (set gennem vinduer; røde pile), hvorimod et ikke-luminescerende panel (venstre) ikke gør. Kredit:Til -
 Silicastrukturer i naturlige sivblade kan udnyttes som elektrodemateriale i lithium-ion-batterierDe distinkte strukturelle og vandafvisende egenskaber ved almindelige siv er blevet brugt af mennesker i evigheder, for eksempel som byggematerialer og til stråtage. Hvordan de mikro- og nanostrukture
Silicastrukturer i naturlige sivblade kan udnyttes som elektrodemateriale i lithium-ion-batterierDe distinkte strukturelle og vandafvisende egenskaber ved almindelige siv er blevet brugt af mennesker i evigheder, for eksempel som byggematerialer og til stråtage. Hvordan de mikro- og nanostrukture -
 Fremstilling af nanostrukturer med silke kunne gøre rene rum grønne rumVandig silkefibroinopløsning af optisk kvalitet, opnået fra kokonerne af Bombyx mori larven, blev anbragt på et substrat og spin-coated for at danne en silkefilm. Både positive og negative resists ble
Fremstilling af nanostrukturer med silke kunne gøre rene rum grønne rumVandig silkefibroinopløsning af optisk kvalitet, opnået fra kokonerne af Bombyx mori larven, blev anbragt på et substrat og spin-coated for at danne en silkefilm. Både positive og negative resists ble
- Spænder sprog til det yderste
- At fremme arven fra jorden giver lokale økonomiske fordele
- Hvordan påvirker luftbevægelsen vejret?
- Hvordan du oplader din mobiltelefon kan kompromittere dens batterilevetid
- Typer af mekanisk Weathering
- Lake Huron synkehul overraskelse:Stigningen af ilt på den tidlige jord forbundet med ændret plan…


