Sammenligning viser værdien af DNA-stregkodning ved udvælgelse af nanopartikler
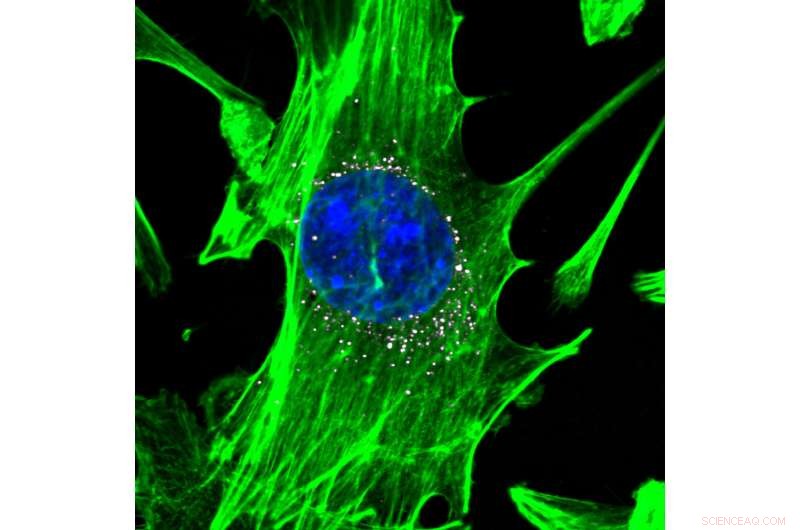
celler, farvet i grøn med blå kerner, er målrettet af nanopartikler, der bærer DNA-stregkoder (hvide). Nanopartiklerne leverer effektivt deres DNA-nyttelast ind i cellerne. Kredit:Daryll A. Vanover, Kalina Paunovska, og Cory Sago hos Georgia Tech
Den første direkte sammenligning af in vitro- og in vivo-screeningsteknikker til identifikation af nanopartikler, der kan bruges til at transportere terapeutiske molekyler ind i celler, viser, at test i laboratorieretter ikke er meget hjælp til at forudsige, hvilke nanopartikler der med succes kommer ind i cellerne i levende dyr.
Den nye undersøgelse viste fordelene ved en in vivo DNA-stregkodningsteknik, som vedhæfter små stykker DNA til forskellige lipid-baserede nanopartikler, som derefter injiceres i levende dyr; mere end hundrede nanopartikler kan testes i et enkelt dyr. DNA-sekventeringsteknikker bruges derefter til at identificere, hvilke nanopartikler der kommer ind i cellerne i specifikke organer, at gøre partiklerne til kandidater til at transportere genterapier til behandling af sådanne dræbere som hjertesygdomme, kræft og Parkinsons sygdom.
Den traditionelle teknik til at identificere lovende nanopartikler undersøger, hvordan partiklerne kommer ind i levende celler, der opbevares i laboratorieretter. For at sammenligne de nye og gamle screeningsteknikker, forskerne tilføjede stregkodede nanopartikler til levende celler i laboratorieretter, og injiceret identiske stregkodede nanopartikler i levende dyremodeller. De fandt næsten ingen sammenhæng mellem de nanopartikler, der blev identificeret som lovende i laboratorietestene, og dem, der faktisk klarede sig godt i musene.
"DNA -stregkodning har potentiale til at fremme videnskaben om at vælge nanopartikler til levering af genterapier, " sagde James Dahlman, en assisterende professor i Wallace H. Coulter Department of Biomedical Engineering ved Georgia Tech og Emory University og undersøgelsens hovedefterforsker. "Ved at bruge denne teknik, virksomheder og akademiske laboratorier kunne udvælge lovende nanopartikler meget mere effektivt. Det kunne accelerere den hastighed, hvormed nanopartikel-baserede terapier bevæger sig ind i klinikken, samtidig med at mængden af krævede dyreforsøg reduceres."
Forskningen, som er støttet af National Institutes of Health, Kræftforskningsinstituttet, Cystic Fibrosis Foundation og Parkinsons Disease Foundation, blev rapporteret 28. februar i bladet Nano bogstaver . Forskningen blev udført af forskere fra Georgia Institute of Technology og Emory University.

Dette nærbillede viser en mikrofluidisk chip, der bruges til at fremstille nanopartikler, der kunne bruges til at levere terapeutiske gener til specifikke organer i kroppen. Der er tilføjet farvede væsker for at fremhæve kanalerne. Kredit:Rob Felt, Georgia Tech
Genetiske terapier, såsom dem lavet af DNA eller RNA, står over for udfordringer på grund af vanskeligheden ved at levere nukleinsyren til de rigtige celler. I de sidste to årtier, forskere har udviklet nanopartikler lavet af en bred vifte af materialer og tilføjet forbindelser såsom kolesterol for at hjælpe med at transportere disse terapeutiske midler ind i cellerne. Men udviklingen af nanopartikelbærere er blevet bremset af udfordringerne med at teste dem, først i cellekultur til at identificere lovende nanopartikler, og senere hos dyr. Med millioner af mulige kombinationer, at identificere de optimale nanopartikler til at målrette mod hvert organ har været overvældende.
Ved at bruge DNA-strenge, der kun er 58 nukleotider lange til entydigt at identificere hver partikel, tillader forskere at springe cellekulturscreeningen helt over - og teste hundrede eller flere forskellige typer nanopartikler samtidigt i blot en håndfuld dyr.
"Hvis du ville teste 200 nanopartikler på traditionel vis, du skal bruge 600 mus - tre for hver type nanopartikel, " sagde Dahlman. "Ved brug af DNA-stregkodningsteknikken, som vi kalder Joint Rapid DNA Analysis of Nanopartikler (JORDAN), vi er i stand til at udføre testen på kun tre dyr."
Undersøgelsen undersøgte nanopartiklers indtrængen i endotelceller og makrofager til in vitro-undersøgelsen, og den samme type celler fra lungen, hjerte og knoglemarv til in vivo -komponenten. De to celletyper er vigtige for en bred vifte af organsystemer i kroppen og spiller en aktiv rolle i sygdomme, der kunne være mål for nukleinsyreterapier. Undersøgelsen sammenlignede, hvordan de samme 281 lipid-nanopartikler leverede stregkoderne i laboratorieretter og levende dyr.
"Der var ingen forudsigelig evne mellem laboratoriefadstestene og dyreforsøgene, " sagde Dahlman. "Hvis in vitro-testene havde været gode forudsigere, så ville partikler, der klarede sig godt i fadet, også have klaret sig godt hos dyrene, og partikler, der klarede sig dårligt i fadet, ville også have klaret sig dårligt i dyrene. Det så vi slet ikke«.

James Dahlman, en adjunkt i Wallace H. Coulter -afdelingen for biomedicinsk teknik ved Georgia Tech og Emory University, rummer en mikrofluidisk chip, der bruges til at fremstille nanopartikler, der kunne bruges til at levere terapeutiske gener. Kredit:Rob Felt, Georgia Tech
Forskerholdet, ledet af co-first forfattere Kalina Paunovska og Cory D. Sago, undersøgte også, hvordan levering af nanopartikler ændrer sig med mikromiljøet af specifikke vævstyper. For det, de kvantificerede, hvordan 85 nanopartikler leverede DNA-stregkoder til otte cellepopulationer i milten, og fandt ud af, at celletyper afledt af myeloide progenitorer havde en tendens til at blive målrettet af lignende nanopartikler.
Forskere er ikke kun interesserede i, hvilke nanopartikler, der leverer terapien mest effektivt, men også som kan levere dem selektivt til specifikke organer. Terapeutik rettet mod tumorer, for eksempel, bør kun leveres til tumoren og ikke til omgivende væv. Terapeutiske midler til hjertesygdomme bør ligeledes selektivt akkumulere i hjertet.
De enkeltstrengede DNA-stregkodesekvenser, der anvendes i teknikken, er omtrent samme størrelse som antisense-oligonukleotider, microRNA og siRNA udvikles til mulige terapeutiske anvendelser. Andre genbaserede terapier er større, og yderligere forskning ville være nødvendig for at afgøre, om teknikken kunne bruges sammen med dem.
Når de lovende nanopartikler er identificeret med screeningen, de ville blive udsat for yderligere test for at verificere deres evne til at levere terapeutika. For at undgå muligheden for, at nanopartikler smelter sammen, kun strukturer, der er stabile i vandige miljøer, kan testes med denne teknik. Kun ikke-toksiske nanopartikler kan screenes, og forskere skal kontrollere for potentiel inflammation genereret af det indsatte DNA.
"Nukleinsyrebehandlinger giver et stort løfte om behandling af en række alvorlige sygdomme, " sagde Dahlman. "Vi håber, at denne teknik vil blive brugt bredt i marken, og at det i sidste ende vil bringe mere klarhed over, hvordan disse lægemidler påvirker cellerne - og hvordan vi kan få dem til de rigtige steder i kroppen. "
 Varme artikler
Varme artikler
-
 Injicerbart nano-netværk styrer blodsukkeret hos diabetikere i flere dage ad gangenNano-netværket frigiver insulin som reaktion på ændringer i blodsukkeret. Kredit:Zhen Gu, North Carolina State University (Phys.org) — I en lovende udvikling for diabetesbehandling, forskere har u
Injicerbart nano-netværk styrer blodsukkeret hos diabetikere i flere dage ad gangenNano-netværket frigiver insulin som reaktion på ændringer i blodsukkeret. Kredit:Zhen Gu, North Carolina State University (Phys.org) — I en lovende udvikling for diabetesbehandling, forskere har u -
 Quantum dot solids:Denne generation af siliciumwafer?Forbindelse af prikkerne:Spil LEGO på atomskala for at bygge atomisk sammenhængende kvanteprikker faste stoffer. Kredit:Kevin Whitham, Cornell University Ligesom single-krystal silicium wafer for
Quantum dot solids:Denne generation af siliciumwafer?Forbindelse af prikkerne:Spil LEGO på atomskala for at bygge atomisk sammenhængende kvanteprikker faste stoffer. Kredit:Kevin Whitham, Cornell University Ligesom single-krystal silicium wafer for -
 Halvleder fungerer bedre, når den er koblet til grafenEt materiale lavet af halvledende polymer placeret oven på grafen leder elektrisk ladning ekstremt godt og kan muliggøre nye elektroniske enheder. Dette værk blev vist på forsiden af tidsskriftet A
Halvleder fungerer bedre, når den er koblet til grafenEt materiale lavet af halvledende polymer placeret oven på grafen leder elektrisk ladning ekstremt godt og kan muliggøre nye elektroniske enheder. Dette værk blev vist på forsiden af tidsskriftet A -
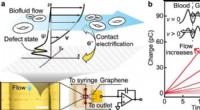 Forskere udvikler ultrafølsomme flow-mikrosensorerTransducering af blodstrømshastighed til elektrisk strøm ved hjælp af en grafen-enkeltmikroelektrodeanordning. Kredit: Naturkommunikation (2021). DOI:10.1038/s41467-021-21974-y Et team af forsker
Forskere udvikler ultrafølsomme flow-mikrosensorerTransducering af blodstrømshastighed til elektrisk strøm ved hjælp af en grafen-enkeltmikroelektrodeanordning. Kredit: Naturkommunikation (2021). DOI:10.1038/s41467-021-21974-y Et team af forsker
- Virksomhedssponsorerede CRISPR kliniske forsøg skal starte i 2018
- NASA-NOAAs Suomi NPP Satellite får to kig på orkanen Maria
- At se stivelse:Ny teknik muliggør skånsom observation af biobrændstofmaterialer
- AI-drevet dynamisk ansigtsmaske tilpasser sig træning, forureningsniveauer
- Nyt kraftproduktions- og fremdriftssystem til satellitter
- Er crowd-control våben farlige? Meget, siger ekspert


