Samtidig overvågning af overflader og proteinfordeling i celler

For at lette analyse i levende celler, teamet planlægger at udvikle et kombineret instrument i næste trin. Kredit:© RUB, Kramer
I en første proof-of-concept undersøgelse, forskere ved Ruhr-Universität Bochum (RUB) har kombineret to mikroskopimetoder, der gør både en celles overflade og fordelingen af et protein i cellen synlig, ved en opløsning i nanometerområdet. Metoden kan bruges til levende celler. Det kan for eksempel hjælpe med at analysere, hvordan kræftmetastaser dannes eller vurdere effekten af specifikke lægemidler. Forskerne fra nanoskopi-arbejdsgruppen på Rubion, den centrale enhed for ionstråler og radionuklider på RUB, rapporterede deres resultater i det anerkendte tidsskrift ACS Nano den 23. maj, 2018.
Et første skridt
Betydeligt mindre end 250 nanometer, proteinkomplekser kan ikke afbildes i detaljer ved hjælp af lysmikroskopiteknikker. For at finde en vej ind, RUB-arbejdsgruppen kombinerede stimuleret emissionsudtømningsmikroskopi (STED) med scanning-ionkonduktansmikroskopi (SICM).
"STED-mikroskopi gør os i stand til at analysere fordelingen af proteiner i høj opløsning. SICM letter højopløsnings-probing af cellemembranen. Følgelig, vi har været i stand til at forbinde fordelingen af det cellulære protein actin med nanostrukturen af cellemembranen, " forklarer Philipp Hagemann, Ph.D. forsker i arbejdsgruppen. "Vores resultater udgør et første skridt mod højopløsningsanalyse af overfladestrukturen, dvs. den biokemiske organisation af cellen og dens omgivende membran, " uddyber Dr. Patrick Happel, leder af nanoskopi arbejdsgruppen.
Forståelse af cellemembranens rolle
Cellemembranen er et fedtlag, der omslutter hver celle, dermed adskille den fra dens omgivelser. For at kommunikere med deres omgivelser, celler har en række forskellige proteiner, der er indlejret i cellemembranen og overfører eksterne stimuli ind i cellens indre. "Måden proteiner er organiseret i cellemembranen, måden deres position ændres på, og måden disse ændringer er orkestreret på er endnu ikke fuldt ud forstået, " siger Happel. Proteinerne i cellemembranen såvel som selve cellemembranen er væsentlige faktorer i denne proces, når celler ændrer deres position under sårheling, under udvikling, og også mens kræftmetastaser dannes. Forskere omtaler denne proces som migration.
Selvom cellemigration er forskellig mellem forskellige celletyper, et almindeligt aspekt er en udvidelse af cellemembranen i bevægelsesretningen. Inden i organismen, migrerende celler skal bevæge sig gennem ekstremt smalle mellemrum mellem andre celler. Dette er kun muligt, hvis cellen er betydeligt deformeret, og hvis adhæsionskomplekser dannes ved cellens forkant og løsnes ved bagkanten. Samspillet mellem disse biokemiske og biofysiske processer er endnu knap blevet forstået på det molekylære plan, da der ikke eksisterer nogen metode, der er i stand til at overvåge denne dynamiske proces i høj opløsning over en længere periode.
Todelt enhed planlagt
"Vi har registreret dataene successivt med forskellige enheder. Således, vi var i stand til at demonstrere, at vores metode gør nye analyser mulige, "forklarer Astrid Gesper, Ph.D. forsker i arbejdsgruppen.
For at lette analysen i levende celler, teamet planlægger at udvikle et kombineret instrument i næste trin. "Kombinationen af begge metoder vil gøre transportprocesserne synlige i detaljer – hvilket også spiller en afgørende rolle for målrettet anvendelse af lægemidler via nanopartikler, "slutter Patrick Happel.
 Varme artikler
Varme artikler
-
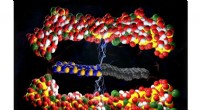
 En beregningsmæssig tilgang til at forudsige strukturen af nano-legeringskatalysatorer afsløretBeregninger viser, at platin-kerne (grå)-palladium-skal (grøn) nanopartikler er særligt stabile. Hydrogenatomer (røde), der adsorberer til partikeloverfladen, omdannes katalytisk til brintgas. Kredit:
En beregningsmæssig tilgang til at forudsige strukturen af nano-legeringskatalysatorer afsløretBeregninger viser, at platin-kerne (grå)-palladium-skal (grøn) nanopartikler er særligt stabile. Hydrogenatomer (røde), der adsorberer til partikeloverfladen, omdannes katalytisk til brintgas. Kredit: -
 Nano-infunderet keramik kunne rapportere om sit eget helbredKeramik med netværksforbundne nanoark af grafen og hvid grafen ville have den unikke evne til at ændre deres elektriske egenskaber, når de belastes, ifølge en forsker ved Rice University. Den overrask
Nano-infunderet keramik kunne rapportere om sit eget helbredKeramik med netværksforbundne nanoark af grafen og hvid grafen ville have den unikke evne til at ændre deres elektriske egenskaber, når de belastes, ifølge en forsker ved Rice University. Den overrask -
 Bimetallisk nanoantenne adskiller lysfarverNanoantennen fungerer som en router for rødt og blåt lys, på grund af, at nanopartiklerne af guld og sølv har forskellige optiske egenskaber. Kredit:Timur Shegai Forskere ved Chalmers Tekniske Uni
Bimetallisk nanoantenne adskiller lysfarverNanoantennen fungerer som en router for rødt og blåt lys, på grund af, at nanopartiklerne af guld og sølv har forskellige optiske egenskaber. Kredit:Timur Shegai Forskere ved Chalmers Tekniske Uni -
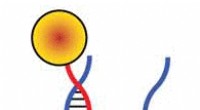 Superopløsningssystem afslører mekanikken i den lille DNA-walkerDenne animerede gif skildrer gangmekanismen bag et DNA-gangsystem, der kunne finde biomedicinske og industrielle anvendelser. Kredit:Purdue University billede/Jared Pike Forskere har introduceret
Superopløsningssystem afslører mekanikken i den lille DNA-walkerDenne animerede gif skildrer gangmekanismen bag et DNA-gangsystem, der kunne finde biomedicinske og industrielle anvendelser. Kredit:Purdue University billede/Jared Pike Forskere har introduceret
- Forskere erhverver 3-D-billeder med LED-rumbelysning og en smartphone
- Flyv med individuelt airconditionerede sæder
- Solradio -signaler kunne bruges til at overvåge smeltende iskapper
- SpaceX CRS-22 mission til rumstation opsender vandbjørne, blæksprutte, solpaneler
- Myte om geni ensom videnskabsmand er farlig
- Studerer Midtvestens jorderosion fra rummet


