Ny platform baseret på biologi og nanoteknologi fører mRNA direkte til målceller
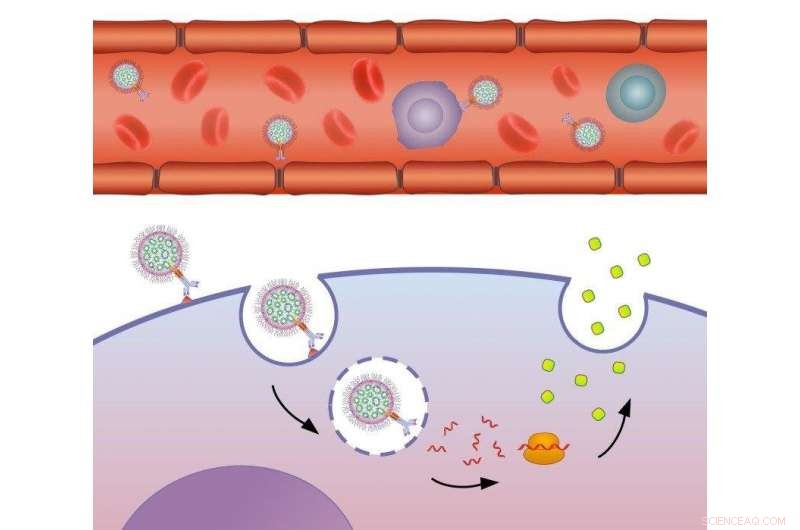
Skematisk illustration af den mekanisme, hvorved laboratoriets målrettede nanopartikler modulerer genekspression i målcellen. Kredit:Nuphar Veiga/American Friends of Tel Aviv University.
At levere en effektiv terapeutisk nyttelast til specifikke målceller med få negative virkninger anses af mange for at være den hellige gral af medicinsk forskning. En ny Tel Aviv University undersøgelse udforsker en biologisk tilgang til at dirigere nanobærere fyldt med protein "game changers" til specifikke celler. Den banebrydende metode kan vise sig nyttig til behandling af utallige maligne sygdomme, inflammatoriske sygdomme og sjældne genetiske lidelser.
Prof. Dan Peer, direktør for Laboratoriet for Precision Nanomedicin på Skolen for Molekylær Cellebiologi ved TAU's Biovidenskabelige Fakultet, ledet forskningen til det nye studie, som blev udført af TAU kandidatstuderende Nuphar Veiga og laboratoriekolleger Meir Goldsmith, Yasmin Granot, Daniel Rosenblum, Niels Dammes, Ranit Kedmi og Srinivas Ramishetti. Forskningen blev offentliggjort i Naturkommunikation .
I løbet af de sidste par år, lipidbærere, der indkapsler messenger-RNA'er (mRNA'er), har vist sig at være ekstremt nyttige til at ændre proteinekspressionerne for en lang række sygdomme. Men at dirigere denne information til specifikke celler er fortsat en stor udfordring.
"I vores nye forskning, vi brugte mRNA-ladede bærere - nanovehicles, der bærer et sæt genetiske instruktioner via en biologisk platform kaldet ASSET - til at målrette de genetiske instruktioner fra et antiinflammatorisk protein i immunceller, " siger prof. Peer. "Vi var i stand til at påvise, at selektivt antiinflammatorisk protein i målcellerne resulterede i reducerede symptomer og sygdommens sværhedsgrad i colitis.
"Denne forskning er revolutionerende. Den baner vejen for introduktionen af et mRNA, der kunne kode for ethvert protein, der mangler i celler, med direkte anvendelser af genetiske, inflammatoriske og autoimmune sygdomme - for ikke at nævne kræft, hvori visse gener overudtrykker sig selv."
ASSET (Anchored Secondary scFv Enabling Targeting) bruger en biologisk tilgang til at dirigere nanobærere ind i specifikke celler for at fremme genmanipulation.
"Dette studie åbner nye veje i cellespecifik levering af mRNA-molekyler og kan i sidste ende introducere det specifikke anti-inflammatoriske (interleukin 10) mRNA som en ny terapeutisk modalitet for inflammatoriske tarmsygdomme, " siger fru Veiga.
"Målrettet mRNA-baseret proteinproduktion har både terapeutiske og forskningsmæssige anvendelser, " afslutter hun. "Fremadrettet, vi agter at bruge målrettet mRNA-levering til undersøgelse af nye terapeutiske midler til behandling af inflammationslidelser, kræft og sjældne genetiske sygdomme."
Sidste artikelNye kvanteprikker forbedrer cellebilleddannelse
Næste artikelForskere skaber skalerbar platform for on-chip kvanteemittere
 Varme artikler
Varme artikler
-
 Et nyt papir lavet af grafen og proteinfibrillerDet endelige hybride nanokompositpapir lavet af proteinfibriller og grafen efter vakuumfiltreringstørring. Den skematiske rute, som forskerne brugte til at kombinere grafen og proteinfibriller i det n
Et nyt papir lavet af grafen og proteinfibrillerDet endelige hybride nanokompositpapir lavet af proteinfibriller og grafen efter vakuumfiltreringstørring. Den skematiske rute, som forskerne brugte til at kombinere grafen og proteinfibriller i det n -
 Dimensionering af nanopartikler ved hjælp af væskefyldte rørKredit:CC0 Public Domain Funktionaliteten af nanopartikler i et væld af applikationer, herunder lægemiddellevering og nano-optik, er ofte dikteret af deres masse og størrelse. At måle disse egen
Dimensionering af nanopartikler ved hjælp af væskefyldte rørKredit:CC0 Public Domain Funktionaliteten af nanopartikler i et væld af applikationer, herunder lægemiddellevering og nano-optik, er ofte dikteret af deres masse og størrelse. At måle disse egen -
 Forskere sporer nanopartikler fra planter til larverOpbygningen af fluorescerende kvanteprikker i bladene af Arabidopsis-planter er tydelig på dette fotografi af planterne under ultraviolet lys. Kredit:Y. Koo/Rice University I en af de mest omf
Forskere sporer nanopartikler fra planter til larverOpbygningen af fluorescerende kvanteprikker i bladene af Arabidopsis-planter er tydelig på dette fotografi af planterne under ultraviolet lys. Kredit:Y. Koo/Rice University I en af de mest omf -
 Hvordan grafen kunne afkøle smartphone, computer og andre elektronikchipsgrafen, et et-atom-tykt lag grafit, består af kulstofatomer arrangeret i et bikagegitter. Kredit:OliveTree/Shutterstock Med grafen, Rutgers-forskere har opdaget en kraftfuld måde at afkøle små chi
Hvordan grafen kunne afkøle smartphone, computer og andre elektronikchipsgrafen, et et-atom-tykt lag grafit, består af kulstofatomer arrangeret i et bikagegitter. Kredit:OliveTree/Shutterstock Med grafen, Rutgers-forskere har opdaget en kraftfuld måde at afkøle små chi
- Krybskytter truer dyrebar Madagaskar -skov og lemurer
- Kan Nordvestpassagen åbne for erhvervslivet?
- En vulkanologer tager fat på Fuego -udbrud
- Siger mod mavekræft:Ny tilgang til selektiv kemoterapi
- Droner leverer internetforbindelse
- Forskere skaber ingredienser til at producere mad ved hjælp af 3D-print


