CAR T-behandlinger kan have færre bivirkninger end andre kræftimmunterapier
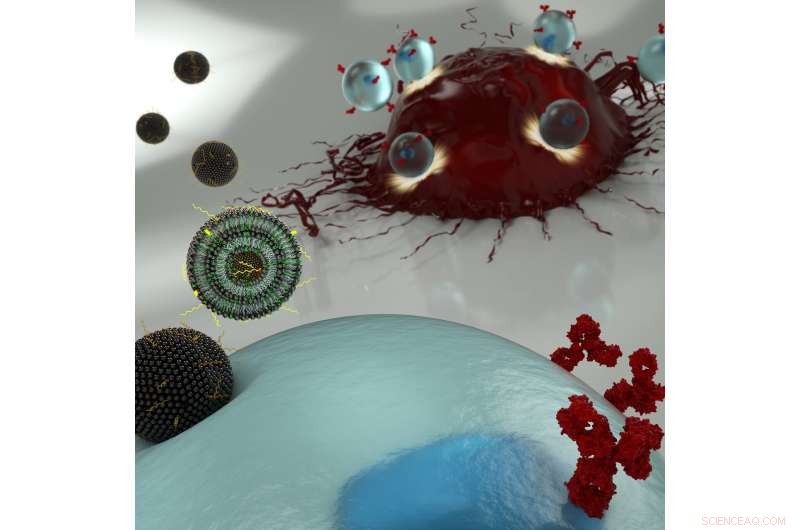
En kunstners illustration af nanopartikler, der transporterer mRNA ind i en T-celle (blå), lader sidstnævnte udtrykke overfladereceptorer, der genkender kræftceller (røde). Kredit:Ryan Allen, Second Bay Studios
Nye kræftimmunterapier involverer udvinding af en patients T-celler og gensplejsning af dem, så de kan genkende og angribe tumorer. Denne teknik er et sandt medicinsk gennembrud, med et stigende antal leukæmi- og lymfompatienter, der oplever fuldstændig remission, siden CAR T-terapi blev godkendt af FDA i 2017.
Denne form for terapi er ikke uden udfordringer, imidlertid. Konstruktion af en patients T-celler er besværligt og dyrt. Og når det lykkes, ændringerne i immunsystemet gør straks patienter meget syge i en kort periode, med symptomer, herunder feber, kvalme og neurologiske påvirkninger.
Nu, University of Pennsylvania forskere har demonstreret en ny ingeniørteknik, der, fordi det er mindre giftigt for T-cellerne, kunne muliggøre en anden mekanisme til at ændre den måde, de genkender kræft på.
Behandlingsforløb med T-celler, der bruger denne mekanisme, kan have færre bivirkninger for patienterne.
Forskernes nye ingeniørteknik går ud på at transportere messenger-RNA (mRNA) over T-cellens membran via en lipid-baseret nanopartikel, frem for at bruge et modificeret HIV-virus til at omskrive cellens DNA. At bruge den tidligere tilgang ville være at foretrække, da det kun giver en midlertidig ændring af patientens immunsystem, men den nuværende standardmetode til at få mRNA forbi cellemembranen kan være for giftig til at bruge på det begrænsede antal T-celler, der kan udvindes fra en patient.
Forskerne demonstrerede deres teknik i en undersøgelse offentliggjort i tidsskriftet Nano bogstaver . Det blev ledet af Michael Mitchell, Skirkanich Adjunkt i innovation ved Institut for Bioteknik ved Penns School of Engineering and Applied Science, og Margaret Billingsley, en kandidatstuderende i sit laboratorium.
De samarbejdede med en af pionererne inden for CAR T-terapi:Carl June, Richard W. Vague professor i immunterapi og direktør for Center for Cellular Immunotherapies i Abramson Cancer Center og direktør for Parker Institute for Cancer Immunotherapy ved Penn's Perelman School of Medicine.
CAR T-terapi involverer konstruktion af en patients egne T-celler, så de udtrykker kimære antigenreceptorer, "CAR" af "CAR T, " på deres overflader. Disse receptorer gør det muligt for T-cellerne at genkende kræftceller som fremmede angribere og fjerne dem fra kroppen. Nuværende tekniske teknikker involverer at fjerne en række af en patients T-celler, omskrive deres DNA med en virus, så de udtrykker disse CAR'er, derefter injicere dem tilbage i patienten.
"Denne virale ingeniørmetode producerer T-celler med permanent CAR-ekspression, men det fører til alvorlige bivirkninger, da CAR T -cellerne forbliver aktive i patienten, selv efter udryddelse af kræftceller, " siger Billingsley. "Ved at bruge mRNA til at generere CAR T-celler, imidlertid, skaber T -celler med forbigående CAR -ekspression. Dette kan give klinikere mulighed for at administrere CAR T -celleterapier i doser for at målrette kræftceller uden at skade så mange raske celler i processen, dermed afbøde bivirkningerne."
En sådan tilgang har endnu ikke vundet klinisk indpas, da metoder til at få mRNA ind i T-celler stadig er begrænsede. Den nuværende standard, elektroporation, som involverer perforering af cellemembranen med en elektrisk puls, er ikke en attraktiv mulighed, da den meget invasive proces har en høj risiko for at dræbe T-cellen eller påvirke dens funktionalitet. Selv når de er optimeret, elektroporation resulterer ofte i celledød i 50 procent af cellerne under cellefremstillingsprocessen.
I betragtning af omkostningerne, vanskeligheder og indsatser forbundet med at erhverve disse celler fra en CAR T-patient, en langt mindre toksisk metode til indførelse af mRNA er nødvendig, før denne teknik er et levedygtigt alternativ til DNA-redigeringsmetoden.
Mitchell, Billingsley og deres kolleger satte sig således for at finde en passende leveringsplatform til at snige mRNA forbi T -cellens membran i tilstrækkelige mængder til, at de kunne translateres til de ønskede receptorproteiner.
Imidlertid, da T -celler ikke let optager materiale fra deres miljø, at finde den rigtige nanopartikel til denne applikation var en udfordring. Yderligere, det ville være afgørende, at platformen omfatter både meget effektiv levering og lav cytotoksicitet - en sjælden kombination.
"Når man leverer terapeutisk mRNA ind i celler, du skal altid balancere styrke med giftige bivirkninger, " Mitchell siger. "Vores laboratorieingeniører udvikler ioniserbare lipid-nanopartikler, der sikkert kan krydse cellulære membraner, men frigiver terapeutisk mRNA specifikt, når det skal frigives. Det ser vi som en kæmpe fordel, som den nuværende kliniske standard, elektroporation, dræber en stor del af patientens T -celler. "
"Desuden, " han siger, "Vi forestiller os som en platformsteknologi til levering af T-celler, da vi kan lave mRNA'er til forskellige terapeutiske CAR'er, eller andre terapeutiske receptorer meget hurtigt ved blot at ændre mRNA -sekvensen, og har derfor en række terapeutiske anvendelser."
Med in vitro eksperimenter, forskerne viste, at deres nanopartikler genererede CAR T-celler, der var lige så effektive til at dræbe kræftceller som de viralt konstruerede CAR T-celler, der i øjeblikket er i klinisk brug. Næste trin vil omfatte in vivo undersøgelser af virkningerne af dette leveringssystem, undersøge virkningerne af forbigående CAR -ekspression på terapeutisk effekt og bivirkninger.
"I betragtning af den stigende værktøjskasse af RNA-terapi, nanopartikellevering af RNA har brede anvendelsesmuligheder for T-celleteknologi, herunder genetisk redigering af T-celle-DNA og modulering af proteinekspression, siger June.
 Varme artikler
Varme artikler
-
 Neurale netværk vil hjælpe med at fremstille kulstof nanorørKredit:Skoltech Tynde film lavet af kulstof nanorør lover meget for avanceret optoelektronik, energi og medicin, dog med deres fremstillingsproces underlagt tæt overvågning og strenge standardiser
Neurale netværk vil hjælpe med at fremstille kulstof nanorørKredit:Skoltech Tynde film lavet af kulstof nanorør lover meget for avanceret optoelektronik, energi og medicin, dog med deres fremstillingsproces underlagt tæt overvågning og strenge standardiser -
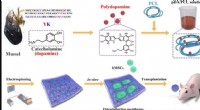 Knoglevævsteknik - nano-lim polymermembraner til robust knogleregenereringSkematisk tegning af fremstillingen af de konstruerede membraner via elektrospinning af PCL og PDA NPer. Kredit:NPG Asia Materials, doi:10.1038/s41427-019-0139-5 I en ny undersøgelse nu offentli
Knoglevævsteknik - nano-lim polymermembraner til robust knogleregenereringSkematisk tegning af fremstillingen af de konstruerede membraner via elektrospinning af PCL og PDA NPer. Kredit:NPG Asia Materials, doi:10.1038/s41427-019-0139-5 I en ny undersøgelse nu offentli -
 Kevlarbaseret kunstig brusk efterligner den magiske virkelighedDet kunstige brusk er meget fleksibelt, men alligevel modstandsdygtigt over for rivning. Kredit:Joseph Xu, Michigan Engineering Communications &Marketing Bruskens enestående væskestyrke, hvilket e
Kevlarbaseret kunstig brusk efterligner den magiske virkelighedDet kunstige brusk er meget fleksibelt, men alligevel modstandsdygtigt over for rivning. Kredit:Joseph Xu, Michigan Engineering Communications &Marketing Bruskens enestående væskestyrke, hvilket e -
 Lovende nanomaterialers oprindelse afsløretPauk Dunk, en kemiforsker ved Florida State. Forskere fra Florida State University tilbyder en ny forståelse af, hvordan et spændende nanomateriale - metallofulleren - dannes i et nyligt offentlig
Lovende nanomaterialers oprindelse afsløretPauk Dunk, en kemiforsker ved Florida State. Forskere fra Florida State University tilbyder en ny forståelse af, hvordan et spændende nanomateriale - metallofulleren - dannes i et nyligt offentlig


