Knoglevævsteknik - nano-lim polymermembraner til robust knogleregenerering
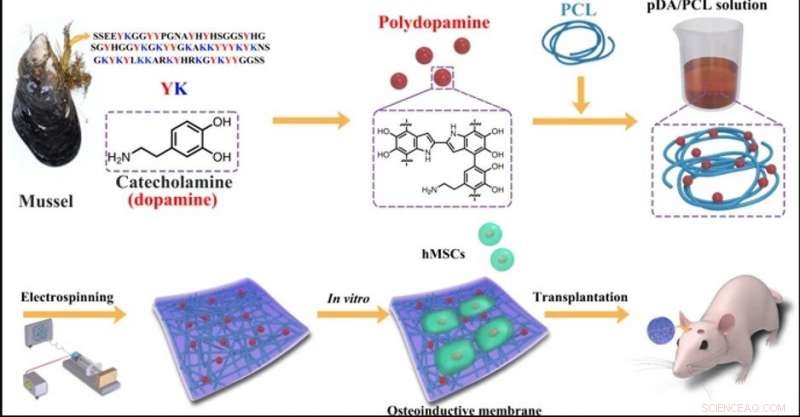
Skematisk tegning af fremstillingen af de konstruerede membraner via elektrospinning af PCL og PDA NP'er. Kredit:NPG Asia Materials, doi:10.1038/s41427-019-0139-5
I en ny undersøgelse nu offentliggjort på NPG Asia materialer , bioingeniører rapporterer udviklingen af en ny fibrøs membran med stamceller til at reparere knogledefekter i kranier på mus. For det, de inkorporerede muslingeinspireret polydopaminprotein som en lovende forbindelse til at binde biologiske stoffer til membranoverfladerne, meget som klæbende proteiner i muslinger. I arbejdet, Yi Deng og et forskerhold i de tværfaglige afdelinger for kemiteknik, Maskiningeniør, materialeteknologi, center for fremtidige materialer og regenerativ medicin i Kina og Australien, belagt de biokompatible membraner med polydopaminnanopartikler for at danne mange topologiske steder for calciumvedhæftning og knoglefejl reparation.
Holdet inkuberede de ubelagte og coatede membraner med stamceller isoleret fra knoglemarv og implanterede membranerne for at regenerere kranieknogledefekter i levende mus. Efter et 2-måneders translationelt studie, de afslørede de klæbrige membraners evne til at lede stamceller til at producere betydeligt større mængder knogle, sammenlignet med ubelagte membraner. Knoglefejl og skader kan almindeligvis forekomme på mikroskopisk niveau som medfødte defekter, på grund af ulykker eller som aldersrelateret degenerativ sygdom. De fleste knogledefekter kan ikke repareres spontant af selvhelbredende mekanismer, hvilket fører til et presserende behov for at udvikle robuste biomaterialer, der letter knoglereparation i knogleforskning og knoglevævsteknik.
Bioingeniører kan manipulere stamcelledifferentiering for at danne modne osteoblaster via guidet vævsregenerering (GTR) på overflademembraner for at optimere, storstilet knogleregenerering. Inden for materialevidenskab og avancerede funktionelle materialer, elektrospundne membraner har fået massiv opmærksomhed for sådanne guidede vævsteknologiske strategier på grund af flere biokompatible fordele, inklusive:
- Biomimik for stamcellevedhæftning
- Stort overfladeareal for at lette celleadhæsion og vækst
- Evnen til at danne 3-D fibrøse membraner og accelerere det osteogene potentiale af adskillige stamcellelinjer (fra mus, rotter og menneskearter).
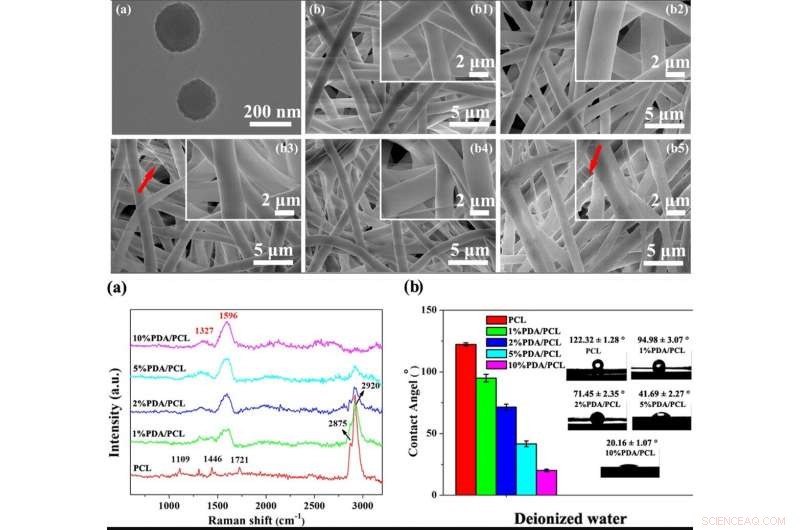
TOP:Mikromorfologier af PDA NP'er og elektrospundne PDA/PCL fibrøse membraner. et TEM-billede af PDA NP'er; b SEM-billeder af den (b1) uberørte PCL, (b2) 1 % PDA/PCL, (b3) 2 % PDA/PCL, (b4) 5 % PDA/PCL, og (b5) 10 % PDA/PCL fibrøse membraner. De røde pile i b peger på filamenterne. BUND:Kemiske bestanddele af PDA/PCL fibrøse membraner. (a) Raman-spektre og (b) kontaktvinkler med tilsvarende vanddråbebilleder af PDA/PCL-fibrøse membraner. Kredit:NPG Asia Materials, doi:10.1038/s41427-019-0139-5
Materialeforskere klassificerer syntetiske GTR-materialer i to hovedkategorier som (1) bioabsorberbare og (2) ikke-absorberbare materialer; hvor ikke-absorberbare materialer skal fjernes efter implantation via en anden operation, forårsager øgede sundhedsudgifter, mens det kompromitterer nygenereret væv. I modsætning, bionedbrydelige membraner såsom polyvinylalkohol (PVA), poly (lactid-co-glycolid) (PLGA) eller PCL foretrækkes til kliniske implantationer, selvom biologiske komplikationer alvorligt har hæmmet deres kliniske adoption.
I nærværende arbejde, derfor, Deng et al. brugte det bioinspirerede klæbende protein udskilt fra muslinger som en 'materiale-uafhængig' og let overfladebelægning, ingeniørstrategi baseret på katekolkemi. Polydopamin (PDA) kan lette osteoblastisk differentiering af stamceller på en række forskellige substrater som en nanoskala biomaterialebelægning, at støtte mesenkymal stamcellebinding og inducere omprogrammering af humane somatiske celler. Alligevel, PDA-nanolag kan let delaminere fra overflader for at fremkalde lokal celleapoptose eller inflammatoriske reaktioner som bivirkninger. Deng et al. implementeret specifikke eksperimentelle trin for at overvinde de eksisterende begrænsninger og udvikle en ny biokompatibel og bionedbrydelig membran i laboratoriet. Det nyudviklede biomateriale eller fibrøse membran vil give en gunstig niche til at styre lokale stamcellers skæbne til at danne osteoblaster til knogleregenerering.
Trin et:Engineering PDA-inkluderet PCL (PDA/PCL) med elektrospinning
Forskerne brugte katekolkemi til fremstilling og syntese af PDA/PCL-fibrøse membraner. De spredte PDA-nanopartiklerne (NP'er) ensartet i PCL via kontinuerlig sonikering og vortexing for at danne de fibrøse membraner via elektrospinning. Deng et al. brugte et scanningselektronmikroskop (SEM) og observerede overfladeegenskaber af det tilfældige, mikron-størrelse fibrøst netværk. Forholdsvis, de rene PCL elektrospundne membraner forblev glatte, hvorimod integrationen af PDA NP'er gjorde fiberoverfladerne ru. Forskerne bekræftede den nye overfladekemi ved hjælp af Raman-spektre og røntgenfotoelektronspektroskopi (XPS) analyse. Biomaterialerne var hydrofile, hvilket tillod proteinadsorption og cellevedhæftning. Forskerne udførte kontaktvinkelmålinger for at verificere overfladefugtigheden og forbedret hydrofilicitet efter PDA-modifikation sammenlignet med den rene, umodificerede PCL-membraner.
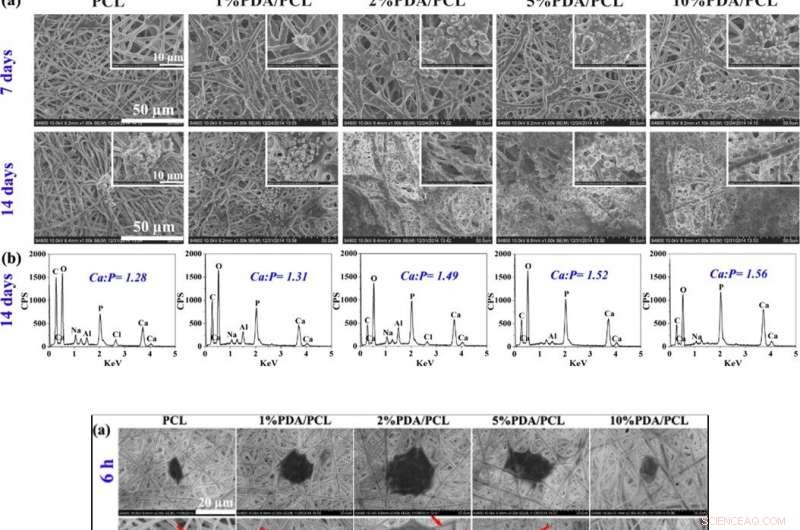
TOP:Knoglelignende knuder. (a) SEM-fotografier af PDA/PCL-fibrøse membraner erhvervet efter iblødsætning i SBF i 7 og 14 dage. (b) EDS-data og Ca/P-forhold for partikelsedimenterne på overfladen af PDA/PCL-fibrøse membraner efter 14 dage. NEDERST:Cellevedhæftning og spredning. (a) SEM og b CLSM observation af adhærerende hMSC'er på de konstruerede fibrøse membraner med forskellige PDA NP-koncentrationer ved 6 og 12 timer. De røde pile peger på pseudopodien. Indsætningerne øverst til højre i (b) viser de forstørrede billeder af en enkelt celle. (c) Cellevedhæftning og (d) proliferationskurver for hMSC'er på prøveoverfladerne opnået via CCK-8. * Repræsenterer p < 0,05 mellem grupper, ** repræsenterer p < 0,01 mellem grupper; og # repræsenterer p < 0,05 sammenlignet med andre grupper. Kredit:NPG Asia Materials, doi:10.1038/s41427-019-0139-5
Trin to:Undersøgelser af overfladekarakterisering
Da bioaktive membraner kan integreres med omgivende knoglevæv (knoglevæv), Deng et al. vurderet dannelsen af knogleapatitlag på overfladen af biomaterialer nedsænket i simuleret kropsvæske (SBF) opløsning. Efter 7 dages nedsænkning, forskerne observerede klyngede nodulære aggregater på PDA/PCL-membranerne, som steg dramatisk på dag 14. Til sammenligning kontrolprøven af uberørt umodificeret PCL tilbageholdt Ca-P-aflejringer efter syv dage, med øer af apatit på dag 14. Efterhånden som PDA-indholdet steg, derfor, mængden af aflejret apatit på overfladen steg. Deng et al. brugte materialekarakteriseringsdataene til at validere forbedret in vitro bioaktivitet af PDA/PCL-membraner sammenlignet med den rene PCL-kontrol.
Trin tre:Biofunktionaliseringsundersøgelser
Forskerne vurderede cytokompatibiliteten (cellebiokompatibilitet) af de konstruerede PDA/PCL-membraner i forhold til celleadhæsion, breder sig, og human mesenkymal stamcelle (hMSC'er) proliferation. hMSC'erne eksisterer stort set i knoglemarven for at hjælpe vævsreparation under skade. Efter 6 timers cellekultur, hMSC'erne med runde cellulære former adhærerede ikke godt på ren PCL, men udtrykte filopodia til membranoverfladevedhæftning på tre varianter af PDA/PCL-membraner. Ved at bruge celletællingseksperimenter og cellelevedygtighed CCK-8 assays, Deng et al. viste, at indholdet af PDA NP'er signifikant påvirkede antallet af levedygtige celler knyttet til overfladen, og observerede optimale overfladeegenskaber med 2 procent PDA/PCL-gruppen i arbejdet.
Forskerholdet bestemte den optimale formel til at konstruere PDA/PCL-membraner til styret knoglevævsregenerering ved at bestemme aktiviteten af alkalisk phosphatase (ALP) og calciummatrixproduktionen af hMSC'er med Alizarin Red S (ARS)-farvning. Cellevækst og osteogen differentiering var lav, når mængderne af PDA NP'er var enten høje eller lave, fordi lave koncentrationer ikke udløste cellevækst, hvorimod høje koncentrationer var toksiske i undersøgelsen.
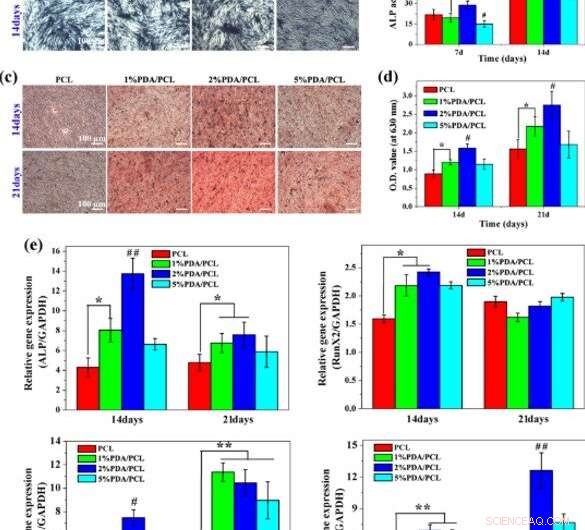
Osteogen differentiering:a, b Farvning og kvantificering af ALP-aktivitet, c, d ARS-farvning og kvantificering af calciumproduktion, og e RT-PCR analyse for osteospecifikke gener på forskellige PDA/PCL fibrøse membraner. * repræsenterer p < 0,05 mellem grupper, **repræsenterer p < 0,01 mellem grupper. # repræsenterer p < 0,05 sammenlignet med andre grupper, og ## repræsenterer p < 0,05 sammenlignet med andre grupper. Kredit:NPG Asia Materials, doi:10.1038/s41427-019-0139-5
Da undersøgelser på molekylært niveau er et stærkt værktøj inden for biomaterialer til bioteknik, Deng et al. undersøgte samspillet mellem hMSC'er og konstruerede membraner ved hjælp af molekylære værktøjer. For det, de overvågede ekspressionen af osteogenese-relaterede gener ALP, Runx2, Col1a1 og OPN i hMSC'er dyrket på membranerne. Efter 7 dage observerede de betydelige niveauer af ALP-genekspression på 2 procent PDA/PCL-prøven.
På dag 14, niveauet af Runx2-gen udtrykt på 1 og 2 procent PDA/PCL-grupper matchede signifikant den rene PCL-gruppe. Imidlertid, inden for 21 dage, forskerne observerede ikke en mærkbar forskel mellem de fire grupper. De verificerede observationerne ved hjælp af immunfluorescensfarvning og valgte 2 procent PDA/PCL-membraner til optimal induktion af hMSC'er til at differentiere til modne osteoblaster.
Trin fire:Translationel undersøgelse
Styret af data fra in vitro eksperimenter, Deng et al. undersøgte in vivo biofunktionaliteten af den mikrofibrøse membran ved hjælp af en dyremodel. For det, de skabte knogledefekter af kritisk størrelse på musekranier og anbragte fibrøse membraner for at dække defekterne, efterfulgt af knogledannelsestest ved hjælp af mikrocomputertomografi (micro-CT), histologiske analyser og fluorescerende mærkning; fire til otte uger efter implantation.
Da de undersøgte 3D-billederne af mikro-CT-kranierne, 2 procent PDA/PCL-membranen tilbød de største områder med ny knogledannelse, med betydelig ekspansion til midten af knogledefekten. Forskerne opnåede et højere indhold af forkalket matrix og knogleremodellering i de 2 procent PDA/PCL-membraner til fænomenal osteokonduktiv integration.
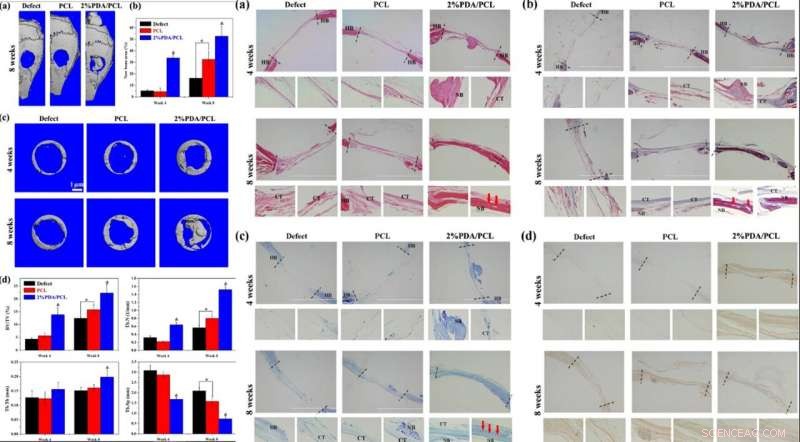
VENSTRE:In vivo evaluering af PDA/PCL fibrøse membraner. (a) Rekonstruerede 3D mikro-CT-billeder af hele kranier efter operation ved 8 uger. (b) Kvantificering af nye knogleområder efter 4 og 8 uger. (c) Mikro-CT-billeder af defekterne og d-knoglehistomorfometri af membranimplantater analyseret ud fra mikro-CT-data efter 4 og 8 uger. * repræsenterer p < 0,05 mellem grupper, og &repræsenterer p < 0,05 sammenlignet med andre grupper. TIL HØJRE:Histologisk og immunhistologisk analyse Histologisk og immunhistologisk analyse af sektionerne for kun calvariale defekter og defekter implanteret med PCL og 2 % PDA/PCL fibrøse membraner 4 og 8 uger efter implantation:(a) H&E-farvning, (b) Masson-farvning, (c) toluidinblå farvning, (d) og immunhistologisk farvning af OCN. HB værtsknogle; CT bindevæv; NB nydannet knogle. De røde pile i a–c peger på blodkarret. Kredit:NPG Asia Materials, doi:10.1038/s41427-019-0139-5
Hæmatoxylin og eosin (H&E) farvningen afslørede fibrøst væv i hulrummene i PCL-gruppen, med forholdsvis synlig knogleomstrukturering i 2 procent PDA/PCL-gruppen. Forskerne observerede også knogle med rigelig vaskularisering efter 8 uger efter operationen i 2 procent PDA/PCL-grupperne. De udførte yderligere farvning med Masson, toluidinblåt og immunhistokemi (IHC) farvning for at identificere ny knogle- og kollagendannelse i dybden. De kombinerede histologiske data afslørede, at anvendelse af PDA NP'er i konstruerede fibrøse membraner signifikant øger knogleregenereringen, understøtter hypotesen om, at in vitro osteodifferentiering også var effektiv in vivo.
På denne måde Yi Deng og kolleger biokonstruerede co-elektrospunne PDA NP'er med en bioinert syntetisk polymer for at konstruere bioinspirerede, fleksible og osteopromotive PDA/PCL fibrøse membraner til knoglevævstekniske anvendelser i regenerativ medicin. Mængden af PDA NP'er inkluderet i kompositten forbedrede den kemiske sammensætning markant, fiberstørrelse og mekaniske egenskaber af de udviklede membraner. Både in vitro-eksperimenter og in vivo-data validerede evnen til ny knogledannelse med 2 procent PDA/PCL-konstruktioner sammenlignet med ren PCL. De konstruerede PCL/PDA-membraner er osteoledende og nemme at transplantere med stort potentiale for GTR-applikationer.
© 2019 Science X Network
 Varme artikler
Varme artikler
-
 Forskere bruger bakterier som mikro-3D-printereVed hjælp af teknikken, forskerne har skabt finjusterede strukturer som denne model af lungealveoler. Kredit:Valeria Azovskaya Et hold ved Aalto-universitetet har brugt bakterier til at producere
Forskere bruger bakterier som mikro-3D-printereVed hjælp af teknikken, forskerne har skabt finjusterede strukturer som denne model af lungealveoler. Kredit:Valeria Azovskaya Et hold ved Aalto-universitetet har brugt bakterier til at producere -
 Mikroprocessorer fra blyantblyNår et ark grafen sidder på toppen af et ark bornitrid i en vinkel, et sekundært sekskantet mønster fremkommer, der bestemmer, hvordan elektroner flyder hen over prøven. Kredit:Brian LeRoy (Phys
Mikroprocessorer fra blyantblyNår et ark grafen sidder på toppen af et ark bornitrid i en vinkel, et sekundært sekskantet mønster fremkommer, der bestemmer, hvordan elektroner flyder hen over prøven. Kredit:Brian LeRoy (Phys -
 Billedteknik muliggør undersøgelser af dynamikken i nanokatalysatorer ved hidtil uset rumlig, tids…(PhysOrg.com) - Små katalysatormaterialer kan deltage i en lang række meget hurtige fysiske og kemiske processer, som nu kan afsløres mere præcist takket være en ny billeddannelsesmetode til dynamiske
Billedteknik muliggør undersøgelser af dynamikken i nanokatalysatorer ved hidtil uset rumlig, tids…(PhysOrg.com) - Små katalysatormaterialer kan deltage i en lang række meget hurtige fysiske og kemiske processer, som nu kan afsløres mere præcist takket være en ny billeddannelsesmetode til dynamiske -
 Forskere gør ikke -giftige, bøjeligt nanosheetEt scanningselektronmikroskopbillede af siden af en stak nanosheets. Indsatsen er et optisk mikroskopbillede af et enkelt eksfolieret nanosheet, for at vise det er optisk gennemsigtigt. Billede:Robi
Forskere gør ikke -giftige, bøjeligt nanosheetEt scanningselektronmikroskopbillede af siden af en stak nanosheets. Indsatsen er et optisk mikroskopbillede af et enkelt eksfolieret nanosheet, for at vise det er optisk gennemsigtigt. Billede:Robi
- Sådan ser du det spektakulære Geminid Meteor -brusebad
- Bevis på vandbevægelse fundet i meteoritter, der først for nylig faldt til Jorden
- Facebook ønsker at holde dig orienteret om nødsituationer, aktive skytter i dit område
- Ny vurdering identificerer globale hotspots for vandkonflikter
- Låget til CHEOPS-rumteleskopet er åbent
- Lokaliseret oxidativt drab af tumorceller af glasagtige jernnanopartikler


