Se og manipulere levende cellers funktioner
Kredit:CC0 Public Domain
En forskergruppe sammensat af professor Takayuki Shibata og hans kolleger ved Institut for Maskinteknik, Toyohashi University of Technology, har givet atomkraftmikroskopi (AFM) større funktionaliteter. Vores forskergruppe er lykkedes med minimalt invasiv kirurgi til levende celler ved hjælp af fotokatalytisk oxidation kontrolleret i et nanoskala -rum og visualisering af dynamisk information om intracellulære biomolekyler. Denne foreslåede teknik til at kontrollere og visualisere processen med cellefunktionsekspression på et højt niveau har et betydeligt potentiale som et stærkt nanofabrikation og nanomålingssystem til at løse livets mysterium.
En integreret forståelse af livsfænomener og styringen heraf er helt afgørende for den videre udvikling af det medicinske og farmaceutiske område. Tesen for at skabe livsinnovation er at løse strukturen og funktionen af biomolekyler, såsom genomer, proteiner, og sukkerkæder og løser også funktionen af celler, som er den grundlæggende enhed for livsaktivitet. Derfor, vi sigter mod at etablere en teknologi til minimalt invasiv kirurgi for at målrette levende celler på et molekylært niveau (Guds hånd til at manipulere cellernes funktion) og visualisere ændringer i den dynamiske adfærd af intracellulære biomolekyler og tilstanden af cellemembranprotein på et enkelt molekylært niveau (Guds øje for at se funktionen af celler), og dermed give en innovativ nanofabrikation og nanomålingsplatform til at løse livets mysterium.
Her, Det er lykkedes vores forskerhold at give to nye funktioner til atomkraftmikroskopi (AFM). Det første fremskridt er at belægge spidsen af en AFM-sonde med en tynd film af titaniumoxid (TiO) 2 ) kendt som en fotokatalysator. Ved denne metode, den fotokatalytiske reaktion er lokaliseret i et rum i nanoskala (100 nm-område) i nærheden af spidsens spids for at opnå minimalt invasiv cellemembranperforering. Som resultat, sandsynligheden for cellemembranperforering når 100%, og en cellelevedygtighed på 100% opnås også med succes, giver os mulighed for at verificere, at minimalt invasiv kirurgi kan udføres. Det andet fremskridt er at indsætte spidsen af en AFM-sonde belagt med sølv (Ag) nanopartikler i en levende celle. Det er således lykkedes os at erhverve et følsomt Raman-spektrum med oprindelse i protein, DNA, lipider, osv. (Tip-Enhanced Raman Spectroscopy, TERS). Ved denne metode, en forskel i forholdet mellem biomolekyler mellem en celles kerne og cytoplasma blev visualiseret som information inde i en celle, og det blev fundet, at der er en omvendt korrelation (et fænomen, der når en stiger, den anden falder) mellem proteiner og glykogen (også kaldet animalsk stivelse) som tidsmæssige ændringer i biomolekyler inde i celler.
For samtidig at opnå nanofabrikation og nanomålingsfunktioner, vi vil etablere en tipforbedret Raman spektroskopisk (TERS) funktion ved at belægge overfladen af en TiO
2
-funktionaliseret AFM-probe med Ag-nanopartikler i fremtiden. Denne funktion vil være i stand til at visualisere processen med nedbrydningsreaktioner af organiske stoffer baseret på fotokatalytisk oxidation (ændringer i molekylære strukturer) under celleoperationen. Vi vil også sigte mod at opnå et middel til at måle et enkelt molekyle i et målcellemembranprotein ved hjælp af den højmolekylære genkendelsesevne af en antigen-antistofreaktion, og vi vil sigte mod at etablere en teknik til selektiv nanofabrikation for et enkelt molekyle i målmembranproteinet identificeret ved ovenstående metoder. Det forventes, at denne foreslåede teknik kan løse livsfunktionernes mekanismer og anvendes til arbejde, såsom udvikling af nye lægemidler.
 Varme artikler
Varme artikler
-
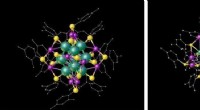 Gylden sølv nanopartikel ligner og opfører sig som guldDen gyldne sølv -nanokluster med 25 sølvatomer og 18 ligandmolekyler, (venstre) uden modion og (højre) med en modion. Strukturerne viser sølvatomer på icosahedrons hjørner (grøn), sølvatomer på icosah
Gylden sølv nanopartikel ligner og opfører sig som guldDen gyldne sølv -nanokluster med 25 sølvatomer og 18 ligandmolekyler, (venstre) uden modion og (højre) med en modion. Strukturerne viser sølvatomer på icosahedrons hjørner (grøn), sølvatomer på icosah -
 Ny hurtig syntese udviklet til tolagsgrafen og højtydende transistorerDette er konceptkunst af krystalstrukturen (ovenfra) af AB-stablet to-lags grafen. Kredit:Peter Allen, UCSB Forskere ved University of California, Santa Barbara, i samarbejde med Rice University,
Ny hurtig syntese udviklet til tolagsgrafen og højtydende transistorerDette er konceptkunst af krystalstrukturen (ovenfra) af AB-stablet to-lags grafen. Kredit:Peter Allen, UCSB Forskere ved University of California, Santa Barbara, i samarbejde med Rice University, -
 Et gennembrud inden for dråbemanipulationNår en kold/varm eller flygtig dråbe frigives på en smurt piezoelektrisk krystal (lithiumniobat) ved omgivelsestemperatur, dråben driver øjeblikkeligt en lang afstand. Kredit:University of Hong Kong
Et gennembrud inden for dråbemanipulationNår en kold/varm eller flygtig dråbe frigives på en smurt piezoelektrisk krystal (lithiumniobat) ved omgivelsestemperatur, dråben driver øjeblikkeligt en lang afstand. Kredit:University of Hong Kong -
 Fleksibel film kan føre til kræftdetektor i telefonstørrelseYoonseob Kim, ChE ph.d.-studerende, viser en fleksibel film, der inducerer cirkulær polarisering af lys. Filmen kunne en dag hjælpe læger med at opdage kræft. Filmen blev demonstreret på U-M North Cam
Fleksibel film kan føre til kræftdetektor i telefonstørrelseYoonseob Kim, ChE ph.d.-studerende, viser en fleksibel film, der inducerer cirkulær polarisering af lys. Filmen kunne en dag hjælpe læger med at opdage kræft. Filmen blev demonstreret på U-M North Cam
- Hvorfor har unge voksne mindre afslappet sex?
- Graphene varmeoverførselsgåde opklaret
- Academy advarede mod at udelukke Netflix fra Oscars
- Naturens skue:En Denali -gletsjer suser ned ad bakke, potentielt hæmmer klatrere og øger oversvøm…
- Kan vi begrænse den globale opvarmning til 1,5 grader C?
- Hvad fortæller Arktis os om klimaændringer?


