Ny ultralang cirkulerende nanopartikel udviklet til kronisk myeloid leukæmi
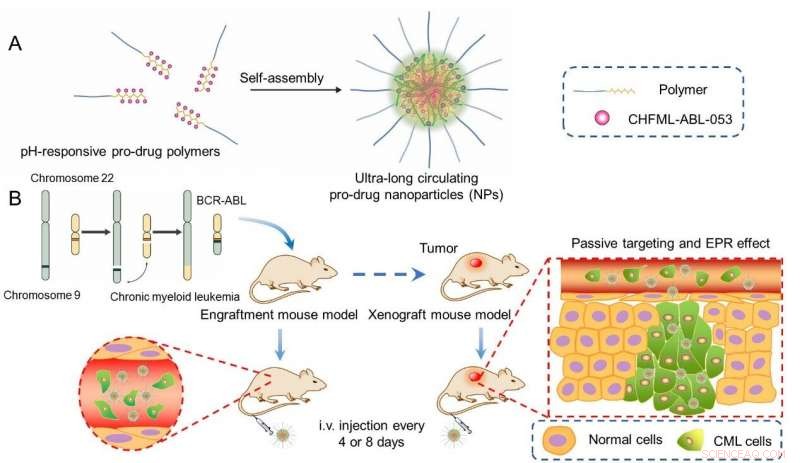
(A) Selvsamling af NP'erne og (B) deres målretning af CML på to modeller. Kredit:FU Liyi, ZOU Fengming, LIU Qingsong og LIU Jing
Et ultralangt cirkulerende nanomateriale er blevet udviklet af forskere gennem konjugering af CHMFL-ABL-053 til en amfifil polymer og efterfølgende selvsamling til en nanopartikel (NP) med høj belastning.
Udviklet af Drs. Fu Liyi og Zou Fengming, og ledet af Profs. Liu Qingsong og Liu Jing fra Institute of Health &Medical Technology, Hefei Institutes of Physical Science, formuleringen kunne i høj grad forbedre dens opløselighed og drastisk forlænge dens cirkulationshalveringstid.
Kronisk myeloid leukæmi (CML) er en klonal hæmatopoietisk stamcelle myeloproliferativ sygdom, som primært er forårsaget af den kromosomale translokation mellem Abelson (ABL) genet og breakpoint cluster region (BCR) genet. Selvom de FDA-godkendte BCR-ABL-hæmmere, såsom Imatinib og Dasatinib osv. kunne i høj grad forbedre patienternes 10-års overlevelsesrate, deres off-mål, såsom DDR1/2 og c-kit, kan føre til reduktion af mastceller, vaskulære bivirkninger og andre uønskede bivirkninger.
Tidligere relateret forskning blev udført af Prof. Liu Qingsong og Prof. Liu Jings gruppe. Og BCR-ABL-hæmmeren CHMFL-ABL-053 havde en bedre selektivitet til målet for BCR-ABL i forhold til andre proteinkinaser. Imidlertid, ligesom alle denne klasse af inhibitorer, det skal behandles oralt hver dag på grund af dets korte halveringstid, hvilket ikke kun ville øge patienternes økonomiske byrde, men også føre til kumulative toksiciteter.
Denne gang, holdet pressede deres arbejde videre for at lave en ændring baseret på deres tidligere arbejde. I 150 dages langsigtede engraftment model eksperiment, lange intravenøse doseringsintervaller af NP'erne (hver 4. eller 8. dag) udviste meget bedre overlevelse og ubetydelige toksiciteter sammenlignet med daglig oral administration af inhibitoren.
NP'erne viste fremragende inhibering af tumorvækst i den subkutane xenograft-model. Den fremragende anti-leukæmiske effektivitet af NP'erne i den lange injektionscyklus på begge modeller kan give en ny, effektiv og sikker terapeutisk strategi for BCR-ABL-positiv CML.
 Varme artikler
Varme artikler
-
 Højhastighedsmarch gennem et lag af grafenEn laserimpuls rammer et todimensionalt lag af grafen og forskyder carbonionernes elektroner. Kredit:Christian Hackenberger I samarbejde med Center for Nano-Optics ved Georgia State University i A
Højhastighedsmarch gennem et lag af grafenEn laserimpuls rammer et todimensionalt lag af grafen og forskyder carbonionernes elektroner. Kredit:Christian Hackenberger I samarbejde med Center for Nano-Optics ved Georgia State University i A -
 Kræftvaccine pakket i små partiklerLeidens forskere har udført succesrige tests ved hjælp af en ny metode til emballering af en kræftvaccine i nanopartikler. Den nye vaccine har fremkaldt en kraftig immunreaktion hos mus. Forskerne men
Kræftvaccine pakket i små partiklerLeidens forskere har udført succesrige tests ved hjælp af en ny metode til emballering af en kræftvaccine i nanopartikler. Den nye vaccine har fremkaldt en kraftig immunreaktion hos mus. Forskerne men -
 Ny måde at flytte atomisk tynde halvledere til brug i fleksible enhederBillede af den tynde film på det originale vækstsubstrat (venstre) og efter at være blevet overført (højre). Kredit:Linyou Cao. Forskere fra North Carolina State University har udviklet en ny måde
Ny måde at flytte atomisk tynde halvledere til brug i fleksible enhederBillede af den tynde film på det originale vækstsubstrat (venstre) og efter at være blevet overført (højre). Kredit:Linyou Cao. Forskere fra North Carolina State University har udviklet en ny måde -
 Forskning producerer de mest nøjagtige 3-D-billeder af 2-D-materialerBillede der viser 3D atomare koordinater af molybdæn (blå), svovl (gul) og tilsat rhenium (orange). Et 2D-billede vises under 3D-modellen. Kredit:University of California, Los Angeles Et UCLA-lede
Forskning producerer de mest nøjagtige 3-D-billeder af 2-D-materialerBillede der viser 3D atomare koordinater af molybdæn (blå), svovl (gul) og tilsat rhenium (orange). Et 2D-billede vises under 3D-modellen. Kredit:University of California, Los Angeles Et UCLA-lede
- Hvordan man laver molekyler med tandstikker & Marshmallows
- Deep learning-drevet DeepEC-ramme hjælper med nøjagtigt at forstå enzymfunktioner
- Molekylære simuleringer viser, hvordan lægemidler blokerer nøglereceptorer
- Kulturel evolution har ikke befriet jæger-samlere fra miljøtvang
- The Plants & Animals of the Coastal Plain
- Kemikere, der overraskende opdagede nanokonfinerede reaktioner, kunne hjælpe med katalytisk design


