Forskere udvikler orale insulinnanopartikler, der kunne være et alternativ til jabs

Et tværfagligt team af forskere fra NTU Singapore fra School of Materials Science and Engineering og Lee Kong Chian School of Medicine har udviklet en lag-for-lag insulin nanopartikel, der en dag kan danne grundlag for en oral medicin, og et alternativ til insulininjektioner til diabetespatienter. Kredit:NTU Singapore
Forskere ved Nanyang Technological University, Singapore (NTU Singapore) har udviklet insulinnanopartikler, der en dag kan blive grundlaget for oral medicin, og et alternativ til insulininjektioner til diabetespatienter.
I et præklinisk studie, NTU Singapore-holdet fodrede rotter med insulinholdige nanopartikler og fandt ud af, at insulin steg i deres blod minutter senere.
Insulinbehandling er ofte en vigtig del af behandlingen af diabetes, en stofskiftesygdom, der påvirker 422 millioner mennesker globalt. I Singapore, antallet af diabetikere forventes at vokse til 1 million – næsten en femtedel af befolkningen – i 2050.
Indgivelse af insulin oralt ville være at foretrække frem for insulinstik for patienter, fordi det forårsager mindre smerte end stik, og kunne dermed føre til forbedret patientcompliance. Men oral dosering er fortsat en udfordring. Da insulin er et protein, det bliver nedbrudt i mave-tarmkanalen, før det overhovedet kan nå blodbanen for at regulere blodsukkeret.
For at overkomme denne udfordring, det tværfaglige team bestående af forskere fra NTU's School of Materials Science and Engineering og Lee Kong Chian School of Medicine (LKCMedicine) designede en nanopartikel fyldt med insulin i kernen, derefter belagt med skiftende lag af insulin og chitosan, et naturligt sukker. Dosering opnås ved at kontrollere antallet af lag i nanopartiklerne.
Gennem laboratorieforsøg med cellekulturer og rottemodeller, holdet ledet af NTU-hovedforsker Dr. Huang Yingying, Lektor Yusuf Ali og tidligere NTU-professor Subbu Venkatraman, demonstreret, at denne lag-for-lag-coatede nanopartikel er stabil, når den passerer gennem maven ind i tyndtarmen med minimal insulinfrigivelse, og er i stand til at passere gennem tarmvæggene ind i blodbanen.
Dr. Huang Yingying fra School of Materials Science and Engineering på NTU, undersøgelsens medansvarlige forfatter, sagde:"Bestræbelser på at udvikle orale insulinprodukter har kun haft ringe succes, fordi disse produkter enten indebærer en sikkerhedsrisiko, eller kræver hyppig dosering på grund af lægemidlets evne til kun at indeholde en lille mængde insulin. Testene af vores NTU-udviklede insulinnanopartikel i rotter viser, at den kan bære en tilstrækkelig stor mængde insulin til den ønskede terapeutiske effekt og samtidig er lille nok til at passere gennem tarmvægge ind i blodbanen. Dette indikerer dets potentielle anvendelse til oral insulinlevering hos mennesker. Vi mener, at det samme koncept også kunne være nyttigt for andre proteinlægemidler, der normalt skal injiceres."
Lektor Yusuf Ali fra NTU LKCMedicine, undersøgelsens medforfatter, sagde:"Insulin indgives nu under huden med en fin nål flere gange om dagen, afhængig af formuleringen. Bortset fra smerten og besværet, disse stød kommer også med en risiko for, at patienter er uvidende om deres lave blodsukkerniveau, som kan udvikle sig til en potentielt dødelig tilstand hos en diabetiker. LKCMedicine tager nu udviklingen af denne nanopartikel fremad med mere præklinisk arbejde, og vi håber på, at vores arbejde en dag kan erstatte smertefulde insulininjektioner med en enkel og lille pille."
Resultaterne blev offentliggjort i det videnskabelige tidsskrift Nanoskala i november.
En flerlags tilgang til oral insulinlevering
Insulin er et naturligt forekommende hormon, der er afgørende for reguleringen af blodsukkerniveauet, især efter et måltid.
Hos raske personer, insulin produceret i bugspytkirtlen kommer ind i blodbanen og distribueres til vigtige metaboliske organer. Det instruerer leveren, muskler, og fedtceller til at optage mere glukose fra blodbanen og gemme det til fremtidig brug.
På samme tid, insulin skubber leveren for at sænke hastigheden af ny glukoseproduktion, og alt i alt, disse tjener til effektivt at reducere blodsukkerniveauet.
I modsætning, diabetic patients do not produce sufficient insulin to meet the body demands. In serious cases, insulin needs to be given via a needle into the fatty tissue beneath the skin. Derfra, it goes into the general blood circulation throughout the body before traveling to the liver.
The NTU-developed oral insulin nanoparticle more closely mimics the route by which natural insulin enters the bloodstream from the liver, an important organ for controlling blood glucose levels.
Each of these nanoparticles is about 200nm in size—at least 1, 000 times smaller than a pollen grain. Insulin is first loaded into the liposome, a tiny sphere at the core of the nanoparticle. The liposome is then coated with 11 alternating layers of insulin and chitosan of three different molecular weights, an approach that allows more insulin to be loaded.
When the insulin nanoparticle enters an acidic environment of the stomach, its layers start to repel each other, resulting in the slow release of insulin from the outermost layer, and leading inwards. While it loses some insulin as it travels down the gastrointestinal tract, the nanoparticle has enough coatings that by the time it is transported through the intestinal wall and into the bloodstream, the insulin in the remaining layers and at the liposome core is still intact.
Proof-of-concept study
To investigate the feasibility of the insulin nanoparticle for oral delivery, the NTU team first conducted a series of lab experiments to establish the nanoparticle's stability, its ability to pass through the intestinal wall, and the efficacy of the insulin in the nanoparticles that have been transported through the intestinal wall.
After leaving the nanoparticles in fluid that simulates the stomach environment, the team found that 6 percent of the insulin from the nanoparticle was released in one hour, and 94 percent remained encapsulated. It takes about one hour for food to pass through the stomach and into the small intestine, which has a less harsh environment.
When tested on the human cell line Caco-2—a widely used model for studying the transport of molecules across the intestinal wall—the scientists found that the amount of insulin transported across was three times higher when loaded into the nanoparticle, compared to bare insulin solution.
The scientists also tested the rate at which nanoparticle insulin is absorbed and cleared in the bloodstream of rats. In rats fed orally with insulin nanoparticles, the insulin concentration in the blood peaked at the 30-minute mark and was entirely eliminated in four hours.
Assoc Prof Yusuf Ali said:"Taken together, these lab experiments showed that our layer-by-layer approach limited the exposure of insulin to the gastrointestinal environment, preventing premature degradation of the insulin. We are now studying if this peak comes earlier than the 30-minute mark—an indicator of how closely the insulin from our nanoparticle follows the ebb and flow of naturally-produced insulin in the bloodstream."
The rapid absorption and elimination of insulin released from these multi-layered nanoparticles demonstrates a proof of concept in replicating meal-related metabolic responses in individuals without diabetes, said Dr. Huang, adding that the level of insulin concentration can be further increased by repeating the number of alternating insulin and chitosan layers on the nanoparticle surface.
Sidste artikelSelvfoldende 3-D lysfølsomme grafenarkitekturer
Næste artikelFysikere opdager forenende mønster i todimensionel ferroelektrik
 Varme artikler
Varme artikler
-
 Gone fishing:Forskere afbilder teknik trolde i stille cellulære havVed at fastgøre en lang nanonål til enden af en AFM-sonde, forskere kan få billeder i høj opløsning af prøver i væske, mens cantileveren svinger i fri luft. Kredit:Majid Minary Erfarne lystfiske
Gone fishing:Forskere afbilder teknik trolde i stille cellulære havVed at fastgøre en lang nanonål til enden af en AFM-sonde, forskere kan få billeder i høj opløsning af prøver i væske, mens cantileveren svinger i fri luft. Kredit:Majid Minary Erfarne lystfiske -
 Forskere gør gennembrud inden for batteriteknologiDr. Kevin Ryan, afbilledet på Materials and Surface Science Institute (MSSI), Universitetet i Limerick. Forskere ved Materials and Surface Science Institute (MSSI), University of Limerick har gjor
Forskere gør gennembrud inden for batteriteknologiDr. Kevin Ryan, afbilledet på Materials and Surface Science Institute (MSSI), Universitetet i Limerick. Forskere ved Materials and Surface Science Institute (MSSI), University of Limerick har gjor -
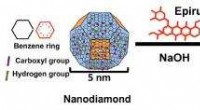 Lovende brug af nanodiamanter til at dræbe kemoresistente kræftstamceller mere effektivtFigur 1:Skematisk model, der viser overflade og kemisk struktur af nanodiamant (ND) og Epirubicin (Epi), syntese og aggregering af Epirubicin-ND-kompleks (EPND). ND repræsenteret i trunkeret oktaeders
Lovende brug af nanodiamanter til at dræbe kemoresistente kræftstamceller mere effektivtFigur 1:Skematisk model, der viser overflade og kemisk struktur af nanodiamant (ND) og Epirubicin (Epi), syntese og aggregering af Epirubicin-ND-kompleks (EPND). ND repræsenteret i trunkeret oktaeders -
 Nye muligheder for transparente kontaktelektroderNanotrådene har diametre omkring 0,1 mikrometer og længder mellem 5 og 10 mikrometer. Kredit:Billede: ACS Nano 3:1767-1774 Findes i fladskærme, solcellemoduler, eller i nye organiske lysemitteren
Nye muligheder for transparente kontaktelektroderNanotrådene har diametre omkring 0,1 mikrometer og længder mellem 5 og 10 mikrometer. Kredit:Billede: ACS Nano 3:1767-1774 Findes i fladskærme, solcellemoduler, eller i nye organiske lysemitteren
- Ny forskning forudsiger, hvilke træer der har størst risiko for billeinvasion
- Katalyserer ammoniakdannelse ved lavere temperaturer med ruthenium
- Fem aktive vulkaner på min Asia Pacific Ring of Fire-overvågningsliste lige nu
- Bidekraftforskning afslører dinosaur-spisende frø
- Mærkelige virksomheder:Myredronninger begraver døde for at forhindre sygdom
- Sådan laver du en vekselstrømstrøm Electromagnet


