Nanobiomateriale øger neuronal vækst hos mus med rygmarvsskader
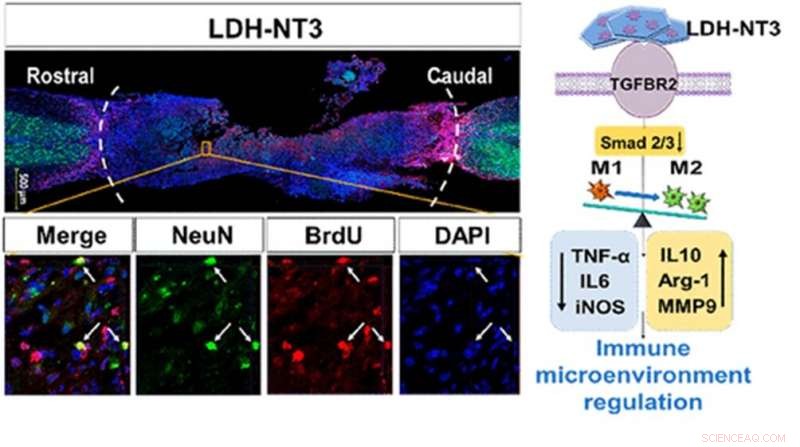
Forskere fra afdelingen for ortopædi på Tongji Hospital har med succes brugt et nanobiomateriale kaldet lagdelt dobbelthydroxid (LDH) til at hæmme det inflammatoriske miljø omkring rygmarvsskader hos mus, accelerere regenerering af neuroner og genopbygning af det neurale kredsløb i rygsøjlen. Kredit:Liming Cheng, Rongrong Zhu, Ortopædisk afdeling, Tongji Hospital ved Tongji University
Forskere fra afdelingen for ortopædi på Tongji Hospital ved Tongji University i Shanghai har med succes brugt et nanobiomateriale kaldet lagdelt dobbelthydroxid (LDH) til at hæmme det inflammatoriske miljø omkring rygmarvsskader hos mus, accelerere regenerering af neuroner og genopbygning af det neurale kredsløb i rygsøjlen. Forskerne var også i stand til at identificere den underliggende genetiske mekanisme, hvormed LDH virker. Denne forståelse bør muliggøre yderligere modifikation af terapien, som i kombination med andre elementer, endelig kunne producere en omfattende, klinisk anvendeligt system til lindring af rygmarvsskade hos mennesker.
Forskningen blev vist i tidsskriftet American Chemical Society ACS Nano den 2. februar.
Der er ingen effektiv behandling for rygmarvsskader, som altid er ledsaget af neuronernes død, brud af axoner eller nervefibre, og betændelse. Selvom kroppen fortsætter med at generere nye neurale stamceller, dette inflammatoriske mikromiljø (det umiddelbare, småskalaforhold på skadestedet) hæmmer alvorligt regenerering af neuroner og axoner. Stadig værre, den forlængede aktivering af immunceller i dette område resulterer også i sekundære læsioner af nervesystemet, til gengæld forhindrer stamcellerne i at differentiere sig til nye celletyper.
Hvis dette aggressive immunrespons på skadestedet kunne modereres, der er mulighed for, at neurale stamceller kan begynde differentiering, og neural regenerering kan forekomme.
I de seneste år, en række nye biomaterialer i nanoskala - naturlige eller syntetiske materialer, der interagerer med biologiske systemer - er blevet designet til at hjælpe med aktivering af neurale stamceller, sammen med deres mobilisering og differentiering. Nogle af disse "nanokompositter" er i stand til at levere lægemidler til skadestedet og fremskynde neuronal regenerering. Disse nanokompositter er særligt attraktive til rygmarvsbehandling på grund af deres lave toksicitet. Imidlertid, få har nogen evne til at hæmme eller moderere immunreaktionen på stedet, og derfor ikke tackle det underliggende problem. I øvrigt, de underliggende mekanismer for, hvordan de virker, er stadig uklare.
Nanolagdelt dobbelthydroxid (LDH) er en slags ler med mange interessante biologiske egenskaber, der er relevante for rygmarvsskader, herunder god biokompatibilitet (evne til at undgå afstødning fra kroppen), sikker biologisk nedbrydning (nedbrydning og fjernelse af molekylerne efter påføring), og fremragende anti-inflammatorisk evne. LDH er allerede blevet udforsket bredt i biomedicinsk teknik med hensyn til immunresponsregulering, men hovedsageligt inden for antitumorterapi.
"Disse egenskaber gjorde LDH til en virkelig lovende kandidat til at skabe et meget mere gavnligt mikromiljø til genopretning af rygmarvsskade, " siger Rongrong Zhu fra afdelingen for ortopædi på Tongji Hospital, første forfatter til undersøgelsen.
Under ledelse af Liming Cheng, tilsvarende forfatter til undersøgelsen, forskerholdet transplanterede LDH til skadestedet på mus, og fandt ud af, at nanobiomaterialet havde signifikant accelereret migration af neurale stamceller, neural differentiering, aktivering af kanaler til neuron excitation, og induktion af aktionspotentiale (nerveimpuls) aktivering. Musene udviste også signifikant forbedret lokomotivadfærd sammenlignet med kontrolgruppen af mus. Ud over, når LDH blev kombineret med Neurotrophin-3 (NT3), et protein, der fremmer vækst og differentiering af nye neuroner, musene havde endnu bedre restitutionseffekter end LDH alene. I det væsentlige, NT3 booster neuronal udvikling, mens LDH skaber et miljø, hvor denne udvikling får lov til at trives.
Derefter, via transskriptionel profilering, eller analyse af genekspression af tusindvis af gener på én gang, forskerne var i stand til at identificere, hvordan LDH udfører sin assistance. De fandt ud af, at når først LDH er knyttet til cellemembraner, det fremkalder større aktivering af genet "transforming growth factor-β-receptor 2" (TGFBR2), faldende produktion af de hvide blodlegemer, der forstærker inflammation og øget produktion af de hvide blodlegemer, der hæmmer inflammation. Ved påføring af et kemikalie, der hæmmer TGFBR2, de fandt, at de gavnlige virkninger var vendt.
Forståelsen af, hvordan LDH udfører disse effekter, skulle nu give forskerne mulighed for at tilpasse terapien for at forbedre dens ydeevne og endelig skabe et omfattende terapeutisk system for rygmarvsskader - der kombinerer disse biomaterialer med neurotrofiske faktorer som NT3 - der kan bruges i klinisk anvendelse på mennesker.
 Varme artikler
Varme artikler
-
 Siliciumoxidhukommelser overskrider en forhindringEt scanningselektronmikroskopbillede viser detaljer om et 1-kilobit tværstangshukommelsesarray designet og bygget på Rice University ved hjælp af siliciumoxid som det aktive element. Kredit:Tour Group
Siliciumoxidhukommelser overskrider en forhindringEt scanningselektronmikroskopbillede viser detaljer om et 1-kilobit tværstangshukommelsesarray designet og bygget på Rice University ved hjælp af siliciumoxid som det aktive element. Kredit:Tour Group -
 Super SQUID:Måleenhed til superledere slår verdensrekorderEt afsnit af et scanningsprobesmikroskop ved hjælp af verdens mindste SQUID (Superconducting Quantum Interference Device) skabt til dato, sondering af en prøve for at måle dets magnetfelt. Dette nye i
Super SQUID:Måleenhed til superledere slår verdensrekorderEt afsnit af et scanningsprobesmikroskop ved hjælp af verdens mindste SQUID (Superconducting Quantum Interference Device) skabt til dato, sondering af en prøve for at måle dets magnetfelt. Dette nye i -
 Guldnanomembraner modstår bøjning i nyt eksperimentEt internationalt team af forskere har opdaget, hvordan man måler en nanomembrans modstand mod både bøjning og strækning ved at rulle det ind i et rør og udføre et enkelt eksperiment for at måle røret
Guldnanomembraner modstår bøjning i nyt eksperimentEt internationalt team af forskere har opdaget, hvordan man måler en nanomembrans modstand mod både bøjning og strækning ved at rulle det ind i et rør og udføre et enkelt eksperiment for at måle røret -
 GO dej gør grafen let at forme og formeMeget bearbejdelig og alsidig, GO-dejen kan let omformes ved at skære, knibe, støbning og udskæring. Kredit:Jiaxing Huang/Northwestern University Et team fra Northwestern University omformer grafe
GO dej gør grafen let at forme og formeMeget bearbejdelig og alsidig, GO-dejen kan let omformes ved at skære, knibe, støbning og udskæring. Kredit:Jiaxing Huang/Northwestern University Et team fra Northwestern University omformer grafe
- Dyr & Planter i Aquatic Biome
- Indblik i potentielle substitutter for dyr platin i brændselscellekatalysatorer
- Politiet arresterer demonstranter på Hawaii, der forsøger at blokere teleskopet
- Polarimetrisk paritet-tid-symmetrisk fotonisk system
- Tre forskellige varianter af magnetiske domænevægge opdaget i helimagnetisk jerngermanium (FeGe)
- Hjernelignende computerchips kan afhjælpe bekymringer om privatlivets fred og drivhusemissioner


