Forskere beskriver en mulig sygdomsfremkaldende mekanisme i hypertrofisk kardiomyopati
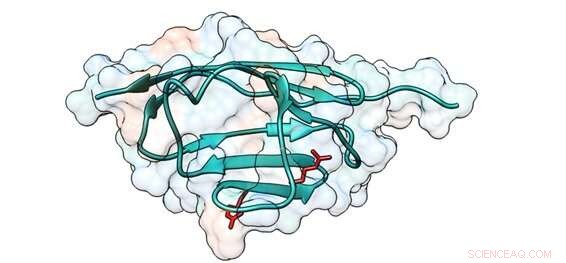
Skema af en cMyBP-C-region, hvor mutationer forårsager aminosyreændringer, der ændrer proteinets mekaniske egenskaber. Positionerne af de berørte aminosyrer er vist med rødt. Kredit:CNIC
Forskere ved Centro Nacional de Investigaciones Cardiovasculares (CNIC) har beskrevet en potentiel sygdomsfremkaldende mekanisme i hypertrofisk kardiomyopati (HCM), den hyppigste arvelige sygdom i hjertet. Studiet, offentliggjort i tidsskriftet ACS Nano , giver den første beskrivelse af en sammenhæng mellem denne sygdom og mekaniske ændringer af en komponent i hjertets kontraktile maskineri.
Hjertemusklen er under konstant mekanisk stress gennem hele livet, da den trækker sig sammen for at pumpe blod til kroppen. Laboratoriet ledet af Dr. Jorge Alegre-Cebollada undersøger, hvordan de mekaniske egenskaber af hjerteproteinerne bestemmer denne muskels fysiologiske adfærd, og hvordan ændringer i disse egenskaber fører til fremkomsten af sygdomme som HCM. I denne sygdom, den hyppigste arvelige sygdom, der påvirker hjertet, venstre ventrikel bliver forstørret, og alvorlige manifestationer omfatter hjertesvigt og pludselig død.
Forskere har i mere end 20 år vidst, at HCM er forårsaget af mutationer i proteiner med en mekanisk funktion i hjertet. En af udfordringerne ved kardiovaskulær genetik er at identificere, hvilke af de genetiske varianter, der findes hos patienter og deres familier, der forårsager sygdom. Det er vigtigt at vide, om en mutation er sygdomsfremkaldende eller ej, fordi denne information vil bestemme den kliniske opfølgning af familiemedlemmer og, potentielt, deres behandling.
Den nye undersøgelse, koordineret af Dr. Jorge Alegre-Cebollada, analyseret hjertemyosinbindende protein C (cMyBP-C).
Første forfatter Carmen Suay-Corredera forklarede, at cMyBP-C, som regulerer hjertesammentrækning, er det hyppigst muterede protein hos HCM-patienter. "En høj andel af mutationer i cMyBP-C-genet forårsager aminosyreændringer i proteinet; de mekanismer, hvorved disse mutationer forårsager HCM, er ikke præcist kendte."
Dr. Alegre-Cebolladas gruppe, i tæt samarbejde med kliniske og molekylære forskere i Europa og USA, oprette en database over cMyBP-C varianter med en klar forbindelse til HCM med henblik på at definere de molekylære defekter, der ligger til grund for sygdommen.
Brug af bioinformatik og eksperimentelle tilgange, forskerholdet opdagede, at omkring halvdelen af disse mutationer påvirker integriteten af cMyBP-C messenger RNA (mRNA) eller protein. Disse resultater er allerede blevet accepteret til offentliggørelse i Journal of Biological Chemistry og har været genstand for en kommentarartikel i det førende medicinske genetiktidsskrift Genetik i medicin .
Mens ændringer i mRNA eller proteinintegritet kunne forklare patogeniciteten af halvdelen af mutationerne analyseret i den tidligere undersøgelse, Suay-Carredera påpegede, at den anden halvdel ikke forårsager sygdom ad denne vej.
"Det er netop disse varianter, som forårsager HCM gennem ukendte mekanismer, som vi analyserede i den nye undersøgelse, " forklarede Dr. Alegre-Cebollada, der leder gruppen Molecular Mechanics of the Cardiovascular System på CNIC.
Ved at bruge avancerede biofysiske teknikker baseret på atomkraftmikroskopi, holdet viste, at nogle af de sygdomsfremkaldende mutationer i cMyBP-C producerer defekter i proteinets mekaniske egenskaber, der kan ændre den kontraktile funktion af cardiomyocytter hos HCM-patienter.
"Vi undersøger nu de sygdomsfremkaldende mekanismer af de varianter, der ikke har været forbundet med nogen relevant ændring i tidligere undersøgelser, " sagde Dr. Alegre-Cebollada. Til dette projekt, forskerne arbejder med en række eksperimentelle systemer, fra molekylære systemer til dyremodeller af HCM.
At identificere de molekylære mekanismer, der ligger til grund for HCM, er afgørende for at bestemme, hvilke cMyBP-C-mutationer, der forårsager sygdommen. Denne viden er derfor også afgørende for den kliniske opfølgning og eventuel behandling af patienter og deres familier, siger forfatterne.
 Varme artikler
Varme artikler
-
 Forskere demonstrerer forbedret katalysatorstyring, kan resultere i energibesparelserSyntese og skematisk mekanisk model af ligandstabiliserede åbne klynger. Kredit: Naturnanoteknologi (Phys.org) — Inspireret af, hvordan enzymer virker i naturens biologiske processer, forskere ha
Forskere demonstrerer forbedret katalysatorstyring, kan resultere i energibesparelserSyntese og skematisk mekanisk model af ligandstabiliserede åbne klynger. Kredit: Naturnanoteknologi (Phys.org) — Inspireret af, hvordan enzymer virker i naturens biologiske processer, forskere ha -
 Nanotech filterbelægning giver løfte mod COVID-19Fysikprofessor Seamus Curran har udviklet en belægning designet til at blive brugt på luftfiltre, i stand til at fange luftbårne viruspartikler og fange dem på filterets belægning uden at begrænse luf
Nanotech filterbelægning giver løfte mod COVID-19Fysikprofessor Seamus Curran har udviklet en belægning designet til at blive brugt på luftfiltre, i stand til at fange luftbårne viruspartikler og fange dem på filterets belægning uden at begrænse luf -
 Forskere afslører, hvordan grapefrugter udgør et hemmeligt våben til levering af lægemidlerLipider (højre panel første tre rør) afledt af grapefrugt. GNVer kan effektivt levere en række terapeutiske midler, herunder DNA, RNA (DIR-GNVer), proteiner og anti-cancer lægemidler (GNVs-Drugs) som
Forskere afslører, hvordan grapefrugter udgør et hemmeligt våben til levering af lægemidlerLipider (højre panel første tre rør) afledt af grapefrugt. GNVer kan effektivt levere en række terapeutiske midler, herunder DNA, RNA (DIR-GNVer), proteiner og anti-cancer lægemidler (GNVs-Drugs) som -
 Etableret masseproduktionsteknologi til fast-opløsning legerede nanopartiklerFig. 1 STEM-EDX-analyse af ternære legeringsnanopartikler i fast opløsning. Legeringsopløsningstilstandsevaluering. 10 nm størrelse partikler er en bærer, og partiklerne på 1 til 2 nm, der klæber til
Etableret masseproduktionsteknologi til fast-opløsning legerede nanopartiklerFig. 1 STEM-EDX-analyse af ternære legeringsnanopartikler i fast opløsning. Legeringsopløsningstilstandsevaluering. 10 nm størrelse partikler er en bærer, og partiklerne på 1 til 2 nm, der klæber til
- Kemisk sensor på basis af materialer, der besidder molekylær hukommelse
- Forskere maler nanorør for at få nanobånd
- Sådan fortæller du forskellen mellem mandlige og kvindelige Elephants
- Mål:Lægemiddelresistente bakterier
- Slamdrevne bakterier genererer mere elektricitet, hurtigere
- Succesfulde forskningsartikler citerer unge referencer


