Forskere forklarer, hvordan nanomateriale hjælper antistofrespons
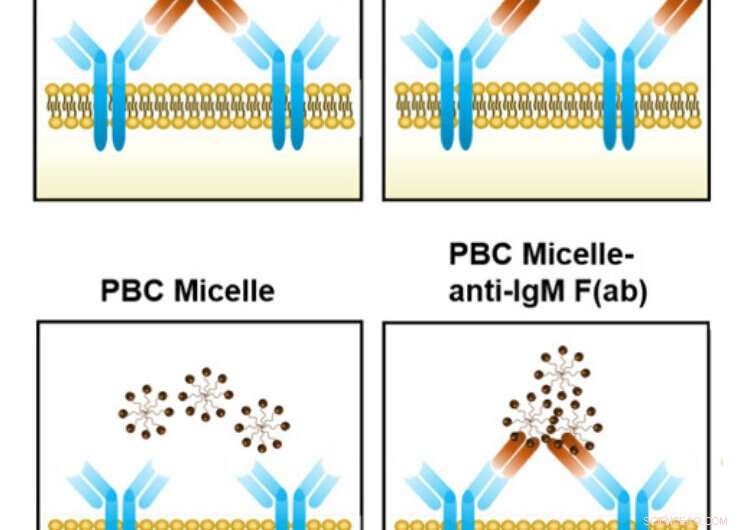
Illustrationen viser, hvordan et nanomateriale forbinder sig med receptorer på immunsystemets B-celler og hjælper dem med at igangsætte antistofproduktion. De to øverste paneler viser anti-immunoglobulin-antistoffragmenter (brune), der binder til immunsystemets B-cellereceptorer (blå). Miceller (sfærer) interagerer ikke med B-cellereceptorer uden disse fragmenter (nederste venstre panel). I nærværelse af fragmenterne, micellerne forbinder fragmenterne og B-cellereceptorerne (nederste højre panel), at øge antistofproduktionen. Kredit:Nanovaccine Institute
Forskernes oprindelige opgave var at finde ud af, hvordan visse polymere nanomaterialer sørgede for en lavinflammatorisk immunrespons og alligevel var i stand til at øge antistofproduktionen som en del af en enkelt dosis vaccine.
Da de først lærte, hvordan disse nanomaterialer på kun 20 til 30 milliardtedele af en meter i størrelse fungerede som vaccinehjælpende adjuvanser, de besluttede at tage det næste videnskabelige skridt.
Kunne de samme små adjuvanser bære antigener fra den virkelige verden til immunsystemets B-celler og gøre dem til antistof-udskillende fabrikker? Ud over, kunne dette være en alternativ måde at producere laboratorieantistoffer til diagnostiske og terapeutiske anvendelser?
Svarene var ja. Cellekultureksperimenter med teknikken producerede antistoffer mod nøgleantigener fra coronavirus, der forårsager COVID-19, og bakterien, der forårsager lungepest.
Den første observation og efterfølgende opdagelse viser, hvordan forskere tilknyttet Nanovaccine Institute baseret på Iowa State University ser på deres forskning fra mange perspektiver:
"Dette er et godt eksempel på det sunde tovtrækkeri mellem en grundforskningsfund om mekanismen for antistofproduktion og en translationel fordel, som vi kan have opfundet en ny antistofproduktionsplatform, " sagde Balaji Narasimhan, direktøren for Nanovaccine Institute, en Iowa State Anson Marston Distinguished Professor in Engineering og Vlasta Klima Balloun Faculty Chair. "Nanovaccine Instituttet brænder begge sider af det stearinlys."
Journalen Videnskabens fremskridt for nylig offentliggjort forskernes resultater. Første forfatter er Sujata Senapati, en tidligere Iowa State ph.d.-studerende i kemisk og biologisk ingeniørvidenskab. Tilsvarende forfattere er Narasimhan og Surya Mallapragada, en Iowa State Anson Marston Distinguished Professor in Engineering, en associeret vicepræsident for forskning og Carol Vohs Johnson Chair i Chemical and Biological Engineering. (Se sidebjælken for hele forskerholdet.)
Tilskud fra National Institute of Allergy and Infectious Diseases, en del af National Institutes of Health, støttet forskernes arbejde.
Det er ligesom en stige
Det var klart for forskerne, at disse nanomaterialer - "pentablok copolymer miceller, " ifølge forskernes papir - hjalp B-celler med at initiere antistofproduktion. (Miceller er strukturer, der samler sig selv i vand eller olier, efterhånden som deres molekyler tilpasser sig på grund af deres vandelskende eller vandhadende egenskaber.)
"Fra vores undersøgelser, vi forstod meget tidligt, at disse selvsamlende miceller er forskellige fra de andre typer adjuvanser derude, "Senapati sagde. "Hvad vi ikke vidste var årsagen bag denne unikke type immunrespons genereret af dem, og det var for mig den mest spændende del af dette projekt."
Mallapragada sagde, at forskerne var i stand til at skræddersy kemien af nanomaterialerne, skabe "miceller med ekstra funktionalitet."
En af disse funktioner er positiv ladede micellers evne til at associere med flere antigener og interagere direkte med receptorer på B-celler, ifølge avisen. Denne tværbinding af B-celle-receptorerne førte til bedre antistofproduktion og et forbedret immunrespons på en vaccine.
"Disse miceller fungerer som et stillads til at tværbinde to receptorer, " sagde Michael Wannemuehler, en associeret direktør for Nanovaccine Institute og en Iowa State professor i veterinær mikrobiologi og forebyggende medicin.
Han sagde, at tværbindingen er stærk og stabil, som en stige kroget i begge ender, og er effektiv til at stimulere antistofproduktion af B-cellerne.
Den cellulære aktivering kom uden den inflammatoriske reaktion, der ledsager andre vaccineadjuvanser, potentielt producere en "'lige rigtige' immunrespons", der kunne være "kritisk i det rationelle design af vacciner til ældre voksne", som ofte lider af kronisk inflammation, ifølge avisen.
Fremstilling af laboratorieantistoffer
Nu hvor forskerne forstod "behind-the-scenes" mekanismen bag micellernes antistofboost, Senapati sagde, at de ville se, hvad de ellers kunne finde.
"Det næste oplagte skridt var så at teste vores hypotese med antigener fra nogle virkelige patogener og se, om disse miceller potentielt kunne bruges til at producere antistoffer mod dem, " hun sagde.
De brugte micelle stilladserne til at præsentere antigener for SARS-CoV-2, virus, der forårsager COVID-19, og Yersinia pestis, bakterien, der forårsager lungepest, til B-celler i kultur.
Disse celler begyndte at generere "laboratorie-skala mængder af terapeutiske antistoffer" mod de to antigener, "yderligere at udvide værdien af disse nanomaterialer for hurtigt at udvikle modforanstaltninger mod infektionssygdomme, " ifølge avisen.
Disse antistoffer kan potentielt bruges til diagnostiske testsæt eller til behandlinger såsom de monoklonale antistoffer, der er udviklet til at behandle COVID-19, sagde Wannemuehler.
"Der er forskellige måder at producere antistoffer på, " Narasimhan sagde. "Den metode, vi fandt, er et alternativ, der kunne være ret kraftfuldt, hvis det er generaliseret til andre sygdomme. Det kunne være en plug-and-play-platform."
Fordi det er en effektiv vaccineadjuvans og antistofproducent, avisen siger, at nanomaterialeplatformen udviklet af undersøgelsesholdet er "et meget alsidigt værktøj i udviklingen af flere modforanstaltninger mod nye og genopståede infektionssygdomme."
 Varme artikler
Varme artikler
-
 Nanopartikler i forbrugerprodukter kan ændre normalt tarmmikrobiom væsentligtKredit:Mary Ann Liebert, Inc., udgivere Eksponering af en model menneskelig tyktarm for metaloxid -nanopartikler, på niveauer, der kan være til stede i fødevarer, forbrugsvarer, eller behandlet dr
Nanopartikler i forbrugerprodukter kan ændre normalt tarmmikrobiom væsentligtKredit:Mary Ann Liebert, Inc., udgivere Eksponering af en model menneskelig tyktarm for metaloxid -nanopartikler, på niveauer, der kan være til stede i fødevarer, forbrugsvarer, eller behandlet dr -
 Nogle piezoelektriske materialer kan være falskeKredit:CC0 Public Domain Piezorespons kraftmikroskopi (PFM) er den mest udbredte teknik til karakterisering af piezoelektriske egenskaber på nanoskala, dvs. til bestemmelse af visse materialers ev
Nogle piezoelektriske materialer kan være falskeKredit:CC0 Public Domain Piezorespons kraftmikroskopi (PFM) er den mest udbredte teknik til karakterisering af piezoelektriske egenskaber på nanoskala, dvs. til bestemmelse af visse materialers ev -
 Tredimensionel mikroteknologi med origami-foldekunstAntoine Legrain, doktorgradskandidat ved University of Twente, har udviklet en metode til at designe mikroteknologi i tre dimensioner. Den eksisterende minielektronik i computere og smartphones, for e
Tredimensionel mikroteknologi med origami-foldekunstAntoine Legrain, doktorgradskandidat ved University of Twente, har udviklet en metode til at designe mikroteknologi i tre dimensioner. Den eksisterende minielektronik i computere og smartphones, for e -
 Proces til overgang af to-lags grafen til diamanthårdt materiale ved stød opdagetVed at lægge tryk på nanoskalaen med et indrykker på to lag grafen, hvert enkelt atom tyk, CUNY-forskere forvandlede den bikagede grafen til et diamantlignende materiale ved stuetemperatur. Kredit:Ell
Proces til overgang af to-lags grafen til diamanthårdt materiale ved stød opdagetVed at lægge tryk på nanoskalaen med et indrykker på to lag grafen, hvert enkelt atom tyk, CUNY-forskere forvandlede den bikagede grafen til et diamantlignende materiale ved stuetemperatur. Kredit:Ell
- Undersøgelse viser, at forbrugerne bliver knyttet til mærker, der øger deres tillid
- Synchrotron X-ray kaster lys over nogle af verdens ældste dinosauræg
- Atomisk tynde byggeklodser kunne gøre optoelektriske enheder mere effektive
- Undersøgelse viser, at fodboldhold, der synger deres nationalsang med passion, er mere tilbøjelige…
- På vej til at lave en overkommelig bil, Tesla afskærer job
- Grøn omstilling:Hele verden kan lære af en lille by på Island


