Nyt lægemiddelleveringssystem frigiver kun terapeutisk last, når der er bakterier til stede
Kredit:Dahlia Alkekhia et al., ACS Applied Materials &Interfaces (2022). DOI:10.1021/acsami.2c02614
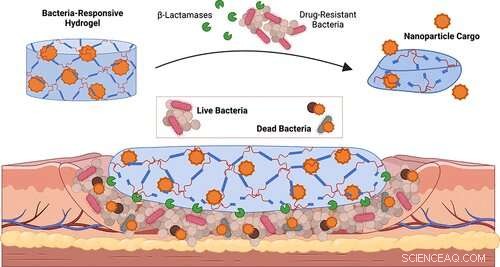
Et team af forskere fra Brown University har udviklet et nyt responsivt materiale, der kun er i stand til at frigive indkapslet last, når patogene bakterier er til stede. Materialet kunne bruges til at lave sårforbindinger, der reagerer hurtigt på spirende infektioner, men kun leverer medicin efter behov.
Udviklingen er særlig relevant i lyset af den globale krise med antibiotikaresistens, siger forskerne, da materialet kan hjælpe med at bekæmpe infektioner og samtidig adressere resistensproblemet.
"Vi har udviklet et bakterie-udløst, smart lægemiddelleveringssystem," sagde Anita Shukla, en lektor ved Browns School of Engineering, som ledede materialets udvikling. "Vores hypotese er, at teknologier som denne, der reducerer mængden af lægemiddel, der kræves for effektiv behandling, også kan reducere både bivirkninger og potentialet for resistens."
Det nye materiale, beskrevet i tidsskriftet ACS Applied Materials and Interfaces , er en hydrogel - et hydreret polymernetværk. Hydrogeler er yderst biokompatible og kan bruges til at indkapsle en række nanopartikler eller små molekyler. De bruges ofte i sårforbindinger. "Smarte" eller responsive hydrogeler dukker op som lovende platforme for lægemiddellevering. De kan fås til at reagere på det lokaliserede miljø - fremskynde eller sænke frigivelsen af medicin som reaktion på temperatur, pH eller andre faktorer.
Til dette nye materiale udviklede Shukla og hendes team en hydrogel, der er følsom over for β-lactamaser, en klasse af enzymer, der frigives af en række forskellige skadelige bakterier. Tilstedeværelsen af β-lactamaser får materialets tværbundne polymernetværk til at nedbrydes, hvilket frigiver de terapeutiske nanopartikler, der holdes indeni.
"Det interessante er, at β-lactamaser faktisk er en væsentlig årsag til antibiotikaresistens, da de ødelægger β-lactam-antibiotika, som er nogle af vores mest almindeligt ordinerede antibiotika," sagde Shukla. "Men vi har taget denne bakterielle forsvarsmekanisme og brugt den mod bakterierne."
I en række laboratorieforsøg viste Shukla og et hold af Brown-kandidatstuderende, at materialet faktisk er følsomt over for β-lactamaser, og frigiver kun nanopartikellast, når β-lactamaser eller β-lactamase-producerende bakterier var til stede. Ellers holdt materialet sin last indkapslet. Holdet planlægger at fortsætte med at udvikle og teste materialet, til sidst i de kliniske omgivelser som en sårforbinding, der kan reagere på nye infektioner.
"Vi mener, at dette er noget, der har potentialet til at blive oversat til klinikken," sagde Shukla. "Vi fortsætter med at arbejde hen imod det."
Yderligere forfattere på undersøgelsen er Dahlia Alkekhia og Cassi LaRose fra Brown's Center for Biomedical Engineering. + Udforsk yderligere
Ny indsigt i kampen mod antibiotikaresistens
 Varme artikler
Varme artikler
-
 Bor får en nano-opdatering:Forskere finder stabile 2D-strukturer med unikke egenskaberProjektioner af 2 × 2 × 1 supercelle af Pmmn-bor-struktur langs [001] og [100] retninger. (Phys.org) – National Nanotechnology Initiative definerer nanoteknologi som forståelse og kontrol af stof
Bor får en nano-opdatering:Forskere finder stabile 2D-strukturer med unikke egenskaberProjektioner af 2 × 2 × 1 supercelle af Pmmn-bor-struktur langs [001] og [100] retninger. (Phys.org) – National Nanotechnology Initiative definerer nanoteknologi som forståelse og kontrol af stof -
 Udvikling af silicium-metal kompositmateriale til genopladelige lithium-ion-batterier med høj kapac…Scanning elektronmikroskop billede af en nanostruktureret silicium-metal komposit udviklet i denne undersøgelse som et nyt anodemateriale til genopladelige Li-ion batterier. Kredit:National Institute
Udvikling af silicium-metal kompositmateriale til genopladelige lithium-ion-batterier med høj kapac…Scanning elektronmikroskop billede af en nanostruktureret silicium-metal komposit udviklet i denne undersøgelse som et nyt anodemateriale til genopladelige Li-ion batterier. Kredit:National Institute -
 En effektiv elektrokemisk interkalationsmetode til højtydende produktion af TMD nanosheetsSkematiske illustrationer af den elektrokemiske lithium-ion interkalationsbaserede eksfolieringsproces. Kredit:Yang, R., Mei, L., Zhang, Q. et al. /DOI-nummer:10.1038/s41596-021-00643-w Todimension
En effektiv elektrokemisk interkalationsmetode til højtydende produktion af TMD nanosheetsSkematiske illustrationer af den elektrokemiske lithium-ion interkalationsbaserede eksfolieringsproces. Kredit:Yang, R., Mei, L., Zhang, Q. et al. /DOI-nummer:10.1038/s41596-021-00643-w Todimension -
 Forskere udvikler magnetisk omskiftelig mekanokemoterapi for at overvinde tumorresistensIllustrationen af mekano-kemoterapien til at dræbe tumorceller. Kredit:NIMTE Prof. Wu Aiguos team på Cixi Institute of Biomedical Engineering, Ningbo Institute of Materials Technology and Engine
Forskere udvikler magnetisk omskiftelig mekanokemoterapi for at overvinde tumorresistensIllustrationen af mekano-kemoterapien til at dræbe tumorceller. Kredit:NIMTE Prof. Wu Aiguos team på Cixi Institute of Biomedical Engineering, Ningbo Institute of Materials Technology and Engine
- Adgang til DNA i cellernes kraftcenter til behandling af sygdom
- Ny indsigt i hovedårsagen til abort, opdaget fødselsdefekter
- Frankrig opfordrer til et wake-up call om skat for amerikanske webgiganter
- Undersøgelse:Sorte amerikanere er mest interesserede i COVID-19-nyheder
- NASAs nye spektrometer til at hjælpe fremtidige besætninger med at klare kosmisk stråling
- Ny planet opdaget i kredsløb om den unge Mælkevejsstjerne


