In vivo produktion af CAR-T-celler ved hjælp af virus-mimetiske fusogene nanovesikler
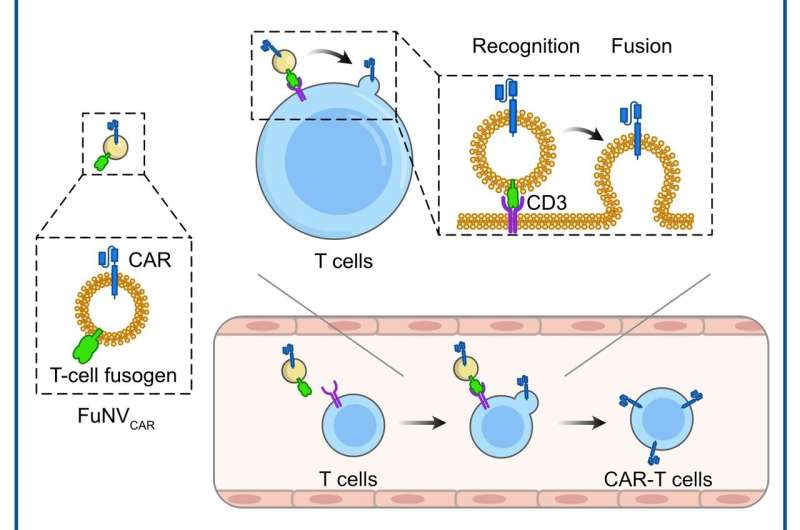
Kimæriske antigenreceptorer (CAR'er) er syntetiserede membranproteiner, der gør det muligt for lymfocytter at genkende og reagere på de specifikke antigener i målceller. På trods af den imponerende effektivitet af CAR-T-celleterapi til behandling af B-celle lymfom eller leukæmi, har den dyre og komplekse fremstillingsproces hindret dens udbredte kliniske anvendelse.
Tidligere forskning har undersøgt brugen af nanopartikler til levering af nukleinsyrer til at programmere cirkulerende T-celler in vivo, strømline CAR-T-cellegenerering og undgå behovet for at isolere T-celler fra patienter. I mellemtiden kunne indsættelse af CAR-proteinet direkte i T-cellemembranen præsentere en ligetil metode, der omgår komplikationer såsom cytokinfrigivelsessyndrom (CRS) og den tumorigeniske risiko forbundet med tilfældig viral genindsættelse i genomet.
Anført af prof. Jun Wang og prof. Cong-Fei Xu fra School of Biomedical Sciences and Engineering ved South China University of Technology, har forskere udviklet en lovende strategi, der involverer direkte fusion af CAR-molekyler, præ-udtrykt på fusogene nanovesikler (FuNV'er), til T-celler, hvorved CAR-T-celler konstrueres in vivo.
De konstruerede T-cellefusogenet ved at tilføje et anti-CD3 enkeltkædet variabelt fragment til reovirus eller mæslingevirusfusogen. De viste, at FuNV'er afledt af T-celle-fusogen-udtrykkende celler bar en betydelig mængde T-celle-fusogen, som effektivt inducerede fusionen mellem NV'er og T-celler både in vitro og in vivo.
I betragtning af den kliniske succes af anti-CD19 (αCD19) CAR-T-celler blev de konstruerede celler, der udtrykker T-cellefusogen og αCD19 CAR-protein, konstrueret til at producere αCD19 CAR-bærende FuNV'er (FuNVCAR ). CAR-T-celleproduktion blev opnået med succes ved at levere CAR-protein til T-celler via FuNVCAR in vitro og in vivo. I mellemtiden, intravenøs injektion af FuNVCAR effektivt hæmmet B-celle lymfom vækst.
For yderligere at udforske den potentielle toksicitet af FuNVCAR , blev blodtællinger og biokemiske serumanalyser udført efter 2 dage og 14 dage, hvilket viser sammenlignelighed med kontrolgruppen. Gennem hele behandlingen med FuNVCAR , blev der ikke observeret nogen signifikante ændringer i kropsvægt hos mus.
Endvidere, i modsætning til traditionel CAR-T-cellebehandling, behandling med FuNVCAR inducerede ikke en forhøjet frigivelse af inflammatoriske cytokiner. Denne observerede forskel kan tilskrives forbigående CAR-T-celler produceret af FuNVCAR , som gennemgår begrænset og midlertidig aktivering, hvilket mindsker den vedvarende frigivelse af inflammatoriske cytokiner.
Sammenfattende introducerer denne undersøgelse en ny tilgang til in vivo CAR-T-celleproduktion gennem FuNV-medieret CAR-proteinlevering. Det er dog vigtigt at bemærke, at denne strategi muligvis ikke er egnet til patienter med kompromitteret T-cellefunktion.
Resultaterne er offentliggjort i tidsskriftet Science Bulletin .
Flere oplysninger: Gui Zhao et al., In vivo-produktion af CAR-T-celler ved hjælp af virus-mimetiske fusogene nanovesikler, Science Bulletin (2023). DOI:10.1016/j.scib.2023.11.055
Leveret af Science China Press
 Varme artikler
Varme artikler
-
 En pille til levering af biomedicinske mikromotorerDisse piller kunne snart bruges til at levere bittesmå mikromotorer i menneskekroppen. Kredit:American Chemical Society At bruge små mikromotorer til at diagnosticere og behandle sygdom i menneske
En pille til levering af biomedicinske mikromotorerDisse piller kunne snart bruges til at levere bittesmå mikromotorer i menneskekroppen. Kredit:American Chemical Society At bruge små mikromotorer til at diagnosticere og behandle sygdom i menneske -
 Berøringsfølsom plastikhud heler sig selvEt lille stykke af det selvhelbredende materiale skæres i skiver med en skalpel. Forskerne siger, at materialet reparerer sig selv på omkring 30 minutter. Kredit:L.A. Cicero (Phys.org) – Et team a
Berøringsfølsom plastikhud heler sig selvEt lille stykke af det selvhelbredende materiale skæres i skiver med en skalpel. Forskerne siger, at materialet reparerer sig selv på omkring 30 minutter. Kredit:L.A. Cicero (Phys.org) – Et team a -
 Enkel skal af plantevirus udløser immunrespons mod kræftSkallene af en almindelig plantevirus, inhaleres i en lungetumor eller injiceres i æggestokkene, tyktarms- eller brysttumorer, ikke kun udløste immunsystemet hos mus til at udslette tumorerne, men gav
Enkel skal af plantevirus udløser immunrespons mod kræftSkallene af en almindelig plantevirus, inhaleres i en lungetumor eller injiceres i æggestokkene, tyktarms- eller brysttumorer, ikke kun udløste immunsystemet hos mus til at udslette tumorerne, men gav -
 Nanotekniske elektroder for at give små generatorer et løftEt 3D atomisk kraftmikroskop topografibillede af metalliske nanopartikler deponeret på grafit. Kan vores affald være en del af svaret på menneskehedens energiproblemer? Nogle forskere mener det, t
Nanotekniske elektroder for at give små generatorer et løftEt 3D atomisk kraftmikroskop topografibillede af metalliske nanopartikler deponeret på grafit. Kan vores affald være en del af svaret på menneskehedens energiproblemer? Nogle forskere mener det, t
- Nedbør vil være afgørende for, at planter kan modvirke den globale opvarmning
- Fysikere sporer, hvordan kontinuerlige ændringer i dimensionalitet påvirker en supervæskes kollek…
- Byboere kan have en overordnet indflydelse på at bremse den globale opvarmning
- ESA lytter med på sort hul-mission
- Connecticut statslige agenturer målrettet i cyberangreb
- Gyldne nano-pile danner grundlag for eksotiske nye overbygninger


