Stabilisering af mRNA-vacciner til levering til celler
Vacciner og terapier baseret på messenger-RNA kunne afgives lettere på grund af en ikke-toksisk polymer, der beskytter RNA og kontrollerer dets frigivelse inde i cellerne.
Fremkomsten af vacciner, der bruger messenger-RNA (mRNA) til at styre immunogen proteinsyntese, bedst kendt i vacciner mod COVID-19, stimulerer forskere til at finde bedre måder at holde mRNA'et stabilt og levere det effektivt.
Et team ved University of Tokyo, med samarbejdspartnere i Japan og Kina, har nu udviklet polymerer, der kan interagere med, stabilisere og indkapsle mRNA, hvilket muliggør en yderst effektiv levering til dyrkede humane celler og celler fra levende mus. De har publiceret deres arbejde i tidsskriftet Science and Technology of Advanced Materials .
"Ud over vacciner mod infektionssygdomme præsenterer mRNA lovende muligheder for hidtil usete behandlinger som proteinerstatningsterapier, genredigering og immunterapier," siger Horacio Cabral fra University of Tokyo-teamet. "Men for at frigøre det fulde potentiale af disse avancerede terapier er udviklingen af sikre og effektive bæresystemer altafgørende."
Forskerne undersøgte måder at finjustere strukturen af deres polymermolekyler for at give dem mulighed for at interagere med mRNA for at beskytte det. De biokompatible og ikke-toksiske polymerer var af en type kaldet blok-copolymerer, bygget af alternerende segmenter af forskellige kemiske grupper, i dette tilfælde polyethylenglycol og polyglycerol.
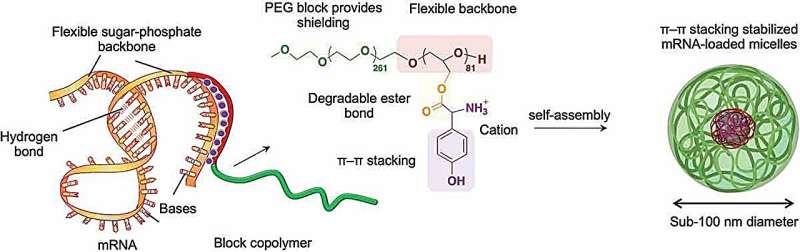
Men nøglen til at opnå passende interaktion med mRNA var at knytte specifikke positivt ladede aminosyregrupper til den lange polymerskelette. Den positive ladning tiltrækker generelt polymeren til negativt ladet RNA, og de valgte aminosyrer var også i stand til at interagere med dele af mRNA'et i en proces kaldet pi-pi (π-π) stabling. Dette involverer interaktioner mellem elektroner i et træk kaldet pi-bindinger i cykliske molekylære ringe stablet side om side i de interagerende molekyler.
"Dette er en meget tilpasselig tilgang, der tillader finjustering af vores polymers interaktioner med mRNA," siger Cabral. Som et resultat blev mRNA'et stabiliseret meget effektivt, hvilket overvindede en stor ulempe ved ustabilitet fundet med alternative tilgange.
Polymeren og mRNA samles spontant til sfæriske bundter - miceller - der effektivt leverede mRNA-lasten ind i dyrkede celler og også i museceller efter intramuskulær injektion. mRNA'et blev let frigivet inde i cellerne for at generere de proteiner, det kodede for ved høj effektivitet og i betydeligt længere tid end alternative metoder.
"Dette arbejde var meget udfordrende på grund af den sarte natur af mRNA, et meget skrøbeligt molekyle, der har brug for beskyttelse uden for målcellerne, men øjeblikkelig eksponering for cellemaskineriet, når først det er inde," siger Cabral. Han tilføjer, "Vores succes er spændende på grund af dets potentiale til at transformere mRNA-leveringsteknologier, hvilket muliggør præcis konstruktion, innovative frigivelsesstrategier og overvindelse af kritiske barrierer for at øge stabiliteten og effektiviteten i mRNA-baserede terapier."
Flere oplysninger: Wenqian Yang et al., Blok-catiomerer med flankerende hydrolyserbare tyrosinatgrupper forbedrer in vivo mRNA-levering via π–π-stabling-assisteret micellær samling, Science and Technology of Advanced Materials (2023). DOI:10.1080/14686996.2023.2170164
Journaloplysninger: Videnskab og teknologi for avancerede materialer
Leveret af National Institute for Materials Science
 Varme artikler
Varme artikler
-
 Cellulær mikroRNA-detektion med miraklerUddrag fra time-lapse-filmen af miRNA-detektion på 1 time ved hjælp af miRacles-assay. Kredit:Science Advances, doi:10.1126/sciadv.aau9443 MikroRNAer (miRNAer) er korte ikke-kodende regulatorisk
Cellulær mikroRNA-detektion med miraklerUddrag fra time-lapse-filmen af miRNA-detektion på 1 time ved hjælp af miRacles-assay. Kredit:Science Advances, doi:10.1126/sciadv.aau9443 MikroRNAer (miRNAer) er korte ikke-kodende regulatorisk -
 Discovery er nøglen til metalslid i glidende dele (m/ video)Denne billedsekvens afslører overraskende væskelignende adfærd i et massivt stykke metal, der glider over et andet, dannelse af defekter, der fører til slid på metaldele. (Øverst) To billedrammer af m
Discovery er nøglen til metalslid i glidende dele (m/ video)Denne billedsekvens afslører overraskende væskelignende adfærd i et massivt stykke metal, der glider over et andet, dannelse af defekter, der fører til slid på metaldele. (Øverst) To billedrammer af m -
 Materiale til polymersolceller kan egne sig til bearbejdning af store arealerEn demonstrationssolpark baseret på polymersolceller på Danmarks Tekniske Universitet i Roskilde, Danmark. Kredit:DTU Energi På trods af alt det løfte, de har vist i laboratoriet, polymersolceller
Materiale til polymersolceller kan egne sig til bearbejdning af store arealerEn demonstrationssolpark baseret på polymersolceller på Danmarks Tekniske Universitet i Roskilde, Danmark. Kredit:DTU Energi På trods af alt det løfte, de har vist i laboratoriet, polymersolceller -
 Nye nanoburre kan tilføje et arsenal af behandlinger mod hjertesygdomme(PhysOrg.com) - Forskere ved MIT og Harvard Medical School har bygget målrettede nanopartikler, der kan klamre sig til arterievægge og langsomt frigive medicin, et fremskridt, der potentielt giver et
Nye nanoburre kan tilføje et arsenal af behandlinger mod hjertesygdomme(PhysOrg.com) - Forskere ved MIT og Harvard Medical School har bygget målrettede nanopartikler, der kan klamre sig til arterievægge og langsomt frigive medicin, et fremskridt, der potentielt giver et
- Hurtig oprensning og karakterisering af cirkulerende små ekstracellulære vesikler på en etiketfri…
- LCO og NASAs Kepler arbejder sammen for at bestemme oprindelsen af supernova
- Nattehimlens naturlige lysstyrke
- EN RAVAN i solen
- Voldelig afbrænding afsløret i hjertet af et sort hul-system
- Sådan identificeres røde og sorte stribede slanger


