Evaluering af effekter på og uden for målet af selvsamlet EGFR siRNA leveringssystem
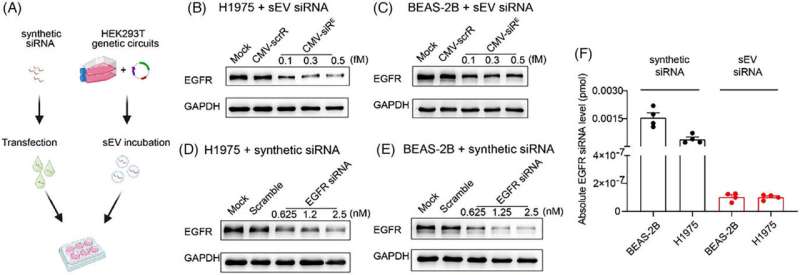
I en undersøgelse offentliggjort i Clinical and Translational Medicine , en forskergruppe fra Nanjing University evaluerede virkningerne på og uden for målet af selvsamlet siRNA-leveringssystem.
RNA-interferens (RNAi)-terapi involverer levering af små interfererende RNA (siRNA) til målceller for at fremkalde terapeutiske effekter. Selvom siRNA udviser specifik binding til målgenet for on-target-effekter, kan det også interagere med ikke-target-gener, hvilket resulterer i off-target-effekter. En af de vigtigste udfordringer i RNAi-terapi ligger således i at opnå en balance mellem on-target og off-target-effekter for at øge den ønskede on-target-påvirkning og samtidig minimere den tilhørende off-target-risiko.
Nanjing Universitys forskningsgruppe, Chen-Yu Zhang og Xi Chen, udviklede en unik siRNA-leveringstilgang ved at omprogrammere værtsleveren til at syntetisere selvsamlende siRNA'er indkapslet i små ekstracellulære vesikler (sEV'er) til levering til specifikke væv for at behandle forskellige sygdomme.
I denne undersøgelse undersøgte forfatterne yderligere virkningerne på og uden for målet af det selvsamlede siRNA-leveringssystem, idet de adresserede udfordringerne ved in vivo-siRNA-levering og fremhævede dets terapeutiske potentiale og biosikkerhed. De understregede den overlegne styrke af de selvsamlede siRNA'er til at dæmpe specifikke mål sammenlignet med syntetiske siRNA'er.
Transkriptomisk analyse bekræftede yderligere minimale off-target-effekter i normalt væv og signifikante anti-EGFR-effekter i tumorceller in vivo. Samlet set giver undersøgelsen lovende indsigt i den terapeutiske effekt og bivirkninger af det in vivo selvsamlede siRNA-leveringssystem.
Betydningen af resultaterne
Denne undersøgelse har afsløret den imponerende effektivitet af selvsamlet sEV-indkapslet siRNA, som udviste potent interferens på EGFR-protein med kun 1/2.000.000 af den syntetiske transfektionsmængde. Denne åbenbaring indikerer, at de endogent behandlede sEV-indkapslede siRNA'er problemfrit fungerer i modtagerceller på fysiologiske niveauer, mens akkumuleringen af suprafysiologiske niveauer af syntetiske siRNA'er i normale celler kan forårsage cytotoksicitet.
Derfor er den in vivo selvsamlede siRNA-leveringsstrategi ikke kun effektiv ved en ret lav siRNA-koncentration i tumorceller, men udviser også bedre biosikkerhed for somatiske celler end syntetiske siRNA'er.
SiRNA'ers off-target aktivitet kan føre til uforudsete fænotyper og kompromittere de terapeutiske fordele ved siRNA'er. Denne undersøgelse vurderede omhyggeligt de off-target-risici ved in vivo selvsamlede EGFR-siRNA'er gennem transkriptomisk sekventering.
Der blev ikke observeret nogen statistisk signifikant berigelse for perfekte match mellem EGFR siRNA-frøregionen og 3'-UTR'er af nedregulerede transkripter i normalt væv. I tumorvæv viste genontologi (GO) berigelsesanalyse, at de fleste af de øverste GO-termer var tæt forbundet med EGFR-signalering. Dataene indikerer, at virkningerne uden for målet i normalt væv er minimale sammenlignet med virkningerne på målet observeret i tumorceller.
Med hensyn til de potentielle risici forbundet med mætning af det endogene miRNA-maskineri med eksogene siRNA'er, afslørede analyse af miR-122-målgener efter in vivo selvsamlet siRNA-behandling kun 13 signifikante ændringer blandt 1.566 potentielle mål.
Størstedelen af miR-122-mål udviste lignende ekspressionsmønstre sammenlignet med ubehandlet gruppe. Disse data indikerer, at in vivo selvsamlede EGFR-siRNA'er er til stede på passende fysiologiske niveauer og har ringe chance for at forårsage hepatotoksicitet gennem forstyrrelser i de iboende miRNA-veje.
Samlet set betegner denne undersøgelse en ny retning for RNAi-terapi, der har betydelige implikationer for den kliniske indførelse af det in vivo selvsamlende siRNA-leveringssystem.
I modsætning til konventionel genterapi udviser denne metode høj specificitet med minimal risiko uden for målet og ingen toksiske bivirkninger. Derudover tilbyder undersøgelsen ny indsigt til vurdering af etablerede og ikke-etablerede bivirkninger i udviklingen af in vivo siRNA-terapi for forskellige gener.
Flere oplysninger: Hongyuan Guo et al., Evaluering af virkninger på og uden for målet af selvmonteret epidermal vækstfaktorreceptor lille interfererende RNA-leveringssystem, Klinisk og translationel medicin (2024). DOI:10.1002/ctm2.1579
Leveret af Nanjing University School of Life Sciences
 Varme artikler
Varme artikler
-
 Maskinlæring kigger ind i nano-akvarierSkemaet viser en forenklet version af de trin, forskere har taget for at forbinde væskefaseelektronmikroskopi og maskinlæring for at producere et strømlinet dataoutput, der er mindre kedeligt at behan
Maskinlæring kigger ind i nano-akvarierSkemaet viser en forenklet version af de trin, forskere har taget for at forbinde væskefaseelektronmikroskopi og maskinlæring for at producere et strømlinet dataoutput, der er mindre kedeligt at behan -
 Multikomponent nanostrukturer med justerbare optiske egenskaberBNL-forskere brugte DNA-linkere med tre bindingssteder (sorte strenge) til at forbinde guld-nanopartikler (orange og røde kugler) og fluorescerende farvestofmolekyler (blå kugler) mærket med komplemen
Multikomponent nanostrukturer med justerbare optiske egenskaberBNL-forskere brugte DNA-linkere med tre bindingssteder (sorte strenge) til at forbinde guld-nanopartikler (orange og røde kugler) og fluorescerende farvestofmolekyler (blå kugler) mærket med komplemen -
 DNA-origami tager flugten i et nyt område af nanomaskinerDNA -mekanoteknologi udvider mulighederne for forskning, der involverer biomedicin og materialevidenskab, siger Khalid Salaita, ret, professor i kemi ved Emory University og medforfatter til artiklen,
DNA-origami tager flugten i et nyt område af nanomaskinerDNA -mekanoteknologi udvider mulighederne for forskning, der involverer biomedicin og materialevidenskab, siger Khalid Salaita, ret, professor i kemi ved Emory University og medforfatter til artiklen, -
 Undersøgelse viser, at størrelsen påvirker strukturen af hule nanopartiklerDette er en halvoxideret 26 nm nanopartikel. Ni-regionen er farvet rød, og NiO er farvet blå og grøn. Kredit:Dr. Joe Tracy, North Carolina State University En ny undersøgelse fra North Carolina St
Undersøgelse viser, at størrelsen påvirker strukturen af hule nanopartiklerDette er en halvoxideret 26 nm nanopartikel. Ni-regionen er farvet rød, og NiO er farvet blå og grøn. Kredit:Dr. Joe Tracy, North Carolina State University En ny undersøgelse fra North Carolina St
- Lavt tab, all-fiber system til stærk og effektiv kobling mellem fjerne atomer
- Taiwans kæmper med betelnøddeafhængighed
- Små grafenradioer kan føre til Internet of Nano-Things
- CBS lancerer et 24-timers streaming sportsnyhedsnetværk
- Grundlæggende krav til vækst i prokaryoter og eukaryoter
- Oprettelse af en perfekt fælde til lys


