Brug af bittesmå fælder til at studere proteininteraktioner kan give ny viden om svære at behandle sygdomme

Proteiner, der danner klumper, forekommer i mange svære at behandle sygdomme, såsom ALS, Alzheimers og Parkinsons. Mekanismerne bag, hvordan proteinerne interagerer med hinanden, er svære at studere, men nu har forskere ved Chalmers Tekniske Universitet i Sverige opdaget en ny metode til at fange mange proteiner i fælder i nanostørrelse. Inde i fælderne kan proteinerne studeres på en måde, som ikke har været mulig før.
"Vi tror på, at vores metode har et stort potentiale til at øge forståelsen af tidlige og farlige processer i en række forskellige sygdomme og på sigt føre til viden om, hvordan lægemidler kan modvirke dem," siger Andreas Dahlin, professor ved Chalmers, der har ledet forskningsprojektet. .
Forskningen er blevet præsenteret i den videnskabelige artikel "Stable trapping of multiple proteins at physiological conditions using nanoscale chambers with macromolecular gates," for nylig offentliggjort i Nature Communications .
Proteiner, der danner klumper i vores kroppe, forårsager en lang række sygdomme, herunder ALS, Alzheimers og Parkinsons. En bedre forståelse af, hvordan klumper dannes, kunne føre til effektive måder at opløse dem på på et tidligt tidspunkt, eller endda forhindre dem i at dannes helt. I dag findes der forskellige teknikker til at studere de senere stadier af processen, hvor klumperne er blevet store og dannet lange kæder, men indtil nu har det været svært at følge den tidlige udvikling, hvor de stadig er meget små. Disse nye fælder kan nu hjælpe med at løse dette problem.
Forskerne beskriver deres arbejde som verdens mindste porte, der kan åbnes og lukkes med et tryk på en knap. Portene bliver til fælder, der låser proteinerne inde i kamre på nanoskala. Proteinerne forhindres i at undslippe, hvilket forlænger den tid, de kan observeres på dette niveau, fra et millisekund til mindst en time. Den nye metode gør det også muligt at indeslutte flere hundrede proteiner i et lille volumen, en vigtig egenskab for yderligere forståelse.
"De klumper, som vi gerne vil se og forstå bedre, består af hundredvis af proteiner, så hvis vi skal studere dem, er vi nødt til at kunne fange så store mængder. Den høje koncentration i det lille volumen betyder, at proteinerne naturligt støder ind i hinanden, hvilket er en stor fordel ved vores nye metode," siger Dahlin.
For at teknikken kan bruges til at studere forløbet af specifikke sygdomme, kræves der fortsat udvikling af metoden. "Fælderne skal tilpasses for at tiltrække de proteiner, der er knyttet til den særlige sygdom, du er interesseret i. Det, vi arbejder på nu, er at planlægge, hvilke proteiner der er bedst egnede til at studere," siger Dahlin.
Sådan fungerer de nye fælder
Portene, som forskerne har udviklet, består af såkaldte polymerbørster placeret ved åbningen af kamre i nanostørrelse. Proteinerne, der skal undersøges, er indeholdt i en flydende opløsning og tiltrækkes af kamrenes vægge efter en særlig kemisk behandling. Når portene er lukket, kan proteinerne frigøres fra væggene og begynde at bevæge sig mod hinanden.
I fælderne kan du studere individuelle klumper af proteiner, hvilket giver meget mere information i forhold til at studere mange klumper på samme tid. Klumperne kan for eksempel dannes af forskellige mekanismer og have forskellige størrelser og forskellige strukturer. Sådanne forskelle kan kun observeres, hvis man analyserer dem én efter én.
I praksis kan proteinerne holdes i fælderne i næsten ethvert tidsrum, men på nuværende tidspunkt er tiden begrænset af, hvor længe den kemiske markør – som de skal forsynes med for at blive synlige – bliver tilbage. I undersøgelsen lykkedes det forskerne at bevare synlighed i op til en time.
Flere oplysninger: Justas Svirelis et al., Stabil indfangning af flere proteiner ved fysiologiske forhold ved brug af kamre i nanoskala med makromolekylære porte, Nature Communications (2023). DOI:10.1038/s41467-023-40889-4
Journaloplysninger: Nature Communications
Leveret af det svenske forskningsråd
 Varme artikler
Varme artikler
-
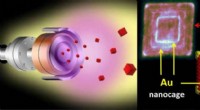 Guld til jern -nanokuberHybrid Au/Fe-nanopartikler kan vokse i en hidtil uset kompleks struktur med en enkelt-trins fremstillingsmetode. Kredit:Helsinki Universitet En af de største udfordringer inden for nanoteknologi e
Guld til jern -nanokuberHybrid Au/Fe-nanopartikler kan vokse i en hidtil uset kompleks struktur med en enkelt-trins fremstillingsmetode. Kredit:Helsinki Universitet En af de største udfordringer inden for nanoteknologi e -
 Bevis for en årtier gammel teori gemmer sig i det tyndeste af materialerKredit:University of Manchester Ved lagdeling af todimensionale (2-D) materialer, forskere som University of Manchester og Cornell University har bekræftet elektrokemiske fænomener baseret på teor
Bevis for en årtier gammel teori gemmer sig i det tyndeste af materialerKredit:University of Manchester Ved lagdeling af todimensionale (2-D) materialer, forskere som University of Manchester og Cornell University har bekræftet elektrokemiske fænomener baseret på teor -
 Liverpool-forskere konstruerer molekylære knuderDe molekylære knuder har dimensioner på omkring to nanometer Forskere ved University of Liverpool har konstrueret molekylære knuder med dimensioner på omkring to nanometer - omkring 30, 000 gange
Liverpool-forskere konstruerer molekylære knuderDe molekylære knuder har dimensioner på omkring to nanometer Forskere ved University of Liverpool har konstrueret molekylære knuder med dimensioner på omkring to nanometer - omkring 30, 000 gange -
 Undersøgelse undersøger, hvordan spin-orbit-interaktion beskytter Majorana nanotrådeEt elektronmikrograf med et skævt billede taget af en af de Majorana nanotrådsenheder, der blev brugt i undersøgelsen. Nanotråden er vist falsk i blå, som delvist er dækket af NbTiN -superlederen vi
Undersøgelse undersøger, hvordan spin-orbit-interaktion beskytter Majorana nanotrådeEt elektronmikrograf med et skævt billede taget af en af de Majorana nanotrådsenheder, der blev brugt i undersøgelsen. Nanotråden er vist falsk i blå, som delvist er dækket af NbTiN -superlederen vi
- Sådan konverteres megawatt til ampere
- I rummets tomhed, Voyager 1 registrerer plasmabrum
- Eksperimenter med solens temperatur tilbyder løsninger på solmodelproblemer
- NASA sporer Betas kraftig nedbør i nedre Mississippi -dal
- Grønlandshvaler kommer til Cumberland Sound i Nunavut for at eksfoliere
- Dramatiske vegetationsændringer i fortiden antyder en frygtelig fremtid


