Nanopartikler leverer behandling direkte til tumorer af dødelig hjernekræft
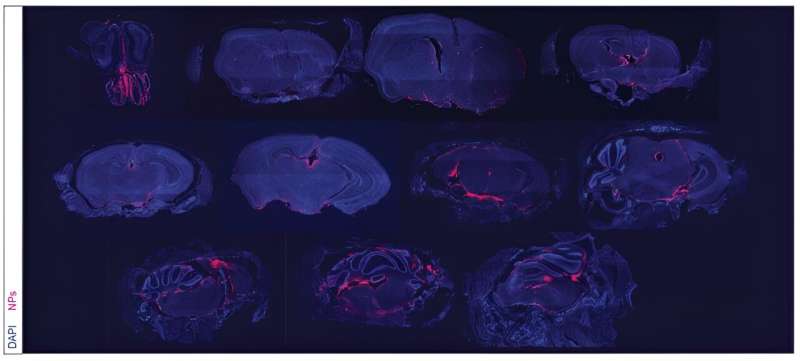
Ved at bruge nanopartikler indgivet direkte i cerebrospinalvæsken (CSF) har et forskerhold udviklet en behandling, der kan overvinde betydelige udfordringer i behandlingen af en særlig dødelig hjernekræft.
Forskerne, ledet af professorerne Mark Saltzman og Ranjit Bindra, administrerede mus med medulloblastom en behandling, der indeholder specialdesignede lægemiddelbærende nanopartikler. Studiet, offentliggjort i Science Translational Medicine , viste, at mus, der modtog denne behandling, levede signifikant længere end mus i kontrolgruppen.
Medulloblastom, en hjernekræft, der overvejende rammer børn, begynder ofte med en tumor dybt inde i hjernen. Kræften er tilbøjelig til at spredes langs to beskyttende membraner kendt som leptomeninges gennem centralnervesystemet, især overfladen af hjernen og CSF.
Leptomeningeal spredning ses i en række primære hjernetumorer, samt i hjernemetastaser fra solide tumorer i bryst, lunge og andre steder. Fordi der ikke er nogen anatomiske barrierer i CSF for at forhindre yderligere vækst, kan disse kræftformer spredes hurtigt.
Målretning af tumorer i CSF har vist sig vanskeligt, til dels fordi væsken hurtigt cirkulerer gennem centralnervesystemet omkring fire gange dagligt hos mennesker, og skyller typisk antitumorlægemidler væk, før de har haft en chance for at akkumulere og have nogen virkning.
"Det er som et vandfaldssystem med en hurtig, hurtig væskestrøm," sagde Minsoo Khang, hovedforfatter af undersøgelsen og en tidligere kandidatstuderende i Saltzmans laboratorium.
For at komme uden om denne forhindring fremstillede forskerholdet nanopartikler, der klæber til tumorer. Disse nanopartikler er designet i Saltzmans laboratorium og er lavet med nedbrydelige polymerer, der langsomt frigiver en DNA-reparationshæmmer, talazoparib, som er FDA-godkendt og i øjeblikket bruges i klinikken til en række kræftformer. Lægemidlet er et af en relativt ny klasse af kræftlægemidler kendt som PARP-hæmmere, som blokerer et enzym, der hjælper med at reparere DNA. Uden evnen til at reparere deres DNA er der større sandsynlighed for, at tumorceller dør.
Nanopartikelbehandlingen injiceres intrathecalt - det vil sige, den leveres direkte mellem leptomeningerne, der beskytter CSF. I løbet af en periode på uger opdagede forskerne tilstedeværelsen af nanopartikler i CSF i så længe som 21 dage efter en enkelt dosering.
"Vi var meget begejstrede for at have fundet et medium, der har langsigtet tilbageholdelse i dette flydende rum, som ellers er udfordrende," sagde Khang.
Behandling af hjernekræft generelt er udfordrende, da få behandlinger kan trænge igennem blod-hjerne-barrieren, et naturligt forsvarssystem, der kan blokere potentielt nyttige lægemidler. Forskerholdets metode kunne tilbyde en løsning.
"Der har været meget lidt arbejde med intrathekal levering af nanopartikler, så vi er meget begejstrede, fordi det kan give os mulighed for at gå efter leptomeningeal spredning af sygdom fra hjernemetastaser," sagde Bindra, Harvey og Kate Cushing professor i terapeutisk radiologi og professor i Patologi. "Dette har virkelig åbnet op for en helt ny måde at behandle disse patienter på, selvom der skal gøres meget mere arbejde."
Brugen af nanopartiklerne til at målrette tumorerne gjorde det muligt for forskerne at bruge lægemidlet talazoparib, som har vist sig at være effektivt i en række solide tumorer uden for hjernen. Fordi lægemidlet har begrænset til ingen penetration af centralnervesystemet, ville en oralt indgivet dosis imidlertid have begrænset effekt mod tumorer med leptomeningeal spredning.
"Ved at indkapsle det i en nanopartikel og direkte injicere det i CSF, får vi nu meget høj eksponering på netop det område," sagde Saltzman, Goizueta Foundation professor i biomedicinsk teknik, kemi- og miljøteknik og fysiologi og medlem af Yale. Cancer Center.
Indgivelse af stoffet intratekalt undgår også at injicere det direkte i hjernen, en teknik, der omtales som konvektionsforstærket levering, en meget udfordrende procedure, der kun kan udføres et par gange om året. Intratekale injektioner er derimod meget mindre invasive og kan gives uden hospitalsophold.
"Dette er enormt for os, for nu kan vi udføre flere nanopartikelbehandlinger over tid," sagde Bindra.
Ud over nanopartikelinjektionen fik mus også en oral dosis af et kemoterapilægemiddel kendt som temozolomid.
"Det er en ny platform, hvor vi kan give disse orale kemoterapier, der kommer på tværs af blod-hjerne-barrieren og et målrettet middel kun i centralnervesystemet," sagde Bindra. "I bund og grund vil denne kompartmentalisering af kombinationsterapi øge synergistisk tumorcelledrab og samtidig minimere systemisk toksicitet."
De mus, der modtog den nanopartikelbaserede behandling, levede betydeligt længere end de mus, der modtog lægemiddelbehandling, der ikke brugte nanopartikler, og endda længere end de mus, der ikke modtog nogen behandling. Yderligere var der meget mindre spredning af kræften i de mus, der modtog de lægemiddelbærende nanopartikler.
Forskerne sagde, at de næste skridt vil være at validere tilgangen i større dyremodeller, til sidst efterfulgt af forsøg på mennesker. Holdet planlægger også at teste behandlingsmetoden på andre kræftformer, især dem, der har tendens til at sprede sig til hjernen.
Flere oplysninger: Minsoo Khang et al., Intratekal levering af nanopartikel PARP-hæmmer til cerebrospinalvæsken til behandling af metastatisk medulloblastom, Science Translational Medicine (2023). DOI:10.1126/scitranslmed.adi1617
Journaloplysninger: Videnskab translationel medicin
Leveret af Yale University
 Varme artikler
Varme artikler
-
 Oprustning af maskiner i nanoskalaEt tog af molekylære tandhjul sammensat af stjerneformede molekyler. Kredit:Gwénaël Rapenne (NAIST og UPS) Geartog er blevet brugt i århundreder til at omsætte ændringer i gearets rotationshastigh
Oprustning af maskiner i nanoskalaEt tog af molekylære tandhjul sammensat af stjerneformede molekyler. Kredit:Gwénaël Rapenne (NAIST og UPS) Geartog er blevet brugt i århundreder til at omsætte ændringer i gearets rotationshastigh -
 Nyt system kan påvise kokain i lave koncentrationerUltrasensitiv påvisning af mycoplasma og kokain, UPV forskere, Valencia. Kredit:Asociación RUVID Forskere fra Valencia og Baskerlandet har udviklet en ny metode til at påvise kokain og mycoplasma
Nyt system kan påvise kokain i lave koncentrationerUltrasensitiv påvisning af mycoplasma og kokain, UPV forskere, Valencia. Kredit:Asociación RUVID Forskere fra Valencia og Baskerlandet har udviklet en ny metode til at påvise kokain og mycoplasma -
 Katalysatorer i atomare skala kan producere billig brintNorth Carolina State University forskere fandt MoS2 tynde film er effektive katalysatorer til brintproduktion. Kredit:Linyou Cao Forskere ved North Carolina State University har vist, at en etatom
Katalysatorer i atomare skala kan producere billig brintNorth Carolina State University forskere fandt MoS2 tynde film er effektive katalysatorer til brintproduktion. Kredit:Linyou Cao Forskere ved North Carolina State University har vist, at en etatom -
 Eksperter er forsigtige over Googles nanopartikelprojektEt Google-projekt for at udvikle nanopartikler, der kan opdage kræftceller inde i kroppen, er et nyttigt bidrag, men står over for vigtige forhindringer, siger eksperter Et Google -projekt om at u
Eksperter er forsigtige over Googles nanopartikelprojektEt Google-projekt for at udvikle nanopartikler, der kan opdage kræftceller inde i kroppen, er et nyttigt bidrag, men står over for vigtige forhindringer, siger eksperter Et Google -projekt om at u
- Barrierer der stopper bakterier
- Læger vil muligvis snart kunne se en hjernetumor brændt væk i realtid
- Massive filamenter giver næring til væksten af galakser og supermassive sorte huller
- Green Deal søger at gøre Europa til det første klimaneutrale kontinent i 2050
- Hvordan konverterer jeg ampere til Kw 3-fase?
- En novelle, lavprismetode detekterer forurenende stoffer i nanoskala under fremstilling af halvleder…


