Carbon-indkapslet magnetit nanodonut foreslået til synergistisk cancerterapi
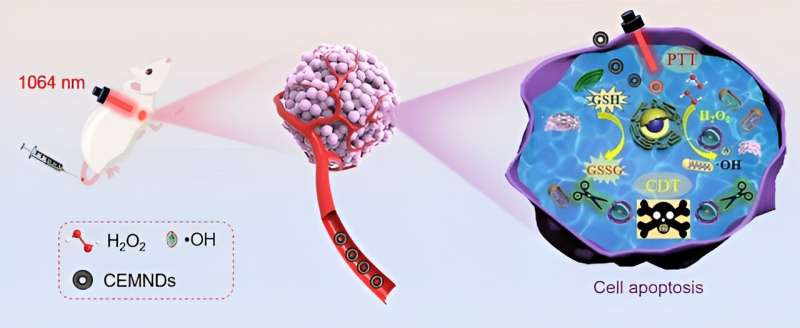
Ved hjælp af Steady-State High Magnetic Field Experimental Facility har forskere ledet af prof. Wang Hui fra Hefei Institutes of Physical Science ved det kinesiske videnskabsakademi i samarbejde med forskere fra University of Washington konstrueret en fotoresponsiv kulstofindkapslet magneto nanodonut (CEMNDs) nanoenzym med dobbelt katalytisk aktivitet til fototermisk forbedret kemodynamisk cancersynergistisk terapi.
Resultaterne blev offentliggjort i Advanced Healthcare Materials .
Jernbaseret nanoenzym-medieret kemodynamisk terapi (CDT) har tiltrukket sig stor opmærksomhed i de senere år for katalytisk tumorterapi. Men tumorcellernes begrænsede optagelse af jernbaserede nanoenzymer og den svage frigivelse af jernioner gør kræftbehandling udfordrende.
Det er effektivt at skabe den kvasi-todimensionelle struktur af det jernbaserede nanoenzym for at øge tumorcelleoptagelsen. Den kvasi-todimensionelle struktur af det jernbaserede nanoenzym fører til et øget specifikt overfladeareal, hvilket muliggør hurtigere jernionfrigivelse og forbedret dannelse af hydroxylradikal (·OH) Fenton-reaktion, og derved optimere tumorterapi.
I denne undersøgelse introducerede forskerne lys-responsive CEMND'er, der udviste dobbelte katalytiske aktiviteter for CDT.
"CEMND'er kan akkumulere inden for tumorsteder og trænge ind i tumorceller, hvor de fungerer som peroxidase-enzymer til at omdanne H2 O2 ind i ·OH," sagde Meng Xiangfu, førsteforfatter af undersøgelsen, "denne katalytiske proces inducerer målrettet tumorcelledød."
Kulstoflaget på CEMND'er konstrueret ved den solvotermiske metode var i stand til at forbedre stabiliteten og biokompatibiliteten af nanoenzymet.
Den todimensionelle konstruktion af CEMND'er forbedrede optagelseshastigheden af CEMNDS i tumorceller, accelererede frigivelsen af jernioner og Fenton-reaktionen i tumormikromiljøet og realiserede CDT's terapeutiske evne. CEMNDs glutathionoxidaseaktivitet fremmede oxidationen af glutathion, beskyttede ·OH dannet af Fenton-reaktionen og forbedrede den terapeutiske effekt af CDT.
Derudover var den optiske absorption af CEMND'er i den anden nær-infrarøde vinduesregion (NIR-II) i stand til effektivt at omdanne lysenergi til varmeenergi, hvilket yderligere realiserede fototermisk forbedret cancerkemodynamisk terapi.
Resultaterne af denne undersøgelse lover at fremme kræftbehandlingsmodaliteter, ifølge forskerne.
Flere oplysninger: Xiangfu Meng et al., Carbon-Encapsulated Magnetite Nanodoughnut som et NIR-II-responsivt nanozyme til synergistisk kemodynamisk-fototermisk terapi, Avancerede sundhedsmaterialer (2023). DOI:10.1002/adhm.202301926
Journaloplysninger: Avanceret sundhedsplejemateriale
Leveret af Chinese Academy of Sciences
 Varme artikler
Varme artikler
-
 Siliciumchip med integreret laser:Lys fra en nanotrådBenedikt Mayer og Lisa Janker er på den molekylære stråleepitaxi-facilitet på Walter Schottky Institute, Münchens tekniske universitet. Kredit:Uli Benz / TUM Fysikere ved det tekniske universitet
Siliciumchip med integreret laser:Lys fra en nanotrådBenedikt Mayer og Lisa Janker er på den molekylære stråleepitaxi-facilitet på Walter Schottky Institute, Münchens tekniske universitet. Kredit:Uli Benz / TUM Fysikere ved det tekniske universitet -
 Forskeres smartphonemikroskop kan opdage en enkelt virus, nanopartikler(Phys.org) – Din smartphone kan nu se, hvad det blotte øje ikke kan:En enkelt virus og stykker materiale mindre end en tusindedel af bredden af et menneskehår. Aydogan Ozcan, en professor i elektro
Forskeres smartphonemikroskop kan opdage en enkelt virus, nanopartikler(Phys.org) – Din smartphone kan nu se, hvad det blotte øje ikke kan:En enkelt virus og stykker materiale mindre end en tusindedel af bredden af et menneskehår. Aydogan Ozcan, en professor i elektro -
 Magnetisk kontrollerede nanopartikler forbedrer slagtilfældebehandlingYiping Zhao er professor i fysik ved UGAs Franklin College of Arts and Sciences. (Phys.org) – Forskere ved University of Georgia og deres samarbejdspartnere har udviklet en ny teknik til at forbed
Magnetisk kontrollerede nanopartikler forbedrer slagtilfældebehandlingYiping Zhao er professor i fysik ved UGAs Franklin College of Arts and Sciences. (Phys.org) – Forskere ved University of Georgia og deres samarbejdspartnere har udviklet en ny teknik til at forbed -
 Ingeniører producerer den mindste 3D-transistor endnuVed at bruge en ny fremstillingsteknik, MIT forskere fremstillede en 3-D transistor mindre end halvdelen af bredden af nutidens slankeste kommercielle modeller, som kunne hjælpe med at proppe lang
Ingeniører producerer den mindste 3D-transistor endnuVed at bruge en ny fremstillingsteknik, MIT forskere fremstillede en 3-D transistor mindre end halvdelen af bredden af nutidens slankeste kommercielle modeller, som kunne hjælpe med at proppe lang
- Siliciumoxidkredsløb bryder barriere:Nanokrystalledere kan føre til massiv, robust 3-D opbevaring
- Surrey NanoSystems har super sort materiale
- Retten til at afbryde forbindelsen kommer Australien – hvad betyder det for dig?
- Stigende CO2 på grund af klimaændringer forbedrer muligvis ikke landbruget, model viser
- Hvordan kvanteprikker kan tale med hinanden
- De mange versioner af en kvindelig videnskabsmand


