Tidligere teori om, hvordan elektroner bevæger sig inden for proteinnanokrystaller, gælder muligvis ikke i alle tilfælde
Undersøgelsen, offentliggjort i tidsskriftet Nature Communications, fokuserede på elektronoverførselsegenskaberne af en specifik type protein nanokrystal kendt som cytochrom c-oxidase. Dette proteinkompleks spiller en afgørende rolle i cellulær respiration, den proces, hvorved celler genererer energi.
Ifølge den fremherskende teori bevæger elektroner sig inden for proteinnanokrystaller gennem en proces kaldet hopping. I hop hopper elektroner fra et proteinmolekyle til et andet og passerer gennem den proteinmatrix, der omgiver dem. Denne bevægelse lettes af det specifikke arrangement af aminosyrer i proteinstrukturen, som skaber energitilstande, der muliggør effektiv elektronoverførsel.
Den nye undersøgelse indikerer dog, at hop muligvis ikke er den eneste mekanisme til elektronoverførsel i proteinnanokrystaller. Ved at bruge avancerede spektroskopiteknikker observerede forskerne, at elektroner i cytochrom c-oxidase bevæger sig på en mere kontinuerlig måde i stedet for diskrete humle. Denne kontinuerlige bevægelse antyder, at elektronerne kan blive delokaliseret, hvilket betyder, at de ikke forbliver begrænset til et enkelt molekyle, men spredt ud over et større område af proteinet.
Denne opdagelse udfordrer den eksisterende forståelse af elektronoverførsel inden for proteinnanokrystaller og rejser spørgsmål om universaliteten af hoppemekanismen. Forskerne foreslår, at den kontinuerlige bevægelse af elektroner i cytochrom c-oxidase kan lettes af proteinkompleksets unikke strukturelle egenskaber, såsom tilstedeværelsen af metalioner og cofaktorer, der forbedrer elektroniske interaktioner.
Resultaterne af undersøgelsen har betydelige implikationer for forståelsen af, hvordan proteiner fungerer på molekylært niveau og kan være med til at danne grundlag for design af bio-inspirerede materialer til elektroniske applikationer. Yderligere forskning er nødvendig for at belyse mekanismerne for elektronoverførsel i forskellige proteinnanokrystaller og bestemme de faktorer, der styrer deres adfærd.
 Varme artikler
Varme artikler
-
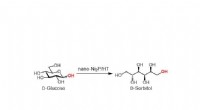 Nikkelphosphid nanopartikelkatalysator er den fulde pakkeFigur 1. Hydrogenering af D-glucose til D-sorbitol. Kredit:Osaka University De fleste katalysatorer, der fremmer omdannelsen af glucose til sorbitol, tilbyder visse egenskaber, mens de kræver ko
Nikkelphosphid nanopartikelkatalysator er den fulde pakkeFigur 1. Hydrogenering af D-glucose til D-sorbitol. Kredit:Osaka University De fleste katalysatorer, der fremmer omdannelsen af glucose til sorbitol, tilbyder visse egenskaber, mens de kræver ko -
 Graphene og atomkrystallerne, der kunne se det næste store gennembrud inden for teknologiGraphene. Kredit:Olive Tree Hvad kunne vi gøre med lagdelte strukturer med de helt rigtige lag? Hvad ville materialernes egenskaber være, hvis vi virkelig kunne arrangere atomerne, som vi vil have
Graphene og atomkrystallerne, der kunne se det næste store gennembrud inden for teknologiGraphene. Kredit:Olive Tree Hvad kunne vi gøre med lagdelte strukturer med de helt rigtige lag? Hvad ville materialernes egenskaber være, hvis vi virkelig kunne arrangere atomerne, som vi vil have -
 På vej mod at erstatte silicium med grafenGrafene består af et enkelt lag af carbonatomer. Kredit:Wikimedia Commons Norske forskere er de første i verden til at udvikle en metode til fremstilling af halvledere af grafen. Denne opdagelse k
På vej mod at erstatte silicium med grafenGrafene består af et enkelt lag af carbonatomer. Kredit:Wikimedia Commons Norske forskere er de første i verden til at udvikle en metode til fremstilling af halvledere af grafen. Denne opdagelse k -
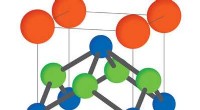 Scanning tunneling mikroskopi afslører oprindelsen af stabile skyrmion gitreFigur 1:Krystalstrukturen af gadolinium ruthenium silicid, som kan være vært for et kvadratisk gitter af hvirvlende magnetiske skyrmioner (orange =gadolinium; grøn =ruthenium; blå =silicium). Kredit
Scanning tunneling mikroskopi afslører oprindelsen af stabile skyrmion gitreFigur 1:Krystalstrukturen af gadolinium ruthenium silicid, som kan være vært for et kvadratisk gitter af hvirvlende magnetiske skyrmioner (orange =gadolinium; grøn =ruthenium; blå =silicium). Kredit
- Påvisning af dødelige sygdomme med rust og sand
- Bjerge, der signalerer forsvinden af gletsjer-fodrede floder
- Kvanteprikker oplyser transport inde i cellen
- Opdrætsresistente kyllinger for forbedret fødevaresikkerhed
- Tests viser, at integrerede kvantechipoperationer er mulige
- Små virksomheder sårbare over for cyberangreb, så lad være med at handle


