Forskere identificerer post-translationel dannelse af anstrengte cyclofaner i bakterier
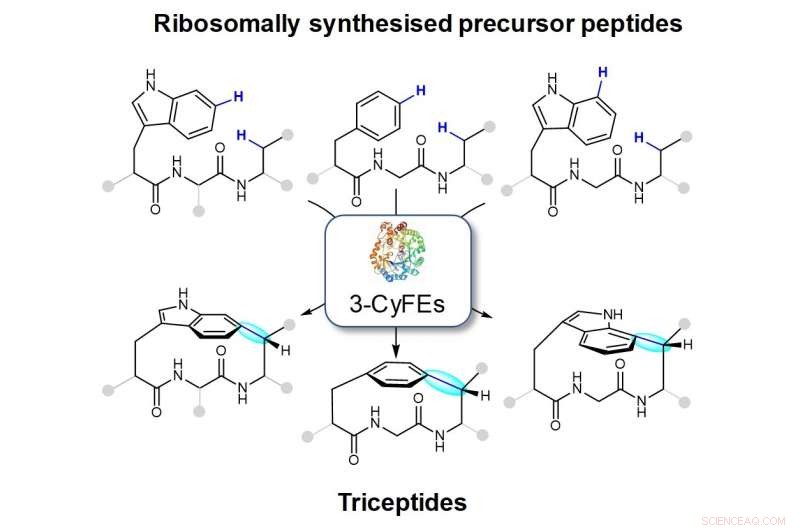
Figur viser makrocykler, der er skabt af de tre-rester cyclofandannende enzymer (3-CyFE'er). Den nye binding er vist i blåt og fremhævet i cyan. Familien af naturlige produkter, der produceres af 3-CyFE'er, kaldes triceptider.
NUS-forskere har identificeret post-translationelle modificerende enzymer i bakterier, der kan skabe en ny familie af cykliske peptider til nye terapeutiske midler.
Cykliske peptider er en velkendt klasse af molekyler, der besidder en række biologiske aktiviteter, herunder antibakterielle, immunosuppressive og kræftbekæmpende egenskaber. Udfordringen ved at skabe nye typer af cykliske peptider ligger i opdagelsen af nye katalytiske reaktioner ved kemisk syntese eller ved brug af enzymer. En strategi til at opnå dette involverer dannelse af carbon-carbon (C-C) bindinger. Imidlertid, C-C-bindingsdannende reaktioner ved ikke-aktiverede carbon-hydrogen (C-H) bindinger er vanskelige, fordi disse positioner er inerte, og selektiviteten er ikke let at kontrollere. At overvinde disse barrierer vil tillade skabelsen af en ny række cykliske peptider på en effektiv og forudsigelig måde.
Forskerteamet ledet af professor Brandon Morinaka fra Farmaceutisk Institut, NUS har fundet reaktioner katalyseret af en række post-translationelle modificerende enzymer fra forskellige bakterier, som potentielt kan bruges til at udvikle vigtige lægemiddelmolekyler. Disse enzymer kan katalysere dannelsen af en C(aryl)-C( sp 3 ) binding mellem sidekæderne af to aminosyrer. Dette molekylære arrangement er det definerende træk for en klasse af naturlige produkter kaldet triceptider (tre rester i cyclofanpeptider) (se figur). Den ringlukkende reaktion resulterer i dannelsen af anstrengte peptidcyclophaner. Selvom disse enzymer er kodet i flere hundrede bakterielle genomer, deres funktion og deres slutprodukter er stort set ukendt.
Disse enzymer tilbyder en ny strategi til modifikation af peptider og kan anvendes til at generere terapeutiske peptider, der viser unik binding til molekylære mål. Cykliseringen af peptider er en generel strategi, der anvendes i naturen og syntetisk kemi for at forhindre nedbrydning af fordøjelsesenzymer. Forebyggelse af nedbrydning er en væsentlig egenskab, der er nødvendig for, at lægemidler kan nå deres mål og repræsenterer en hindring for at bruge peptider som lægemidler.
Disse enzymer er i stand til at installere ringene i en række forskellige mønstre med forskellige aminosyrer. Dette betyder, at bredden af produkter er potentielt stor og kan anvendes til forskellige mål i lægemiddelforskning. Forskellige bakterier fra en række mikrobiomer viste sig at kode for de cyclofandannende enzymer. Mangfoldigheden af produkter antyder, at peptidcyklofaner er mere udbredt end tidligere kendt og kan give en generel anvendelse eller funktion blandt denne klasse af naturlige produkter.
Holdet planlægger at producere yderligere triceptide naturlige produkter og at forstå enzymmekanismen. Deres langsigtede mål er at generere et mangfoldigt udvalg af peptidcyklofanprodukter, som kan bruges som udgangspunkt for at målrette sygdomme af interesse.
Prof Morinaka sagde, "Post-translationelle cyclophan-dannende enzymer tilbyder en ny metode til at skabe forskellige cykliske peptider, der giver nye muligheder inden for peptidteknik og opdagelse af lægemidler."
 Varme artikler
Varme artikler
-
 Højtydende selvsamlet katalysator til SOFCProcessen med legeringsopløsning. Kredit:UNIST En nylig undersøgelse tilknyttet UNIST har introduceret en ny katalysator, der markant kan forbedre ydeevnen af perovskitelektroder i Solid Oxide F
Højtydende selvsamlet katalysator til SOFCProcessen med legeringsopløsning. Kredit:UNIST En nylig undersøgelse tilknyttet UNIST har introduceret en ny katalysator, der markant kan forbedre ydeevnen af perovskitelektroder i Solid Oxide F -
 Elektronkrystallografi viste sig at virke lige så godt som røntgenkrystallografi kun på mindre kr…Identifikation af forbindelser fra heterogene blandinger. EM-gitter forberedt som ovenfor med biotin, brucine, carbamazepin, og cinchoninpulver blandet sammen. Alle fire forbindelser identificeret ved
Elektronkrystallografi viste sig at virke lige så godt som røntgenkrystallografi kun på mindre kr…Identifikation af forbindelser fra heterogene blandinger. EM-gitter forberedt som ovenfor med biotin, brucine, carbamazepin, og cinchoninpulver blandet sammen. Alle fire forbindelser identificeret ved -
 Ekstrem biomimetik - søgen efter naturlige kilder til materialeteknisk inspirationOversigt over transformationen af svampestilladser til en karboniseret 3D -struktur ved 1200 ° C. (A) Typisk cellulær og hierarkisk morfologi af Hippospongia communis demosponge organisk skelet efte
Ekstrem biomimetik - søgen efter naturlige kilder til materialeteknisk inspirationOversigt over transformationen af svampestilladser til en karboniseret 3D -struktur ved 1200 ° C. (A) Typisk cellulær og hierarkisk morfologi af Hippospongia communis demosponge organisk skelet efte -
 Bare tilsæt vand - Kemikere afslører en mekanisme bag doping af organiske halvledereDenne Lewis-syre ændrer de elektriske egenskaber af visse organiske halvledere, når den tilsættes i tilstedeværelsen af vand Kredit: Brett Yurash Halvledere – og vores beherskelse af dem – har g
Bare tilsæt vand - Kemikere afslører en mekanisme bag doping af organiske halvledereDenne Lewis-syre ændrer de elektriske egenskaber af visse organiske halvledere, når den tilsættes i tilstedeværelsen af vand Kredit: Brett Yurash Halvledere – og vores beherskelse af dem – har g


