Hvad er et atom, elektron, neutron og proton?
Atom
Atomer er ekstremt små partikler og kan ikke fordeles yderligere undtagen ved ekstraordinære midler. Tænk på de stykker, der udgør et puslespil. Disse kan teknisk skilles i mindre stykker pap og papir ved at ødelægge dem, men i praktiske øjemed er disse stykker de grundlæggende, udelelige elementer i puslespil.
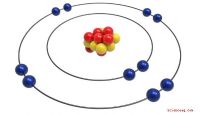
Atomer består af protoner, der bærer en positiv elektrisk ladning ; elektroner, som bærer en negativ ladning og neutroner, der bærer ingen omkostninger. I et almindeligt, elektrisk neutralt atom er antallet af protoner og antallet af elektroner ens.
Atomerets atommasse er omtrent lig med antallet af protoner plus antallet af elektroner, da massen af elektroner er praktisk talt ubetydelig.
Proton
Protonen er i virkeligheden indekspartiklen af ethvert atom. Det er antallet af protoner i et atom, der bestemmer elementets identitet, som et atom tilhører; med andre ord, hvis to atomer har et forskelligt antal protoner, er de ikke det samme element.
Antallet af protoner i et element bestemmer dets atomnummer, Z. Brint er det letteste element og har en proton (Z = 1); uran er det tungeste naturligt forekommende element og har 92 protoner (Z = 92). Hver proton, der tildeles en masse på 1,00728 atommasseenheder (amu), har en ladning betegnet som +1.
Atomer kan eksistere med kun en proton i deres kerne, som det er tilfældet med hydrogenatomer. En kerne uden mindst en ledsagende proton er imidlertid ikke et atom.
Neutronen
Neutroner er ens i størrelse til protoner, med en amu på 1.00867 og beboer også kernen i atomer. Antallet af neutroner i et atom i et elements mest stabile konfiguration er sædvanligvis større end antallet af protoner, idet denne forskel bliver større, idet atomnummeret stiger. Et hydrogenatom har for eksempel en proton men ingen neutroner, mens et heliumatom har to af hver. Tin har på den anden side 50 protoner og 69 neutroner, mens uran har henholdsvis 92 og 146.
Antallet af protoner plus neutroner i et atom er dets massetal, M. Således er antallet af neutroner i et atom er dets atommasse tal minus dets atomnummer eller M - Z.
Hvis et atom vinder eller taber neutroner, forbliver det det samme element, men bliver en isotop af det element. Forskellige isotoper identificeres ved at tilføje M til øverste venstre hjørne af forkortelsen for det pågældende element. For eksempel er 14C en isotop af kulstof (Z = 6), der har otte neutroner snarere end de sædvanlige seks. Elektronen Elektroner er små (0,000549 amu), negativt ladede partikler, der beskrives som omkreds til protonerne og neutronerne, der udgør et atoms kerne, som planeter omkranser solen. Dette er imidlertid en grov beskrivelse i bedste fald, da fremskridt inden for kvantfysik har ført til begrebet diskrete orbitaler om kernen mellem hvilke elektroner kan "hoppe". Disse orbitaler svarer til forskellige elektromagnetiske energiniveauer og er givet navne som s, p, d og f. Bevægelsen af elektroner stammer fra deres belastning på -1 og tiltrækkes af den positivt ladede kerne. Normalt er antallet af elektroner i et atom lig med Z, hvilket gør disse atomer neutrale i total ladning. Nogle atomer har forskellige protoner og elektroner, hvilket resulterer i en netto positiv eller negativ ladning. Disse atomer kaldes ioner.
Sidste artikelHvad er oxidanter?
Næste artikelHvad er Nadph i fotosyntese?
 Varme artikler
Varme artikler
-
 Sådan bygger du en container, hvor is ikke smelter i 4 timerIs kan være vigtig for at nyde en varm sommerdag, lang tur eller udendørs fest. Hvis du skal holde din is fast og ikke har en køler, kan du lave din egen ved hjælp af en papkasse ved hjælp af aluminiu
Sådan bygger du en container, hvor is ikke smelter i 4 timerIs kan være vigtig for at nyde en varm sommerdag, lang tur eller udendørs fest. Hvis du skal holde din is fast og ikke har en køler, kan du lave din egen ved hjælp af en papkasse ved hjælp af aluminiu -
 3D Atom Model Crafts for KidsAt lave et tredimensionelt atom kan være et interessant og uddannelsesmæssigt projekt for et barn. En 3D-atommodel giver ham en bedre ide om, hvilke atomer der ligner, og hvordan de virker. For en eks
3D Atom Model Crafts for KidsAt lave et tredimensionelt atom kan være et interessant og uddannelsesmæssigt projekt for et barn. En 3D-atommodel giver ham en bedre ide om, hvilke atomer der ligner, og hvordan de virker. For en eks -
 Field Trip-ideer til High School ChemistryFeltrejser er en fremragende måde at understrege lektioner og hjælpe eleverne med at forstå, at det, de lærer i klasseværelset, kan anvendes til det virkelige liv. Når man udvikler feltrejser for kemi
Field Trip-ideer til High School ChemistryFeltrejser er en fremragende måde at understrege lektioner og hjælpe eleverne med at forstå, at det, de lærer i klasseværelset, kan anvendes til det virkelige liv. Når man udvikler feltrejser for kemi -
 Hvad påvirker den atomiske radius?Et atoms radius er afstanden fra midten af dets kerne til dets yderste elektroner. Størrelsen på atomerne i de forskellige elementer - f.eks. Brint, aluminium og guld - ændres afhængigt af større
Hvad påvirker den atomiske radius?Et atoms radius er afstanden fra midten af dets kerne til dets yderste elektroner. Størrelsen på atomerne i de forskellige elementer - f.eks. Brint, aluminium og guld - ændres afhængigt af større


