Den skjulte struktur af det periodiske system
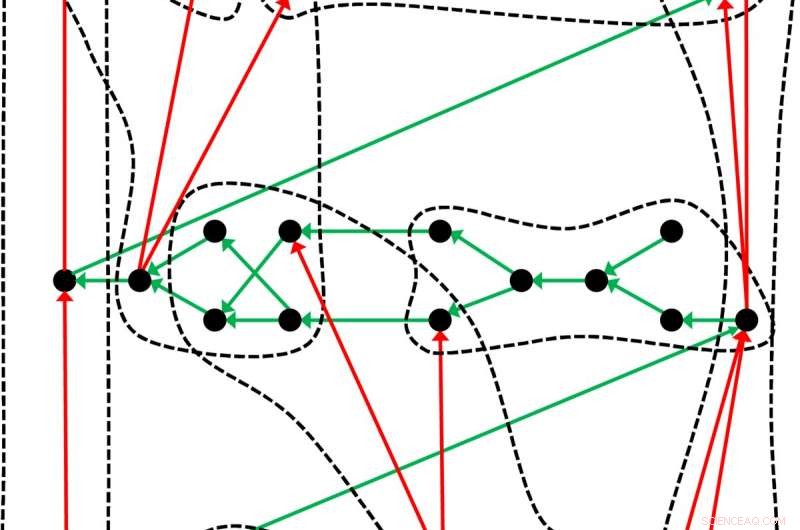
Et lidt anderledes periodisk system:Tabellen over kemiske grundstoffer, som går tilbage til Dmitri Mendeleev og Lothar Meyer, er blot et eksempel på, hvordan objekter – i dette tilfælde de kemiske grundstoffer – kan organiseres i et sådant system. Forskerne fra Leipzig illustrerer den generelle opbygning af et periodisk system med dette eksempel:De sorte prikker repræsenterer objekterne sorteret efter de grønne pile. Ved at bruge et passende kriterium, objekterne kan klassificeres i grupper (stiplede linjer), hvor de røde pile danner en underrækkefølge. Kredit:Guillermo Restrepo, MPI for Matematik i Naturvidenskaberne
Det periodiske system af grundstoffer, som de fleste kemibøger skildrer, er kun ét særligt tilfælde. Denne tabeloversigt over de kemiske grundstoffer, som går tilbage til Dmitri Mendeleev og Lothar Meyer og andre kemikeres tilgange til at organisere grundstofferne, involverer forskellige former for repræsentation af en skjult struktur af de kemiske grundstoffer. Dette er konklusionen af forskere ved Max Planck Institut for Matematik i Videnskaberne i Leipzig og Universitetet i Leipzig i et nyligt papir. Leipzig-forskernes matematiske tilgang er meget generel og kan give mange forskellige periodiske systemer afhængigt af ordens- og klassifikationsprincippet – ikke kun for kemi, men også for mange andre vidensområder.
Det er et ikon for naturvidenskab og hænger i de fleste kemi klasseværelser:det periodiske system af grundstoffer, som i år fejrer 150 års fødselsdag. Den tabelformede oversigt er tæt knyttet til Dmitri Mendeleev og Lothar Meyer - to forskere, der, i 1860'erne, skabt et arrangement af grundstoffer baseret på deres atommasse og ligheder. I dag er de sorteret efter atomnummer (som angiver antallet af protoner i atomkernen) fra den lette brint (en proton) til den syntetiske oganesson (118 protoner). Grundstofferne er også klassificeret i grupper:Atomer i samme søjle har normalt det samme antal elektroner i deres ydre skal.
Periodisk system i forskellige varianter
Ved første øjekast, det periodiske system synes at have bragt en utvetydig og endelig rækkefølge til de i øjeblikket kendte 118 grundstoffer. Men udseendet kan være vildledende, fordi mange ting stadig er kontroversielle:Forskere er ikke enige om, præcis hvilke grundstoffer der hører til i den tredje gruppe under skandium og yttrium. For eksempel, den korrekte position af lanthan og aktinium diskuteres. Hvis man ser nærmere, man vil opdage lidt forskellige varianter af det periodiske system i klasseværelserne, foredragssale, og lærebøger.
Guillermo Restrepo og Wilmer Leal fra Max Planck Institute for Mathematics in the Sciences og University of Leipzig er ikke overraskede. For dem, der er ingen entydigt korrekt arrangement af elementerne; afhængigt af det anvendte kriterium for klassificering, et andet periodisk system resultater. Atomerne kan underinddeles i henhold til elektronkonfigurationen (dvs. antallet og arrangementet af deres elektroner), deres kemiske adfærd, deres opløselighed, eller deres forekomst i geologiske aflejringer. Det er nu almindeligt accepteret, at de kemiske grundstoffer skal arrangeres efter deres atomnummer og opdeles i grupper efter deres elektronkonfiguration. Men selv for dette periodiske system, der er mange forskellige former for repræsentation. For eksempel:som en spiral med forskellige buler, pyramideformet, eller som en tredimensionel blomst.
En fælles struktur bag de periodiske systemer
Guillermo Restrepo og Wilmer Leal har nu systematisk undersøgt det periodiske systems flertydighed. Dette har ført til fund, som også er af betydelig betydning ud over kemi. Derfor, alle former for repræsentation af de kemiske grundstoffer er baseret på en fælles struktur, som matematikere omtaler som en ordnet hypergraf. Det ærværdige periodiske system af Mendeleev og Meyer giver således kun en repræsentation af den generelle struktur, som Guillermo Restrepo og Wilmer Leal nu postulerer. Nye arrangementer kan også til enhver tid udledes heraf. Guillermo Restrepo sammenligner derfor rækkefølgen af de kemiske grundstoffer med en skulptur, hvorpå lyset falder fra forskellige retninger. "De forskellige skygger, som figuren kaster, er de periodiske tabeller. Det er derfor, der er så mange måder at skabe disse tabeller på. På en måde, periodetabellerne er fremskrivninger. Fremskrivninger af den interne struktur i det periodiske system."
Forskerne fra Leipzig forsøger nu at bestemme den skjulte matematiske struktur, som de kendte periodiske skemaer for kemi er baseret på. Indtil videre, de har defineret tre betingelser, der skal være opfyldt for at etablere et periodisk system. Først, man har brug for genstande, der skal bestilles. For Mendeleev, Meyer og skaberne af de andre kendte periodiske skemaer for kemi, disse er de kemiske grundstoffer. These objects must be arranged according to some properties such as the atomic mass or the atomic number (i.e. the number of protons). Endelig, one criterion is required to group the objects in classes. Mendeleev and Meyer used the chemical similarity for this.

A periodic table of chemical bonds:Each of the 94 circles with chemical element symbols represents the bond that the respective element forms with an organic residue. The bonds are ordered according to how strongly they are polarized. Where there is a direct arrow connection, the order is clear:Bonds of hydrogen, for eksempel, are more polarized than bonds of boron, fosfor, and palladium. The same applies to rubidium in comparison to caesium, which has particularly low polarized bonds and is therefore at the bottom of the new periodic table. If there is no direct arrow between two elements, they may still be comparable – if there is a chain of arrows between them. For eksempel, the bonds of oxygen are more polarized than the bonds of bromine. Bonds represented by the same colour have the same binding behaviour and belong to one of the 44 classes. Credit:Guillermo Restrepo, MPI for Mathematics in the Sciences
Periodic table of chemical bonds
"If these three conditions are met, periodic tables can also be created for other chemical objects and even for objects outside chemistry, " says Guillermo Restrepo. He and Wilmer Leal show this by looking at the chemical bonds between atoms of 94 elements and different conjugates. The polarizability of 94 single-covalent bonds, where bonds are arranged according to the electronegativity and atomic radius of one of the bonded atoms. For eksempel, fluorine, chlorine, or oxygen are highly electronegative and assume relatively small atomic radii in compounds. The bonds are then classified based on how much they resemble each other.
"We have investigated almost 5, 000 substances consisting of two elements in different proportions, " explains Guillermo Restrepo. "We then looked for similarities within this data. For eksempel, sodium and lithium are similar because they combine with the same elements in the same proportions (e.g. with oxygen or chlorine, bromine, and iodine). We thus found patterns we can use to classify the elements."
A periodic table as a network instead of a matrix
In the 44 classes of chemical elements, there are some similarities with the main groups of Mendeleev's and Meyer's periodic table. For eksempel, the alkali metals sodium and lithium are found in one group because they form the same simple salts with halogens such as chlorine or fluorine. Like the elements themselves, the bonds of the four halogens (fluorine, chlorine bromine, and iodine) are also found in the same group. Imidlertid, there are also classifications that differ significantly from those in the conventional periodic table. For eksempel, carbon and silicon are no longer in the same class because they form very different compounds.
The representation of the periodic table of chemical bonds also has nothing to do with the familiar matrix-like arrangement of the classical periodic tables of the elements. I stedet, the 94 covalent bonds are represented in a network of differently colored circles. Each circle represents a chemical bond, and the colou symbolizes belonging to one of the 44 groups. Because now two criteria are used for the sorting, there is no longer any clear order of the atoms (like in the tables of Mendeleev and Meyer)—mathematicians speak of a partial order. The circles are therefore connected to other circles by one or more arrows, thereby creating an ordered hypergraph.
Periodic tables in other scientific fields
The chemical elements and their compounds can also be represented in completely different periodic tables—depending on the underlying order and classification principle. What's more:The objects of numerous other scientific fields and their applications can also be arranged in periodic tables. For eksempel, ordered hypergraphs are used in information systems and web mining. Possible periodic systems also emerge when countries are considered; these can be classified according to social or economic indicators as well as geographical proximity or cultural similarity. Other examples can be found in engineering, environmental sciences, sociologi, and many other disciplines. The scientists not only study periodic systems because of their importance for chemistry, men, først og fremmest, because of their applications in many other disciplines.
 Varme artikler
Varme artikler
-
 Krig mod stoffer forårsager aggressiv politiarbejde, siger ekspertKredit:123rf.com/Rice University Krigen mod stoffer har givet politiet dækning for aggressive taktikker og unødvendige møder med borgere, ifølge Katharine Neill Harris, Alfred C. Glassell, III, Fe
Krig mod stoffer forårsager aggressiv politiarbejde, siger ekspertKredit:123rf.com/Rice University Krigen mod stoffer har givet politiet dækning for aggressive taktikker og unødvendige møder med borgere, ifølge Katharine Neill Harris, Alfred C. Glassell, III, Fe -
 Gamle egyptere samlede fugle fra naturen til ofring og mumificeringScene fra Books of the Dead (Det egyptiske museum), der viser den ibis-hovedet gud Thoth, der optager resultatet af den endelige dom. Kredit:Wasef et al. 2019 I det gamle Egypten, Hellige ibiser b
Gamle egyptere samlede fugle fra naturen til ofring og mumificeringScene fra Books of the Dead (Det egyptiske museum), der viser den ibis-hovedet gud Thoth, der optager resultatet af den endelige dom. Kredit:Wasef et al. 2019 I det gamle Egypten, Hellige ibiser b -
 Albinisme i Tanzania:Hvad kan man gøre for at bryde stigmatiseringenKredit:Unsplash/CC0 Public Domain Det lette fysiske udseende af mennesker med albinisme er forårsaget af en arvelig tilstand, som resulterer i mangel på melanin. Det betyder, at folk med albinisme
Albinisme i Tanzania:Hvad kan man gøre for at bryde stigmatiseringenKredit:Unsplash/CC0 Public Domain Det lette fysiske udseende af mennesker med albinisme er forårsaget af en arvelig tilstand, som resulterer i mangel på melanin. Det betyder, at folk med albinisme -
 Hvordan erhvervskompetencer påvirker migrationKredit:Pixabay Hvilke egenskaber kendetegner mennesker, der migrerer til et andet land for en bedre indkomst fra andre i deres hjemland? Det faktum, at formel uddannelse alene ikke er nok til at b
Hvordan erhvervskompetencer påvirker migrationKredit:Pixabay Hvilke egenskaber kendetegner mennesker, der migrerer til et andet land for en bedre indkomst fra andre i deres hjemland? Det faktum, at formel uddannelse alene ikke er nok til at b
- Power Walk på denne måde:Forskere udvikler enheder, der udnytter energi fra hverdagens bevægelser
- 3 måder at hjælpe seksualforbrydere med at genintegrere sikkert tilbage i samfundet
- Bobcat 743 Specifikationer
- Forskere udvikler ErSb nanostrukturer med applikationer i infrarøde og terahertz-områder
- Ion qubits giver et tidligt glimt af detektering af kvantefejl
- Forskere samler et bibliotek af sukkerarter


