Forskere opretter en enhed til ultra-præcis genom-sekventering af enkelte humane celler
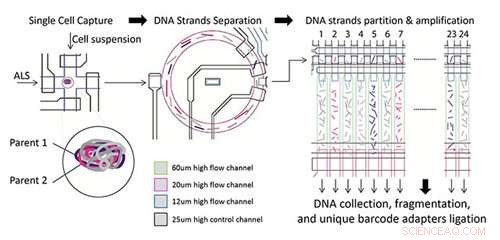
Oversigt over eksperimentel proces ved hjælp af SISSOR -teknologi. En enkelt celle i suspension identificeret ved billeddannelse og fanget, derefter separeres kromosomale DNA-molekyler i enkeltstrenget form, som derefter fordeles tilfældigt og opdeles i 24 MDA-kamre og skubbes ind i luftfyldt kammer og reaktionsopløsning. MDA -reaktion opstår efter, at der er påført varme på enheden ved 30 grader C natten over, før indsamling og behandling til stregkodet sekvensbibliotek. Kredit:University of California - San Diego
Et tværfagligt team af forskere ved University of California San Diego har udviklet en teknologi til meget præcis sekventering og haplotyping af genomer fra enkelte humane celler. Deres resultater blev offentliggjort online forud for Procedurer fra National Academy of Sciences ( PNAS ) trykt udgave.
"Nøjagtig sekventering af enkeltceller gør det muligt at identificere mutationer, der forårsager kræft og genetisk sygdom, "sagde seniorforfatter Kun Zhang, professor i bioingeniør ved UC San Diego Jacobs School of Engineering. "På samme tid, præcis haplotyping giver mulighed for genotyping af haplotyper, kombinationer af forskellige gener eller alleler som en gruppe fra begge forældre. "
Zhangs medforfattere fra Institut for Bioingeniør omfatter professor Xiaohua Huang og postdoktoralforsker og alumnus Wai Keung Chu (MS, Ph.d. '11, '16), hvem er første forfatter til PNAS -artiklen. Samarbejdspartnere om forskningen fra Institut for Computer Science and Engineering (CSE) omfatter professor Vineet Bafna, der er ekspert i bioinformatik i Center for Microbiome Innovation og CHO Systems Biology Center, begge ved UC San Diego, Ph.d. studerende Peter Edge, og CSE -alumnus Vikas Bansal (Ph.D. '08), nu en fakultet-tilknyttet CSE og professor i pædiatri ved UC San Diego School of Medicine. Tilføjelse til projektets tværfaglige rødder er Department of Electrical and Computer Engineering (ECE) alumnus Ho Suk Lee (MS, Ph.d. '11, '15), nu hos Broadcom, som lånte sin ekspertise inden for mikrofluidiske enheder til encellede analyser samt mange års arbejde i bioingeniørlaboratorierne hos både professorer Zhang og Huang.
Kliniske anvendelser af genom -sekventering kræver høj nøjagtighed i DNA -sekventering. Ifølge CSE's Bafna, indtil nu, mange applikationer var off-limits, fordi de nuværende teknologier ikke var præcise nok til at kunne udføres på niveau med den enkelte menneskelige celle.
"Mange individer bærer alleler, der forårsager genetisk sygdom eller disponerer dem for kræft, "sagde Bafna." Hvert gen har to alleler, en fra hver forælder. En af allelerne kan indeholde sygdomsfremkaldende mutationer. Bærerne kan være asymptomatiske, men deres afkom kan vise symptomer på grund af kombinationen af dårlige alleler eller haplotyper fra begge forældre. "
Tag tilfælde af par, der håber at blive gravid via in vitro-befrugtning (IVF). "For genetisk diagnostik før IVF -implantation, et menneskeliv er involveret, så den største nøjagtighed er påkrævet, "forklarede bioingeniørprofessor Xiaohua Huang." Med vores teknologi, vi kan lave meget præcis sekventering og haplotyping af genomet baseret på en enkelt celle biopsieret fra tidlige embryoner. "
Ud over IVF præimplantationsdiagnostik og tidlig kræftdetektion, andre potentielle anvendelser af UC San Diego-udviklet teknologi inkluderer højkvalitets kontrol af genomredigerede humane celler til terapeutiske formål. "Med eksplosionen i brugen af CRISPR/Cas9 og andre målrettede genomredigeringsteknikker, nye behandlinger kunne være justerede versioner af patientens egne celler, "sagde første forfatter og bioingeniør Ph.D. -studerende Wai Keung Chu." Teknologien gør det muligt at bruge en enkelt celle i det 'redigerede' gen og returnere resultater, der ville være lige præcise, som hvis vi sekventerede mange celler. "
Den pågældende teknologi har to nye aspekter:en mikrofluid processor, der muliggør manipulation af enkelte celler og separate kromosomstrenge i forskellige kamre; og beregningsmetoder, der udnytter strenginformationen til haplotyping og fejlkorrektion. UC San Diego-forskerne har kaldt det "Single-Stranded Sequencing using micrOfluidic Reactors" (SISSOR).
"I det væsentlige muliggør den samtidig sekventering af meget lange fragmenter af alle fire tråde i det kromosomale DNA fra begge forældre, "forklarede CSE bioinformatik ph.d. -studerende Peter Edge, der arbejder i pædiatri professor Vikas Bansal's Genome Information Science lab. "Dette giver os mulighed for at foretage sammenligninger og rette for fejl."
SISSOR -teknikken bryder også det, der er blevet kaldt 'forbandelsen af polymeraser', som indfører fejl ved kopiering af DNA. Desværre, bemærkede CSE's Bafna, "vi kan ikke læse genominformation fra enkeltceller uden polymeraser, så vi måtte finde på en løsning, der slipper af med de fejl. "
Baseret på deres fund, PNAS-papirets medforfattere var i stand til at demonstrere "den mest præcise encellede genom-sekvensering til dato."
Seniorforfatter Kun Zhang siger, at forskningssamarbejdets tværfaglige karakter var afgørende for at finde en mere præcis måde at sekvensere DNA fra enkeltceller. "Vores tilgang kan samtidig give større nøjagtighed og længere haplotyper end andre eksisterende tilgange, "konkluderede Zhang." Denne innovation krævede ekspertise, der går ud over, hvad der normalt findes i en enkelt afdeling, og denne sag er et vidnesbyrd om UC San Diego voksende tværfaglige forskningskultur, der gjorde det muligt for os at hente samarbejdspartnere fra andre afdelinger, der var kritiske for en teknologi, hvis udbytte forhåbentlig vil blive målt i redde liv-og måske flere sunde børn født via in vitro befrugtning. "
 Varme artikler
Varme artikler
-
 Statistisk modellering hjælper fiskeriforvaltere med at fjerne invasive arterSouth Dakota Game Fish and Parks biologer Dave Lucchesi og Todd St. Sauver, foran; South Dakota State University kandidatstuderende Matt Hennen, i orange hætte, og besætningsmedlemmer fra Dave Raw Fis
Statistisk modellering hjælper fiskeriforvaltere med at fjerne invasive arterSouth Dakota Game Fish and Parks biologer Dave Lucchesi og Todd St. Sauver, foran; South Dakota State University kandidatstuderende Matt Hennen, i orange hætte, og besætningsmedlemmer fra Dave Raw Fis -
 Hvad er de fem hovedfunktioner i skeletsystemet?Skeletsystemet er opdelt i to dele, det aksiale skelet og appendikulære skelet. Det aksiale skelet omfatter kraniet, rygsøjlen, ribben og brystbenet. Det appendikulære skelet omfatter alle øvre og ned
Hvad er de fem hovedfunktioner i skeletsystemet?Skeletsystemet er opdelt i to dele, det aksiale skelet og appendikulære skelet. Det aksiale skelet omfatter kraniet, rygsøjlen, ribben og brystbenet. Det appendikulære skelet omfatter alle øvre og ned -
 Undersøgelse identificerer sandsynlige scenarier for global spredning af ødelæggende afgrødesygd…Hvede inficeret med stilkrust. Kredit:CIMMYT stilk rust, opkaldt efter de sorte pustler, der inficerer plantestængler, forårsaget ødelæggende afgrødeepidemier og hungersnød i århundreder, før de b
Undersøgelse identificerer sandsynlige scenarier for global spredning af ødelæggende afgrødesygd…Hvede inficeret med stilkrust. Kredit:CIMMYT stilk rust, opkaldt efter de sorte pustler, der inficerer plantestængler, forårsaget ødelæggende afgrødeepidemier og hungersnød i århundreder, før de b -
 Sådan fungerer biomimikMenneskelige forsøg på at skabe effektive flyvende maskiner involverede ofte at studere, hvordan fugle flyver. Fabrice Coffrini/AFP/Getty Images Ubåde af den fremtidige fart gennem vandet ved hjælp a
Sådan fungerer biomimikMenneskelige forsøg på at skabe effektive flyvende maskiner involverede ofte at studere, hvordan fugle flyver. Fabrice Coffrini/AFP/Getty Images Ubåde af den fremtidige fart gennem vandet ved hjælp a
- Europa viser udfordringer for amerikanske tilsynsmyndigheder mod Big Tech
- Drake slår ny streamingrekord - i videospil
- Hvad er jordens revolutionstid?
- Sekundære bygningsenheder (SBU'er) - vendepunktet i udviklingen af metal-organiske rammer (MOF'er…
- Undersøgelse afslører sammensætningen af gel-lignende stof opdaget af Change-4 rover på Moons …
- Metode til lagdeling af metaller med 2-D-materialet kan føre til helt nye egenskaber


