Forskere tyder mekanismer, der ligger til grund for ældningens biologi

Aldrende celler skifter periodisk deres kromatintilstand. Billedet illustrerer "til" og "fra" mønstre i individuelle celler. Kredit:UC San Diego
At forstå de faktorer, der styrer aldring, har været en af menneskehedens endeløse stræben, fra ungdommens mystiske springvand til praktiske sunde regimer for at forlænge levealderen.
Et team af forskere ved University of California San Diego har hjulpet med at tyde den dynamik, der styrer, hvordan vores celler ældes, og med det konsekvenser for forlængelse af menneskelig levetid. Som beskrevet i en undersøgelse offentliggjort i Procedurer fra National Academy of Sciences , en gruppe ledet af biolog Nan Hao anvendte en kombination af teknologier inden for teknik, datalogi og biologi for at analysere molekylære processer, der påvirker aldring.
Når cellerne ældes, skader i deres DNA akkumuleres over tid, fører til forfald i normal funktion og til sidst resulterer i død. En naturlig biokemisk proces kendt som "chromatin silencing" hjælper med at beskytte DNA mod skader. Silencing -processen omdanner specifikke områder af DNA fra en løs, åben tilstand til en lukket, dermed beskytter DNA -regioner. Blandt de molekyler, der fremmer dæmpning, er en familie af proteiner - stort set konserveret fra bakterier til mennesker - kendt som sirtuins. I de seneste år, kemiske aktivatorer af sirtuins har fået stor opmærksomhed og markedsføres som næringsstoffer for at hjælpe chromatin -dæmpning i håb om at bremse aldringsprocessen.
Men på samme tid, forskere har fundet ud af, at sådan chromatin -dæmpning også forhindrer de beskyttede DNA -regioner i at udtrykke RNA'er og proteiner, der udfører biologiske funktioner, og som følge heraf, overdreven dæmpning kan afspore normal cellefysiologi.
Brug af banebrydende beregningsmæssige og eksperimentelle tilgange i gær, som gjorde det muligt for forskerne at spore chromatin -lyddæmpning i hidtil uset detalje gennem generationer under ældning, UC San Diego -forskerne opdagede, at et fuldstændigt tab af sådan lyddæmpning fører til accelereret cellealdring og død. Imidlertid, forskerne fandt på samme måde, at kontinuerlig chromatin -dæmpning også fører celler til en forkortet levetid.
Så er chromatin -dæmpning eller ikke at dæmpe svaret på forsinkelse af ældning? Svaret stammer fra den nye undersøgelse:Begge.
Ifølge forskerne, naturen har udviklet en smart måde at løse dette dilemma på.
"I stedet for at blive i tilstanden til at dæmpe eller dæmpe tab, celler skifter deres DNA mellem de åbne (dæmpningstab) og lukkede (lyddæmpende) tilstande periodisk under ældning, "sagde Hao." På denne måde, celler kan undgå en forlænget varighed i begge stater, hvilket er skadeligt, og opretholde en tidsbaseret balance, der er vigtig for deres funktion og levetid. "
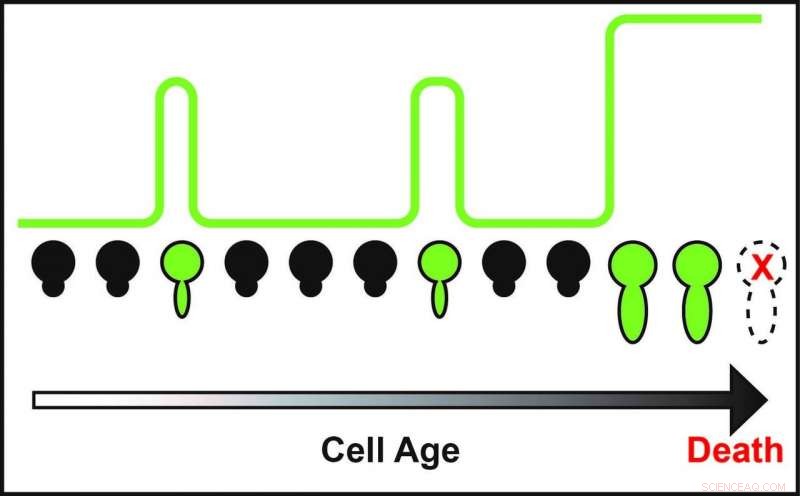
Celler skifter periodisk mellem "til" og "fra" i deres kromatintilstand under ældning. Aldrede celler mister denne koblingsevne, resulterer i celledød. Disse fund afdækker en potentiel årsag til cellulær ældning og foreslår nye måder at fremme levetid på. Kredit:UC San Diego
Fordi de udførte deres eksperimenter i gær, forskerne siger, at analyse af en sådan dynamik hos mennesker sandsynligvis vil være meget mere kompleks og kræve mere indviklede undersøgelser.
"Når cellerne bliver gamle, de mister deres evne til at opretholde denne periodiske omstilling, resulterer i ældede fænotyper og til sidst død, "sagde Hao." Implikationen her er, at hvis vi på en eller anden måde kan hjælpe celler med at forstærke skift, især når de bliver ældre, vi kan bremse deres ældning. Og denne mulighed er det, vi forfølger i øjeblikket. "
Hao krediterer resultaterne til et tværfagligt team af UC San Diego -forskere, der har komplementær ekspertise og deler en fælles interesse i undersøgelsen af aldring, herunder fakultet, studerende og postdoktorer. Ud over Haos ekspertise inden for molekylærbiologi/kvantitativ biologi, andre fakultetsmedlemmer i teamet inkluderer Lorraine Pillus (Molecular Biology), Jeff Hasty (Molecular Biology/Bioengineering) og Lev Tsimring (BioCircuits Institute). Det PNAS papir markerer de første betydningsfulde fund fra samarbejdet.
"Jeg tror, at dette samarbejde i den nærmeste fremtid vil frembringe mange nye indsigter, der vil transformere vores forståelse inden for den grundlæggende biologi for aldring og vil føre til nye strategier til at fremme levetid hos mennesker, "sagde Hao.
 Varme artikler
Varme artikler
-
 Sporing af et plantetrin:Efter frøspredning ved hjælp af chloroplast -DNACaliforniens guldfelter ( Lasthenia californica ) vokser i det sydlige Oregon, USA. Kredit:Monica Grasty Planter spreder deres frø ud over landskabet for at kolonisere nye områder, men det er sv
Sporing af et plantetrin:Efter frøspredning ved hjælp af chloroplast -DNACaliforniens guldfelter ( Lasthenia californica ) vokser i det sydlige Oregon, USA. Kredit:Monica Grasty Planter spreder deres frø ud over landskabet for at kolonisere nye områder, men det er sv -
 Biofysikere afslører nøjagtig foldning af et enkelt genModel til adskillelse af DNA, der foldes til en struktur kaldet kromatin. Kredit:Leiden Institute of Physics Den måde, hvorpå gener foldes, bestemmer deres aktivitet i vores krop. Leiden Universit
Biofysikere afslører nøjagtig foldning af et enkelt genModel til adskillelse af DNA, der foldes til en struktur kaldet kromatin. Kredit:Leiden Institute of Physics Den måde, hvorpå gener foldes, bestemmer deres aktivitet i vores krop. Leiden Universit -
 Hvordan kan en mutation i DNA påvirke proteinsyntesen?Nogle DNA-mutationer er tavse og har ingen virkning, men andre påvirker protein, essentielle molekyler for livet, der regulerer, om genet er aktivt eller ikke, fremstiller mere eller mindre protein el
Hvordan kan en mutation i DNA påvirke proteinsyntesen?Nogle DNA-mutationer er tavse og har ingen virkning, men andre påvirker protein, essentielle molekyler for livet, der regulerer, om genet er aktivt eller ikke, fremstiller mere eller mindre protein el -
 Tornadoer-effekter på PeopleTornadoes udøver ødelæggelse, uanset hvor de rører ned. Udover at forårsage tab af liv, flytter tornadoer bygninger, plukker træer fra jorden og sender noget, der ikke er forankret til jorden, der fly
Tornadoer-effekter på PeopleTornadoes udøver ødelæggelse, uanset hvor de rører ned. Udover at forårsage tab af liv, flytter tornadoer bygninger, plukker træer fra jorden og sender noget, der ikke er forankret til jorden, der fly
- Forskere finder, at cuttlebones mikrostruktur sidder på et sødt sted
- Hvordan flere stjernesystemer udvikler sig
- Citronsyre Pulver Anvendelser
- Hvordan virker en katapult?
- Sådan beregnes kombinationer og permutationer
- Hvad tænker folk egentlig om immigration til Australien? Vi analyserede deres internetforbrug for a…


