Designermolekyle peger på behandling af sygdomme forårsaget af DNA-gentagelser

En afbildning af den dobbelte spiralformede struktur af DNA. Dens fire kodningsenheder (A, T, C, G) er farvekodet i pink, orange, lilla og gul. Kredit:NHGRI
Ved at bruge et molekyle designet til at overvinde en vejspærring dannet af en almindelig type genetisk fejl, forskere ved University of Wisconsin-Madison har gjort fremskridt i retning af nye molekylære behandlinger af Friedreichs ataksi - en sjælden, men dødelig lidelse - i laboratorieskålen og hos dyr.
Friedreichs, ligesom mindst 40 andre genetiske sygdomme, er forårsaget af stræk af gentagne DNA, der forhindrer protein i at dannes korrekt.
Gentagelserne kan indeholde hundredvis af identiske, korte sekvenser af DNA (såsom GAAGAAGAAGAA ...). Ved nogle sygdomme, inklusive Friedreichs, gentagelserne bliver vejspærringer for cellulære maskiner, der afkoder genet og begynder at lave det protein, som cellen har brug for. Ved andre sygdomme, såsom den neurologiske tilstand Huntingtons, gentagelser kan resultere i overskydende protein, som i sig selv kan blive giftig.
I forskning rapporteret i denne uge i tidsskriftet Videnskab , Aseem Ansari, en professor i biokemi og genomik ved UW-Madison, og kolleger viste, at deres "molekylære protese" kan hjælpe cellulært maskineri med at overvinde blokaden fra gentagelserne i Friedreichs ataksi.
En komponent i protesen lokaliserer gentagelserne, så hjælper den anden cellemaskineri-soldaten forbi gentagelserne med at afkode genet korrekt.
Friedreich optræder kun hos én amerikaner ud af 50, 000, men det er fatalt og umuligt at behandle, siger Ansari. "Disse børn akkumulerer gentagelser i et gen for et protein kaldet frataxin, som mitokondrier, cellens kraftcenter, behov for at behandle energi. Uden frataxin, væv, der bruger mest energi, kommer først til skade:hjernen, hjerte og bugspytkirtel."
Allerede som 5 -årig, bevægelse er svækket "fordi hjernen ikke har den energi, den har brug for, og den ophober også DNA-skader, " siger Ansari, som har en fælles aftale med Genome Center of Wisconsin på UW-Madison. "De fleste unge mennesker med Friedreichs udvikler alvorlige hjerteproblemer og er kørestolsbundne, men sygdommen er så sjælden, at få medicinalfirmaer investerer i den."
I Ansari-gruppen, Graham Erwin, Matthew Grieshop og Asfa Ali dannede et team, der designede og skabte prototypemolekylet, og også orkestreret samarbejde med kolleger på UW-Madison, medicinalfirmaet Novartis, og et førende lægecenter i Indien.
Det Videnskab publikationen hvilede på to slags eksperimenter:
- I undersøgelser af cellelinjer fra mere end 20 Friedreichs patienter, den molekylære protese genoprettede ekspression af frataxinproteinet.
- Hos mus, der indeholder transplanterede humane celler, der bærer omkring 310 GAA-gentagelser, protesen genoprettede ekspressionen af et signalprotein til næsten normalt.
Molekylet, der testes, er designet til at hjælpe enzymet, der læser, eller "transskriberer, "DNA ved de forvirrende gentagelser. Når det når den anden side, enzymet, kaldet RNA polymerase, læser genet og laver RNA, der igen koder for frataxin, proteinet, der mangler i Friedreichs ataksi.
En del af det nye molekyle er "en retningssøger, som vi konstruerede til at lokalisere problemet i patientens genom, " siger Ansari. Når den finder de besværlige gentagelser, "den anden komponent bringer maskineriet ind, der hjælper RNA-polymerase med at smutte gennem gentagelserne og lave det korrekte transkript og efterfølgende det funktionelle protein."
Forståelsen af frataxins rolle og hvordan gentagelser blokerer dets syntese startede med undersøgelser i gærceller og derefter frugtfluer, Siger Ansari. "I disse simple organismer, videnskabsmænd drillede ud præcis, hvad gentagelsesregionen lavede, og de samme principper var på arbejde i menneskelige celler. Uden den forståelse, vi ville ikke have været i stand til at udtænke vores molekyler, som fremhæver behovet for at studere biologi på alle niveauer."
Selvom biokemien er kompleks, konceptet med at ignorere gentagelser er ikke, siger Ansari. "Hvis vi sammenligner enzymet, der læser DNA, med en motor, der bevæger sig ned ad 'sporet' af DNA, gentagelsen kan stoppe det koldt, få det til at springe for langt frem, eller sylt det i 'til' -positionen, så det danner en giftig mængde af proteinet. "
De nye resultater offentliggjort i denne uge i Videnskab foreslår, at "vi har fundet ud af, hvordan vi tænder den del af genet, der ignoreres, uden at gøre noget andet sted, " siger Ansari.
Selv når patienter og familier længes efter en kur, det vil sandsynligvis tage flere år, før medicintestning begynder, Ansari advarer.
Ansari, der har forsøgt at optrevle gentagelser i omkring 15 år på UW-Madison, opnåede indledende succes i 2004, da hans gruppe designede "to-hovedet" molekyler med et "DNA-læsehoved", der ville levere molekylet til et bestemt sted i en persons genom, og et "dockinghoved", der ville forankre en cellulær maskine for at tvinge genet til at blive læst korrekt på det sted.
Derefter, Ansari siger, forskere fandt ud af, at molekylet blev "distraheret", mens det svævede i et hav af DNA og undlod at skelne hundredvis af "look-alike" steder fra dets faktiske mål.
I 2013, finansieringen var tørret ud, og kun et tilskud fra W.M. Keck Foundation gjorde det muligt for Ansari at fortsætte med at søge for at undgå gentagelserne.
Mens mange bestræbelser på at behandle Friedreichs screener millioner af lægemidler, "Vi arbejder ud fra en dybere forståelse af problemet, " siger Ansari. "Når vi forstod, hvorfor enzymet blev blokeret, vi designede rationelt syv molekyler for at hjælpe enzymet med at passere obstruktionen."
Wisconsin Alumni Research Foundation har ansøgt om to patenter på opdagelsen, som Ansari mener kunne anvendes bredere. "Med de seneste fremskridt inden for menneskelig genomsekventering, mere end 40 sygdomme er blevet anerkendt som følge af mikrosatellitgentagelser, " siger Ansari, herunder skrøbelig X, som forårsager udviklingsmæssige vanskeligheder, og nogle typer muskeldystrofi.
"Nu hvor vi er begyndt at forstå, hvordan vi kan uskadeliggøre disse gentagelser, " han siger, "Vi ser dette som en generel løsning, et molekylært ingeniørprincip. Vi ville sekvensere genomet og finde ud af problemet, og lav et molekyle skræddersyet til den enkelte. Det er en ny præcisionsskræddersyet vej til personlig medicin."
 Varme artikler
Varme artikler
-
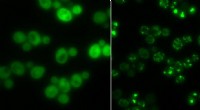 Klumper som midlertidig opbevaringGærceller uden proteinaggregater (til venstre) og dem med (lyse lysende pletter):I tider med sult, Klumperne tjener som midlertidig opbevaring for proteiner. Kredit:Matthias Peter / ETH Zürich For
Klumper som midlertidig opbevaringGærceller uden proteinaggregater (til venstre) og dem med (lyse lysende pletter):I tider med sult, Klumperne tjener som midlertidig opbevaring for proteiner. Kredit:Matthias Peter / ETH Zürich For -
 Mødre foretrækker døtre,Fædre foretrækker sønner, Undersøgelse siger En ny undersøgelse viste, at det er naturligt for kvinder at foretrække deres døtre og mænd deres sønner. Geber86/Getty Images Ny forskning hævder
Mødre foretrækker døtre,Fædre foretrækker sønner, Undersøgelse siger En ny undersøgelse viste, at det er naturligt for kvinder at foretrække deres døtre og mænd deres sønner. Geber86/Getty Images Ny forskning hævder -
 Celler fornemmer og udforsker deres omgivelserFor at gennemføre forskningen, forskere udviklede nogle lavstivheds gel-substrater, som et mønster af guldnanosfærer, der er dækket af et protein, klæbes til, og som kan kontrollere dens adskillelse.
Celler fornemmer og udforsker deres omgivelserFor at gennemføre forskningen, forskere udviklede nogle lavstivheds gel-substrater, som et mønster af guldnanosfærer, der er dækket af et protein, klæbes til, og som kan kontrollere dens adskillelse. -
 Sociale interaktioner tilsidesætter genetik, når fugle lærer nye sangeBengalesiske finker. Kredit:Brainard lab / UCSF Ny UC San Francisco -forskning finder ud af, at selv om unge mandlige sangfugle er genetisk disponerede for at lyde som deres fædre, beriget tidlig
Sociale interaktioner tilsidesætter genetik, når fugle lærer nye sangeBengalesiske finker. Kredit:Brainard lab / UCSF Ny UC San Francisco -forskning finder ud af, at selv om unge mandlige sangfugle er genetisk disponerede for at lyde som deres fædre, beriget tidlig
- Betydningen af røde orme i Ecosystem
- Overdreven nedbør som skader majsudbyttet som ekstrem varme, tørke
- Paris klimaforpligtelse, der lammer USA's vækst:Det Hvide Hus
- Hvad tænker folk egentlig om immigration til Australien? Vi analyserede deres internetforbrug for a…
- Sensor måler yoctonewton-kræfter hurtigt
- Forskere forklarer langsomtgående jordskælv kendt som langsom glidehændelser


