Forskere finder potentielle våben til kampen mod antibiotikaresistens
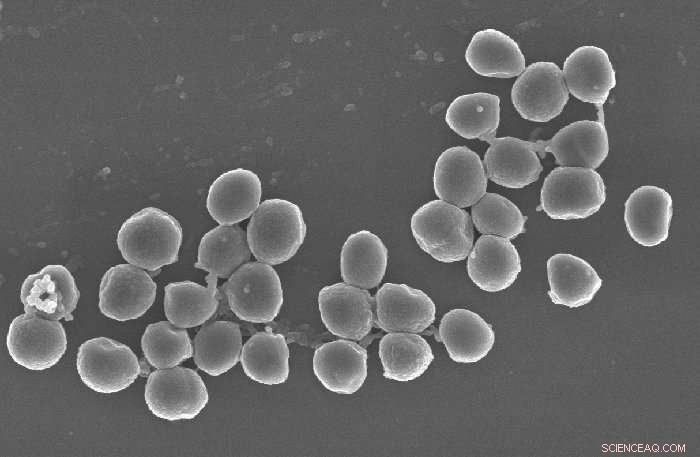
Elektronmikrofotografier af S. aureus . Kredit:Conlon Lab, UNC School of Medicine
Forskere ved UNC School of Medicine har fundet ud af, at en bakterie kan blive meget mere eller mindre modtagelig for et antibiotikum afhængigt af det specifikke bakteriesamfund i dens midte.
Forskerne fandt specifikt, at bakterien Pseudomonas aeruginosa kan producere specifikke molekylære faktorer, der dramatisk øger eller mindsker et antibiotikums evne til at dræbe Staphylococcus aureus, en anden bakterie, som ofte smitter sammen med P. aeruginosa .
Fundene, udgivet i PLoS Biologi , pege på muligheden for nye antibiotika, der anvender disse faktorer til at øge antibiotikafølsomheden.
Forskningen viser også, hvordan forståelsen af den præcise blanding af bakterier og deres interaktioner kan blive en standard del af klinisk praksis i behandling af bakterielle infektioner, især de mere farlige infektioner, der involverer antibiotikaresistens. Læger måler i øjeblikket antibiotikafølsomheden hos en inficerende bakterieart ved at undersøge den isoleret fra andre arter.
"Interaktionerne med P. aeruginosa kan helt ændre sig S. aureus 's modtagelighed for standard antibiotika, " sagde seniorforfatter Brian P. Conlon, PhD, adjunkt i mikrobiologi og immunologi ved UNC.
Resistens over for antibiotika fra bakterier og andre mikrober er en igangværende folkesundhedskrise, bidrager til omkring to millioner infektioner og 23, 000 dødsfald om året i USA, ifølge Centers for Disease Control and Prevention. P. aeruginosa , for eksempel, er et multiresistent patogen forbundet med hospitalserhvervede infektioner, herunder respirator-associeret lungebetændelse. Som for S. aureus ¬, nogle stammer forårsager ikke sygdom. Andre forårsager de klassiske "staph"-infektioner, som antibiotika dræber. Andre stammer, selvom, er antibiotika-resistente.
Forskere har kørt for at finde måder at overvinde modstanden af disse og andre bakterier.
Et spor i kapløbet om at overvinde antibiotikaresistens, som Conlon og kolleger afslørede, er, at S. aureus antager nogle gange en langsomt voksende, "lav-energi" tilstand, der gør det sværere at dræbe med antibiotika. Conlons team antog, at denne lavenergitilstand kunne opstå fra konkurrence mellem arter. Med andre ord, en co-inficerende bakterieart kan have udviklet evnen til at producere faktorer, der sætter mikrobielle konkurrenter i en ulempe. Sådanne faktorer kan omfatte toksiner, enzymer, eller forskellige bakterielle komponenter, der er unikke for specifikke stammer.
"Vi ved det P. aeruginosa almindeligvis co-inficerer med S. aureus og udskiller faktorer, der roder med S. aureus stofskiftet, " sagde Conlon. "Så vores hypotese var, at denne interaktion kunne være at kaste S. aureus ind i en mere antibiotika-resistent tilstand."
Conlon og kolleger, herunder førsteforfatter Lauren Radlinski, en kandidatstuderende i Conlon Laboratory, der udførte de fleste af eksperimenterne, undersøgte denne mulighed i den nye undersøgelse. De nedsatte et panel af S. aureus kulturer, udsat dem for molekyler udskilt af 14 forskellige P. aeruginosa stammer, og derefter testede hver kulturs modtagelighed for en af tre antibiotika:vancomycin, tobramycin, og ciprofloxacin.
Resultaterne var slående og har betydning for klinisk praksis.
Det P. aeruginosa påvirkede faktorer S. aureus følsomhed over for alle tre antibiotika, i nogle tilfælde i enormt omfang. Nogle stammer af P. aeruginosa , som forventet, væsentligt reduceret S. aureus 's modtagelighed for tobramycin og ciprofloxacin. Overraskende nok, selvom, mange andre stammer af P. aeruginosa stærkt forbedret S. aureus 's modtagelighed over for antibiotika brugt i eksperimenterne.
"Faktorer udskilt af otte af de P. aeruginosa stammer, for eksempel, inducerede 100 til 1000 gange flere drab af S. aureus af vancomycin, sammenlignet med kontrolkulturen af S. aureus som ikke blev udsat for P. aeruginosa faktorer, " sagde Conlon.
Forskerne identificerede tre specifikke P. aeruginosa faktorer, der var årsag til disse effekter:
- Et proteinskærende enzym kaldet LasA øgede vancomycins evne til at dræbe S. aureus .
- Et sæt fedt-relaterede molekyler kaldet rhamnolipider steg S. aureus 's optagelse af tobramycin.
- Et lille organisk molekyle kaldet HQNO hæmmede stofskiftet af S. aureus , skiftede det til lavenergitilstanden, hvilket gjorde det mere antibiotika-resistent.
Conlon og kolleger sagde, at det kunne være muligt at skabe nye antibiotika, der inkluderer de følsomhedsfremmende faktorer LasA og rhamnolipider - og/eller blokere den følsomhedsreducerende faktor HQNO - for at opbygge et bedre arsenal mod alvorlige bakterieinfektioner.
En anden tilgang ville være at udvikle simple bakterielle genetiske tests, der gør det muligt for læger at opdage, hvornår en co-inficerende bakterie sandsynligvis udskiller faktorer, der har væsentlig indflydelse på antibiotikafølsomheden.
Conlons hold er nu i gang med at sekventere P. aeruginosa stammer for at se, hvordan gensekvenser varierer mellem stammer, og hvordan denne varians påvirker disse stammers evne til at producere de førnævnte faktorer, som Conlons laboratorium har beskrevet.
 Varme artikler
Varme artikler
-
 Rekordmange hvaler talt i Argentinas PatagonienDenne 11. okt. 2017-billede viser en sydlig rethvalbrud i El Doradillo Beach, Patagonien, Argentina. Et rekordstort antal sydlige rethvaler migrerer hvert år fra Antarktis til Argentinas Patagonien fo
Rekordmange hvaler talt i Argentinas PatagonienDenne 11. okt. 2017-billede viser en sydlig rethvalbrud i El Doradillo Beach, Patagonien, Argentina. Et rekordstort antal sydlige rethvaler migrerer hvert år fra Antarktis til Argentinas Patagonien fo -
 Hvad er grundlaget for undtagelser fra Aufbau-princippet?Aufbau betyder opbygning på tysk, og Aufbau-princippet siger, at elektroner fylder elektronskaller omkring atomer i henhold til energiniveauet. Dette betyder, at elektronskaller og underskaller omk
Hvad er grundlaget for undtagelser fra Aufbau-princippet?Aufbau betyder opbygning på tysk, og Aufbau-princippet siger, at elektroner fylder elektronskaller omkring atomer i henhold til energiniveauet. Dette betyder, at elektronskaller og underskaller omk -
 Forskere rapporterer kemisk grundlag for celledelingstimeren, et muligt mål mod kræftTo faser af kræftcelledeling. Billedet viser de replikerede kromosomer i lilla. Cellen indeholder to spindler med mikrotubuli, vist med grønt. I det øverste billede, disse mikrotubuli har knyttet sig
Forskere rapporterer kemisk grundlag for celledelingstimeren, et muligt mål mod kræftTo faser af kræftcelledeling. Billedet viser de replikerede kromosomer i lilla. Cellen indeholder to spindler med mikrotubuli, vist med grønt. I det øverste billede, disse mikrotubuli har knyttet sig -
 Tilpasning til svingende temperaturerConstantin Zohner bestemmer tidspunktet for klorofylnedbrydning i bladene. Kredit:C. Zohner Vegetationens varighed - det vil sige den tid, der går mellem at bladre ud (forekomsten af det første
Tilpasning til svingende temperaturerConstantin Zohner bestemmer tidspunktet for klorofylnedbrydning i bladene. Kredit:C. Zohner Vegetationens varighed - det vil sige den tid, der går mellem at bladre ud (forekomsten af det første
- Tang-dynastiets adelskvinde begravet med sine æsler, for kærligheden til polo
- Spindende elektroner åbner døren til fremtidens hybridelektronik
- Forest Service vejer ændringer i beskyttelsen af salvie ryper
- Standardmodel af universet modstår mest præcise test af Dark Energy Survey (opdatering)
- Optiske teknikker undersøger toksiske stoffer i celler
- En ny måde at observere laserinteraktioner på kan forbedre laserbaseret fremstilling


