Design af et nyt substrat til myogen differentiering fra inducerede pluripotente stamceller
Siden deres opdagelse har forskere gentagne gange demonstreret de potentielle medicinske anvendelser af differentierede celler og væv genereret fra inducerede pluripotente stamceller (iPS). En væsentlig hindring for medicinske anvendelser i den virkelige verden er imidlertid relateret til det substrat, der bruges til at dyrke og inducere iPS-celler til differentierede celletyper.
Især selvom differentieringsprotokoller, der genererer myocytter og muskelstamceller (MuSC'er) fra iPS-celler, er blevet rapporteret, forbliver de relativt lav i effektivitet og kræver brug af et populært dyrebaseret substrat kaldet Matrigel.
Fremadrettet er mere effektive induktionsprotokoller og et skift mod xeno-frie (uden animalske produkter) substrater, der er i stand til at sikre omkostningseffektivitet, reproducerbarhed og sikkerhed, nødvendige.
Til dette formål har et samarbejdende team fra Japan kombineret deres ekspertise for at designe og validere et nyt rekombinant ekstracellulært matrixprotein, kaldet new generation laminin fragments (NGLF'er), til differentiering af iPS-celler til muskelcellelinjer.
Resultaterne af denne undersøgelse blev offentliggjort i Advanced Science den 29. april 2024.
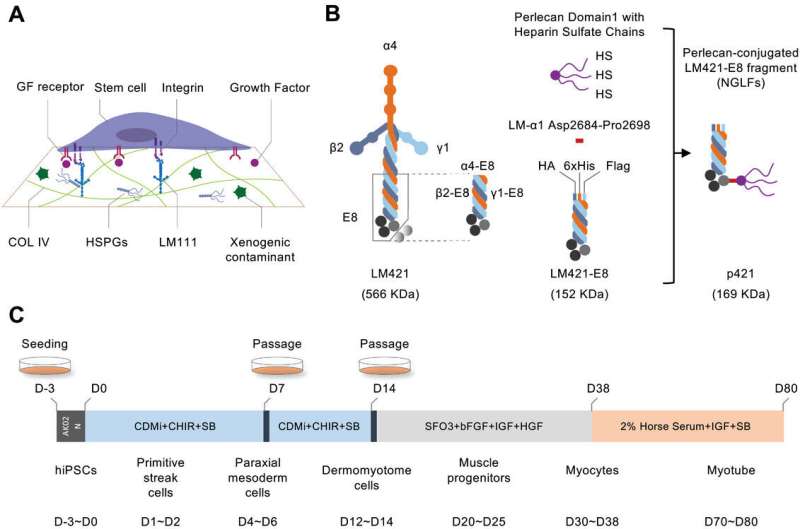
Tidligere undersøgelser har etableret rekombinante laminin E8 (LM-E8) fragmenter som et minimalt substrat for iPS cellekulturer, men de understøtter ikke myogen differentiering. For at identificere en LM-E8-variant, der er i stand til at understøtte myocyt- og MuSC-generering fra iPS-celler, testede holdet forskellige lamininer med forskellige sammensætninger, men fandt ud af, at de kun understøttede drastisk lavere niveauer af myogen differentiering.
Forskerne begrundede, at perlecan, en multifunktionel heparansulfat proteoglycan (HSPG) kerne med flere heparansulfatkæder i Matrigel, kan være afgørende for dens evne til at understøtte forskellige molekylære interaktioner, der er nødvendige for optimal iPS-cellevedligeholdelse og -differentiering, og designet således en LM-E8 vedhæftet til perlecan-domænet 1 med tre HS-kæder (D1-HS).
Forskerne observerede betydelige forbedringer i myogen differentiering ved at knytte denne modifikation til C-termini af LM-E8 varianter. Især p421-isoformen viste den bedste forbedring, endda bedre end Matrigel, så forskerne fokuserede på at bruge denne isoform til at generere myocytter og MuSC'er.
Ved at undersøge differentieringsmarkører på forskellige stadier (dvs. primitiv streak (PS), paraxial mesoderm (PM) og dermomyotom (DM)), bekræftede forskerholdet, at ikke kun NGLF'er er overlegne i forhold til tilsvarende LM-E8-varianter til at fremme stadiespecifikke markørgenekspression, p421 understøtter konsekvent bedre differentiering end nogen anden testet NGLF'er.
Forskerne fandt især, at p421 specifikt understøtter differentiering til PM-stadiet, da der ikke blev observeret gavnlige effekter fra p421 efter PM-dannelse. Ved at bruge heparitinase (til at nedbryde HS-kæder) og surfen (for at hæmme HS-medierede interaktioner), udledte de de gavnlige virkninger af p421, der primært stammer fra HS-delen.
Ved at blokere flere signalreceptorer og deres nedstrøms intracellulære effektorer bestemte de desuden, at p421 hovedsageligt virker gennem bFGF-FGFR-EGF-vejen for at fremme PM-induktion. Genekspressionsanalyse indikerede yderligere, at denne signalering understøttede HOX-genekspression for at fremme udifferentierede iPS-celler mod PS-stadiet.
For at demonstrere vigtigheden af konjugationsorientering mellem LM-E8 og D1-HS genererede forskerne p421-varianter ved at binde HS-delen til den N-terminale ende af β- eller γ-kæden af LM-E8. Selvom disse varianter øgede fasespecifik markørgenekspression, viste p421 væsentlig stærkere effekter ved sammenligning.
Ud fra disse resultater konkluderede forskerholdet, at p421 sandsynligvis hjælper FGFR-signalering ved at bringe HS-bundne FGF'er tættere på celleoverfladen for at fremme FGFR-dimerisering.
Endelig, for at illustrere, hvordan p421 forbedrer myogen differentiering og overvinder uoverensstemmelser, der plager de nuværende induktionsprotokoller, genererede forskerholdet sygdoms- og kontrol-iPS-cellelinjer for to former for muskeldystrofi, Duchene muskeldystrofi (DMD) og Miyoshi-myopati (MM).
Som forventet understøttede p421 stærkt forbedret myogen differentiering fra alle de undersøgte iPS-cellelinjer. Desuden fandt forskerne, at p421 forbedrede myogen differentiering på tværs af flere almindeligt anvendte kulturmedier.
Sammenfattende har forskerholdet med succes skabt et rekombinant proteoglycansubstrat, der understøtter betydelige forbedringer i myogen differentiering og demonstrerede dets underliggende mekanisme.
Det er håbet, at NGLF'er vil hjælpe med at etablere højeffektive, xeno-fri differentieringsprotokoller til at generere iPS-celleafledte muskelcellelinjer til medicinske anvendelser mod forskellige myopatier.
Flere oplysninger: Mingming Zhao et al., Heparan Sulfate Chain-Conjugated Laminin-E8 Fragments Advance Paraxial Mesodermal differentiation efterfulgt af høj myogen induktion fra hiPSC'er, Advanced Science (2024). DOI:10.1002/advs.202308306
Journaloplysninger: Avanceret videnskab
Leveret af Kyoto University
 Varme artikler
Varme artikler
-
 Ny teknologi belyser mikrober, der ikke kan dyrkes i et laboratoriumForskere brugte dette integrerede mikrofluidiske kredsløb til at udføre mini-metagenomisk mikrobiel celleopdeling og genomisk DNA-amplifikation. Kredit:Brian Yu På Stanford University, forskere ha
Ny teknologi belyser mikrober, der ikke kan dyrkes i et laboratoriumForskere brugte dette integrerede mikrofluidiske kredsløb til at udføre mini-metagenomisk mikrobiel celleopdeling og genomisk DNA-amplifikation. Kredit:Brian Yu På Stanford University, forskere ha -
 Udnyttelse af safranfarvens kraft til mad og fremtidige behandlingerEt KAUST-team har udtænkt en metode til at fremstille safrans aktive ingrediens fra frugten af en prydplante populær i Kina, Gardenia jasminoides, vist her til venstre. Til højre ses safran, verdens
Udnyttelse af safranfarvens kraft til mad og fremtidige behandlingerEt KAUST-team har udtænkt en metode til at fremstille safrans aktive ingrediens fra frugten af en prydplante populær i Kina, Gardenia jasminoides, vist her til venstre. Til højre ses safran, verdens -
 Krivende genetiske parasitter kan føre til nyt forsvar mod farlige bakterierFunktioner af plasmider, der koder for CRISPR-Cas-komponenter. (A) Mobilitetsforudsigelser for indsamlingen af ikke-redundante proteobakterielle plasmider analyseret i denne undersøgelse, præsentere
Krivende genetiske parasitter kan føre til nyt forsvar mod farlige bakterierFunktioner af plasmider, der koder for CRISPR-Cas-komponenter. (A) Mobilitetsforudsigelser for indsamlingen af ikke-redundante proteobakterielle plasmider analyseret i denne undersøgelse, præsentere -
 Undersøgelse viser genetiske forskelle mellem uptown og downtown rotter, der bor på ManhattanKredit:CC0 Public Domain (Phys.org) – Et lille team af forskere fra Fordham University og Providence College, både i USA, har fundet ud af, at der er små, men mærkbare genetiske forskelle mellem r
Undersøgelse viser genetiske forskelle mellem uptown og downtown rotter, der bor på ManhattanKredit:CC0 Public Domain (Phys.org) – Et lille team af forskere fra Fordham University og Providence College, både i USA, har fundet ud af, at der er små, men mærkbare genetiske forskelle mellem r
- Hvordan driver klimaændringer migration, og hvad kan man gøre ved det?
- Undersøgelse finder huller i viden om beskyttelse af kulturelle steder mod klimaændringer
- Inden 2025, kuldioxidniveauet i jordens atmosfære vil være højere end på noget tidspunkt i de si…
- NRL-forskere overvåger skiftende Arktis ved hjælp af lyd
- Periscope Facts for Kids
- Teknologi til nedbrydning af bakterier til at bekæmpe lægemiddelresistente superbugs


