Hvilken type binding indeholder alle biologiske makromolekyler sammen?
Her er hvorfor:
* kovalente obligationer Involver deling af elektroner mellem atomer. De er stærke og stabile, hvilket gør dem ideelle til at opbygge de komplekse strukturer af makromolekyler.
* kulhydrater: Monosaccharider er forbundet med glycosidiske bindinger , en type kovalent binding.
* Proteiner: Aminosyrer er forbundet med peptidbindinger , som også er kovalente obligationer.
* lipider: Fedtsyrer er knyttet til glycerol af esterbindinger , en anden type kovalent binding.
* nukleinsyrer: Nukleotider er forbundet med phosphodiester -bindinger , som er kovalente obligationer.
Mens kovalente obligationer er den primære kraft, der holder makromolekyler sammen, spiller andre typer obligationer også vigtige roller:
* Hydrogenbindinger: Disse svagere bindinger hjælper med at stabilisere de tredimensionelle strukturer af makromolekyler, som alfa-helix- og beta-arkstrukturer i proteiner.
* ioniske bindinger: Disse obligationer dannes af tiltrækningen mellem modsat ladede ioner, og de kan hjælpe med at stabilisere visse makromolekylære interaktioner.
* van der Waals Forces: Disse svage kræfter stammer fra midlertidige udsving i elektronfordeling og kan bidrage til den samlede stabilitet.
Selvom kovalente bindinger er hjørnestenen i makromolekylær struktur, hjælper samspillet mellem forskellige typer bindinger med at skabe de forskellige og funktionelle makromolekyler, der udgør levende organismer.
Sidste artikelHvad er fordelen ved at omslutte DNA i en kerne?
Næste artikelHvilket element findes i alle makromolekyler i livet?
 Varme artikler
Varme artikler
-
 Hvorfor bliver vi syge?At blive syg virker måske ikke rimeligt, men der er en grund til at det sker. Se flere sundhedsbilleder. Hemera/Thinkstock Der er mange lidelser, der kan ramme menneskekroppen, lige fra bilsyge til f
Hvorfor bliver vi syge?At blive syg virker måske ikke rimeligt, men der er en grund til at det sker. Se flere sundhedsbilleder. Hemera/Thinkstock Der er mange lidelser, der kan ramme menneskekroppen, lige fra bilsyge til f -
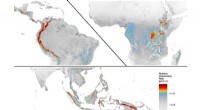 Jordens biodiversitet ændrer sig, efterhånden som planeten opvarmes. Men hvordan?Kort viser fordelingen af tropiske bjergskyskove, som estimeret ved hjælp af skydækkedata fra satellitter. Satellitter, der observerer Jorden, giver mange typer data om planetens økosystemer, og Map
Jordens biodiversitet ændrer sig, efterhånden som planeten opvarmes. Men hvordan?Kort viser fordelingen af tropiske bjergskyskove, som estimeret ved hjælp af skydækkedata fra satellitter. Satellitter, der observerer Jorden, giver mange typer data om planetens økosystemer, og Map -
 Hvordan hårfarve hjælper med at bevare den australske søløvebestandKredit:Unsplash/CC0 Public Domain Et innovativt nyt projekt er at bruge menneskehårfarve på australske søløver ved Carnac og Seal Islands ud for Perths kyst for at spore og lære om den lokale befol
Hvordan hårfarve hjælper med at bevare den australske søløvebestandKredit:Unsplash/CC0 Public Domain Et innovativt nyt projekt er at bruge menneskehårfarve på australske søløver ved Carnac og Seal Islands ud for Perths kyst for at spore og lære om den lokale befol -
 Hvor meget resistente stammer af svampe opstårScanningelektronmikrofotografi af infektiøse gærsporer (lilla) på overfladen af strukturen, hvor de produceres efter seksuel reproduktion (i blåt, basidium). Kredit:Chaoyang Xue, Kasey Carroll og Jo
Hvor meget resistente stammer af svampe opstårScanningelektronmikrofotografi af infektiøse gærsporer (lilla) på overfladen af strukturen, hvor de produceres efter seksuel reproduktion (i blåt, basidium). Kredit:Chaoyang Xue, Kasey Carroll og Jo
- Oceanografisk analyse tilbyder potentielt nedbrudssted for MH370
- At forbinde prikkerne på himlen kunne kaste nyt lys over mørkt stof
- Hvordan hjælper fossilerne i klippelag forskere med at identificere Rock Age?
- Hvad har bølgelængder mellem 380 og 750 nanometer?
- Ændringer i tryk, mere end temperatur, har stor indflydelse på, hvor hurtigt væsker bliver til ga…
- Dansende rosiner:Et simpelt køkkeneksperiment afslører, hvordan genstande kan udvinde energi fra d…


