Hvad er vigtigheden af datalogi inden for mikrobiologi?
1. Dataanalyse og fortolkning:
* sekventering af høj kapacitet: Mikrobiologer genererer massive datasæt fra sekventeringseksperimenter, som kræver kraftfulde beregningsværktøjer til analyse. Dette muliggør identifikation af forskellige mikrober i en prøve, deres overflod og deres genetiske variationer.
* Bioinformatik: Computeralgoritmer analyserer komplekse biologiske data som proteinsekvenser, genekspressionsmønstre og metaboliske veje, hvilket fører til indsigt i mikrobiel evolution, funktion og interaktioner.
* maskinlæring: Algoritmer kan trænes på store datasæt til at forudsige mikrobielle vækstmønstre, identificere potentielle antibiotiske mål og endda diagnosticere sygdomme baseret på mikrobielle signaturer.
2. Automation og screening med høj kapacitet:
* robotsystemer: Automatiske systemer til dyrkning, billeddannelse og analyse af mikrobielle prøver øger effektiviteten og gennemstrømningen i forskning.
* screening med høj kapacitet: Dette tillader test af tusinder af forbindelser mod mikrober til lægemiddelopdagelse og antibiotikaresistensundersøgelser.
* Virtuel screening: Computersimuleringer hjælper med at identificere potentielle lægemiddelkandidater ved at forudsige deres interaktion med mikrobielle mål.
3. Modellering og simulering:
* Mikrobiel økologimodellering: Simuleringer kan forudsige, hvordan mikrobielle samfund udvikler sig og reagerer på miljøændringer, hvilket muliggør udvikling af strategier til manipulering af mikrobielle populationer.
* Metabolisk modellering: Beregningsmodeller giver forskere mulighed for at forstå mikrobielle metaboliske veje og forudsige, hvordan mikrober reagerer på forskellige miljøforhold.
* Cellulær modellering: Simulering af individuelle mikrobielle celler hjælper forskere med at forstå deres vækst, stofskifte og interaktion med deres miljø.
4. Bioteknologi og applikationer:
* Syntetisk biologi: Computerstøttede designværktøjer muliggør konstruktion af nye mikrobielle stammer til forskellige formål, herunder bioremediation, biobrændstofproduktion og udvikling af nye terapeutiske midler.
* Mikrobiel genomteknik: Computational Tools hjælper forskere med at manipulere mikrobielle genomer til at introducere nye træk, forbedre deres funktioner eller studere deres mekanismer.
* Personaliseret medicin: Computerstøttet diagnostik ved hjælp af mikrobielle signaturer kan hjælpe med at skræddersy medicinsk behandling til individuelle patienter.
5. Forskning og uddannelse:
* Datavisualisering: Oprettelse af interaktive og informative visualiseringer af komplekse mikrobielle data forbedrer forståelse og kommunikation.
* online ressourcer og databaser: Offentligt tilgængelige databaser og webbaserede værktøjer giver adgang til store mængder mikrobielle data for forskere og undervisere.
* virtuelle laboratorier og simuleringer: Computerbaserede læringsressourcer giver studerende mulighed for at udforske koncepter inden for mikrobiologi på interaktive og engagerende måder.
I det væsentlige bemyndiger datalogi mikrobiologer til at analysere store datasæt, automatisere eksperimenter, modelkomplekse biologiske systemer og i sidste ende låse nye grænser op i forståelse og manipulere den mikrobielle verden.
Sidste artikelHvad er den måde, en celle, der er sammensat?
Næste artikelHvad er to ting lavet under cellulær respiration?
 Varme artikler
Varme artikler
-
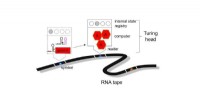 Celler programmeret som computere til at bekæmpe sygdomFigur, der viser RNA-kommandosekvensen. Kredit:Professor Jaramillo/University of Warwick Celler kan programmeres som en computer til at bekæmpe kræft, influenza, og andre alvorlige tilstande – tak
Celler programmeret som computere til at bekæmpe sygdomFigur, der viser RNA-kommandosekvensen. Kredit:Professor Jaramillo/University of Warwick Celler kan programmeres som en computer til at bekæmpe kræft, influenza, og andre alvorlige tilstande – tak -
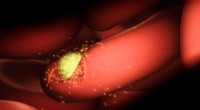 Kaprerparasit blokeret for infiltrerende blodStadig fra WEHI.TV af malariaparasit, der inficerer røde blodlegemer. Kredit:Dr Drew Berry, Walter og Eliza Hall Institute Et stort internationalt samarbejde ledet af Melbourne-forskere har opdage
Kaprerparasit blokeret for infiltrerende blodStadig fra WEHI.TV af malariaparasit, der inficerer røde blodlegemer. Kredit:Dr Drew Berry, Walter og Eliza Hall Institute Et stort internationalt samarbejde ledet af Melbourne-forskere har opdage -
 En sangfugl prangende gul hals? Det er der gener forForskning fra University of British Columbia (UBC) kunne have udpeget nogle af de genetiske maskiner, der er ansvarlige for fjerdragtfarven hos Audubons og myrtesanger, beslægtede, men tydeligt fjerbe
En sangfugl prangende gul hals? Det er der gener forForskning fra University of British Columbia (UBC) kunne have udpeget nogle af de genetiske maskiner, der er ansvarlige for fjerdragtfarven hos Audubons og myrtesanger, beslægtede, men tydeligt fjerbe -
 Cellular division -strategi deles på tværs af alle livsområderSEAS-forskere har fundet ud af, at disse pink-hued archaea-kaldet Halobacterium salinarum-bruger de samme mekanismer til at opretholde størrelse som bakterier og eukaryotisk liv, angiver, at celledivi
Cellular division -strategi deles på tværs af alle livsområderSEAS-forskere har fundet ud af, at disse pink-hued archaea-kaldet Halobacterium salinarum-bruger de samme mekanismer til at opretholde størrelse som bakterier og eukaryotisk liv, angiver, at celledivi
- Hvilken slags reaktion er KL (aq) agno3 (aq) -agl (r) KnO3 (aq)?
- Organisk kemiker bruger slagfluæg som retsmedicinsk værktøj
- Hvad er månens tyngdekraft i forhold til den jord?
- Forskere på jagt efter fossiler til planetdannelse afslører uventede excentriciteter i den nærlig…
- Hvad er 4 endokrine kirtler?
- Hvorfor pigen, der trækker sin vogn, har energi?


