Phosphofructokinase (PFK):Forståelse af allosterisk regulering
Her er en oversigt over, hvorfor PFK betragtes som allosterisk:
* Flere bindingssteder: PFK har to forskellige bindingssteder:
* Aktivt websted: Hvor substratet, fructose-6-phosphat, binder og omdannes til fructose-1,6-bisphosphat.
* Regulativt websted: Hvor allosteriske effektorer binder, hvilket påvirker enzymets aktivitet.
* Konformationsændringer: Bindingen af effektorer til det regulatoriske sted forårsager en ændring i enzymets form (konformation). Denne konformationsændring påvirker det aktive sted, enten aktiverer eller hæmmer dets aktivitet.
* Regulering af aktivitet: PFK's aktivitet reguleres af en række forskellige metabolitter. For eksempel:
* ATP: Høje ATP-niveauer virker som en allosterisk hæmmer, der bremser glykolysen, når cellen har nok energi.
* ADP og AMP: Omvendt aktiverer lave ATP-niveauer og tilstedeværelsen af ADP og AMP PFK, hvilket stimulerer glykolyse til at generere mere ATP.
* Citrat: Et produkt af citronsyrecyklussen, citrat hæmmer også PFK, når energiniveauet er højt.
* Feedbackkontrol: Denne allosteriske regulering giver mulighed for en følsom feedback-mekanisme. Cellen kan hurtigt justere sin glykolytiske hastighed baseret på tilgængeligheden af energi (ATP) og andre metaboliske signaler.
Sammenfattende betragtes PFK som allosterisk, fordi dets aktivitet er reguleret af bindingen af effektorer på et sted, der er forskelligt fra det aktive sted. Denne allosteriske regulering er afgørende for at kontrollere glykolyse og sikre, at cellens energibehov opfyldes effektivt.
Sidste artikelForstå oprindelsen af nye træk i arter:Mutationens rolle
Næste artikelMitose vs. Meiose:Forstå lighederne
 Varme artikler
Varme artikler
-
 Zebrafisk giver overraskende indsigt i, hvordan hjernen reagerer, når temperaturen stigerZebrafisk spiller hovedrollen, når ph.d.-kandidat Anna H. Andreassen eksperimenterer for at finde ud af, hvordan hjerneceller reagerer på temperaturændringer. Kredit:Ingebjørg Hestvik Hvilke organi
Zebrafisk giver overraskende indsigt i, hvordan hjernen reagerer, når temperaturen stigerZebrafisk spiller hovedrollen, når ph.d.-kandidat Anna H. Andreassen eksperimenterer for at finde ud af, hvordan hjerneceller reagerer på temperaturændringer. Kredit:Ingebjørg Hestvik Hvilke organi -
 Har du fortalt dig for følsom? Du kan være en empatAt være empatisk betyder, at du føler folks følelser dybt, og at du er kærlig og omsorgsfuld. Bare pas på ikke at blive udnyttet. Catherine Falls Commercial/Getty Images Hvis du nogensinde har fået a
Har du fortalt dig for følsom? Du kan være en empatAt være empatisk betyder, at du føler folks følelser dybt, og at du er kærlig og omsorgsfuld. Bare pas på ikke at blive udnyttet. Catherine Falls Commercial/Getty Images Hvis du nogensinde har fået a -
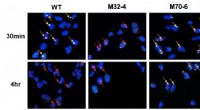 Forskere opnår en ny forståelse af reparationsprocessen for nukleotidudskæringSærskilt rolle for interaktionerne mellem RPA32 og RPA70 med XPA i NER. Celler blev bestrålet med UV, og colokaliseringen af XPA med UV-skadesteder blev visualiseret ved fluorescensmikroskopi. DNA-s
Forskere opnår en ny forståelse af reparationsprocessen for nukleotidudskæringSærskilt rolle for interaktionerne mellem RPA32 og RPA70 med XPA i NER. Celler blev bestrålet med UV, og colokaliseringen af XPA med UV-skadesteder blev visualiseret ved fluorescensmikroskopi. DNA-s -
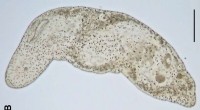 Undersøgelser af havdyr tyder på, at nervesystemet har udviklet sig uafhængigt flere gangeProporus sp., en xenacoelomorph. Kredit:Wikipedia/CC BY 2.5 (Phys.org) – Et team af forskere fra Norge, Sverige og Danmark har fundet beviser, der tyder på, at nervesystemet har udviklet sig uafhæ
Undersøgelser af havdyr tyder på, at nervesystemet har udviklet sig uafhængigt flere gangeProporus sp., en xenacoelomorph. Kredit:Wikipedia/CC BY 2.5 (Phys.org) – Et team af forskere fra Norge, Sverige og Danmark har fundet beviser, der tyder på, at nervesystemet har udviklet sig uafhæ
- Narkotikadetektion:ONR SCOUT tester teknologi til overvågning af ulovlig maritim last
- Cr(NO₃)₃:Forståelse af den kemiske formel for chrom(III)nitrat
- Opdagelse af længe søgte små eksplosioner, der superopvarmer solens korona
- Hvilket er det bedste sted at finde pH -værdier af salte?
- Hvad er de to hovedbevægelser på Jorden, når den rejser gennem rummet?
- Univers


