Forskere opnår en ny forståelse af reparationsprocessen for nukleotidudskæring
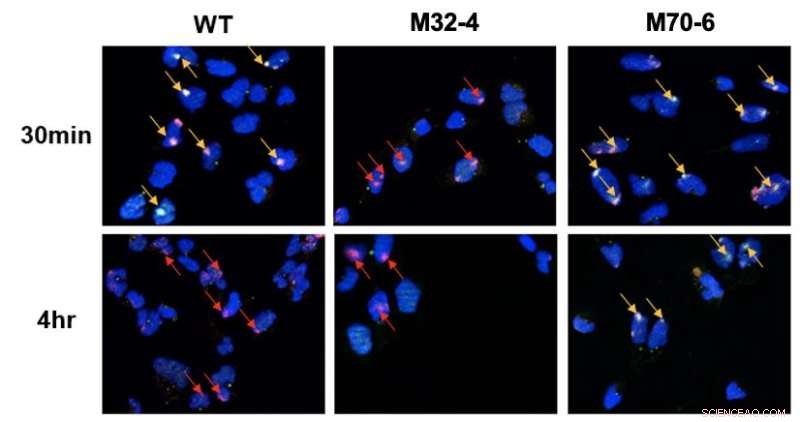
Særskilt rolle for interaktionerne mellem RPA32 og RPA70 med XPA i NER. Celler blev bestrålet med UV, og colokaliseringen af XPA med UV-skadesteder blev visualiseret ved fluorescensmikroskopi. DNA-skader er fremhævet med røde pile, og samlokalisering af XPA med UV-DNA er angivet med gule pile. I XPA-RPA32 mutantceller (M32-4) blev der observeret reduceret XPA-rekruttering til DNA-skade. I XPA-RPA70 mutantceller (M70-6) forblev XPA bundet på beskadigede steder i længere tid. Dette indikerer, at RPA32-interaktion med XPA er nødvendig for rekruttering af XPA til UV-induceret skade, mens RPA70-interaktion med XPA er vigtig for positionering af XPA for fuldførelse af NER. Kredit:Institut for Grundvidenskab
Nukleotidudskæringsreparation (NER) er en vigtig konserveret DNA-reparationsvej, som reparerer forskellige typer skader i genomet, såsom dem, der induceres af ultraviolet lys og miljømæssige midler. Dysfunktion i denne vej kan være skadelig for menneskers sundhed. For eksempel lider personer med defekter i NER af xeroderma pigmentosum, en sygdom karakteriseret ved en ekstrem disposition til sollys-induceret hudkræft på grund af manglende evne til at reparere UV-beskadiget DNA.
Mens NER således modvirker kræftdannelse, er det også vigtigt for antitumorbehandling. Mange antitumormidler, såsom cisplatin, inducerer skade på DNA, som kan repareres af NER. I denne sammenhæng er NER et lægemiddelmål af interesse for at forbedre kræftbehandlingsresultater. På molekylært niveau er NER en meget kompleks og dynamisk molekylær maskine, der involverer over 30 proteiner, der samles ved DNA-læsioner for at udskære skaden og erstatte den med intakt DNA. Denne proces er styret af protein-protein- og protein-DNA-interaktioner.
Et team af forskere ledet af Associate Director Orlando D. Schärer og kandidatstuderende Kim Mihyun fra Center for Genomic Integrity i Institute for Basic Science, Sydkorea, udforskede disse interaktioner. Holdet fandt ud af, at to nøgleproteiner i NER, nemlig xeroderma pigmentosum protein A (XPA) og replikationsprotein A (RPA) proteiner, er nødvendige for at organisere præ-incisionskomplekset i NER.
De to proteiner XPA og RPA er ansvarlige for organiseringen af NER-komplekset, efter at det har fundet skaden i DNA. Den nuværende undersøgelse sammenlignede mutante varianter af disse to proteiner for at undersøge, hvordan de to proteiner engagerer sig i en afgørende interaktion for NER-vejen. Specifikt blev det opdaget, at to interaktionsgrænseflader mellem XPA og RPA er kritiske for NER og har forskellige roller i forløbet. Interaktionen mellem XPA og RPA32 er afgørende for den indledende association mellem XPA og DNA-skade, hvorimod interaktionen mellem XPA og RPA70 er vigtig for fuldførelsen af NER.
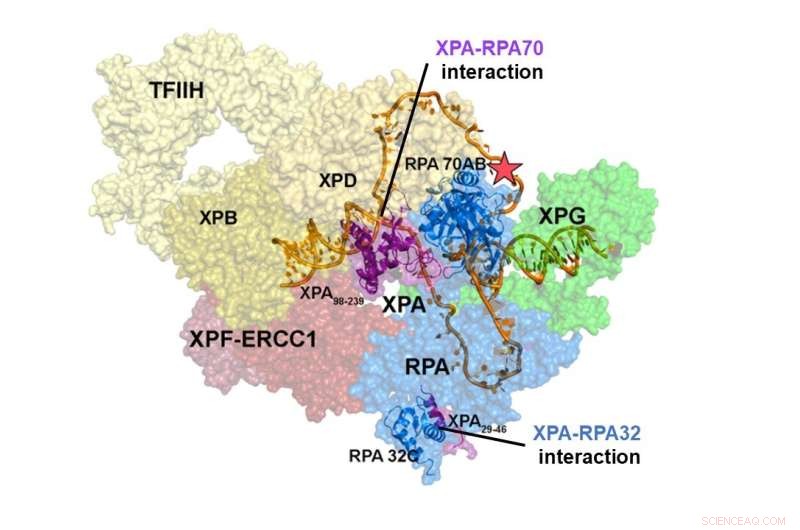
Struktur af NER pre-incision komplekset. Interaktionen mellem XPA og RPA70 er lokaliseret i midten af NER-komplekset, mens interaktionsstedet for XPA og RPA32 er i periferien. Interaktionerne mellem XPA og RPA70 stabiliserer præ-incisionskomplekset og indsnævrer DNA'et til at antage en U-form, som ser ud til at være den aktive form af komplekset, hvilket gør det muligt for det at fjerne DNA-skaden. Kredit:Institut for Grundvidenskab
Integrative strukturelle undersøgelser af et XPA-RPA-DNA-kompleks afslørede, hvordan interaktionerne mellem de to proteiner former NER-komplekset og udløser udskæring af skaden. Interaktionen mellem XPA og RPA32 sker i periferien af komplekset, hvor den letter den indledende samling af proteinerne på skadestedet. Interaktionen mellem XPA og RPA70 er placeret i hjertet af NER-komplekset og tvinger DNA'et til en U-form. Dette gør det muligt for de to ss/dsDNA-forbindelser at blive lokaliseret i umiddelbar nærhed, hvilket gør det muligt for NER-komplekset at incise DNA'et for at fjerne skaden.
Schärer udtalte, at deres "undersøgelse afslørede en overraskende ny model af NER-komplekset, og hvordan interaktionen mellem XPA og RPA former dets arkitektur. Afbrydelse af interaktionen mellem XPA og RPA hæmmer NER, og vores undersøgelse giver en blueprint for, hvordan denne interaktion kan være målrettet af små molekyler for at forbedre kræftbehandlingen. Vi fortsætter med at forfølge opfølgende forskning sammen med vores langsigtede samarbejdspartner på dette projekt, prof. Walter Chazin ved Vanderbilt University."
Denne forskning blev offentliggjort i Proceedings of the National Academy of Sciences . + Udforsk yderligere
Molekylær tags afslører, hvordan beskadigede lysosomer udvælges og markeres til clearance
 Varme artikler
Varme artikler
-
 Banebrydende ny teknologi sat til at accelerere den globale søgen efter afgrødeforbedringHastighedsforædling betyder, at det nu er muligt at dyrke så mange som 6 generationer hvede hvert år - en tredobling i forhold til de teknikker, der i øjeblikket bruges af opdrættere og forskere. Kred
Banebrydende ny teknologi sat til at accelerere den globale søgen efter afgrødeforbedringHastighedsforædling betyder, at det nu er muligt at dyrke så mange som 6 generationer hvede hvert år - en tredobling i forhold til de teknikker, der i øjeblikket bruges af opdrættere og forskere. Kred -
 Hvordan faldende pattedyrpopulationer i Florida Everglades er forbundet med den invasive burmesiske …Culex cedecei, der bider halen på en stiv bomuldsrotte. Kredit:Biology Letters Ny forskning offentliggjort i Biologibreve ser på, hvordan faldende pattedyrpopulationer i Florida Everglades er fo
Hvordan faldende pattedyrpopulationer i Florida Everglades er forbundet med den invasive burmesiske …Culex cedecei, der bider halen på en stiv bomuldsrotte. Kredit:Biology Letters Ny forskning offentliggjort i Biologibreve ser på, hvordan faldende pattedyrpopulationer i Florida Everglades er fo -
 Forskere, der studerer træringe, ser klimaændringssporKerneprøver kan indeholde spor til en skovs reaktion på klimaændringer. Kredit:Stephanie Mitchell/Harvard Staff Photographer Nogle gange er det at komme derhen, hvor du vil hen, et spørgsmål om at
Forskere, der studerer træringe, ser klimaændringssporKerneprøver kan indeholde spor til en skovs reaktion på klimaændringer. Kredit:Stephanie Mitchell/Harvard Staff Photographer Nogle gange er det at komme derhen, hvor du vil hen, et spørgsmål om at -
 Undersøgelse:Laguner fra arktiske glemte kyster sårbare over for klimaændringer og menneskelig ud…WCS-tekniker Thomas House holder en fårefisk - Aukulak Lagoon. Kredit:Kevin Fraley En ny videnskabelig oversigtsartikel ledet af WCS fanger de unikke og dynamiske egenskaber ved kystlaguneøkosystem
Undersøgelse:Laguner fra arktiske glemte kyster sårbare over for klimaændringer og menneskelig ud…WCS-tekniker Thomas House holder en fårefisk - Aukulak Lagoon. Kredit:Kevin Fraley En ny videnskabelig oversigtsartikel ledet af WCS fanger de unikke og dynamiske egenskaber ved kystlaguneøkosystem
- Kunne virksomheder kontrollere territorium i rummet? Under nye amerikanske regler, det kan være mul…
- Sladder er længe blevet misforstået. Sådan kan det hjælpe dit arbejde og sociale liv
- Lytte til motorblade for at stoppe fejl, katastrofer
- Nanojars fanger opløst kuldioxid, giftige ioner fra vand
- Advarsel om klimaændringer fra kollapsede gamle byer
- Nye angreb på grafikprocessorer bringer brugernes privatliv i fare


