Gensplejsning:Udnyttelse af DNA til landbrug, medicin og bioteknologi
Comstock/Comstock/Getty Images
Gener er lineære strækninger af DNA, der koder for funktionelle enheder - proteiner, enzymer eller nukleinsyrer. Ved strategisk at kombinere fragmenter af eksisterende gener i laboratoriemiljøer skaber forskerne nye genetiske konstruktioner, der udviser nye egenskaber. Denne teknik, kendt som molekylær kloning, er grundlaget for gensplejsning og muliggør introduktion af manipuleret DNA i planter, dyr eller dyrkede cellelinjer.
Hvorfor splejse gener?
Mens nogle går ind for minimal genetisk interferens, giver gensplejsning håndgribelige fordele på tværs af flere sektorer. Forskere bruger rutinemæssigt denne metode til at dissekere genfunktion, identificere terapeutiske mål og udvikle afgrøder med øget sygdomsresistens, ernæringsværdi eller miljømæssig modstandskraft. Inden for medicin giver genterapi – et aktivt felt understøttet af adskillige kliniske forsøg – skræddersyede løsninger til arvelige lidelser, der mangler effektive småmolekylære behandlinger. Derudover tjener konstruerede gener som produktionsplatforme for proteinbaserede lægemidler, vacciner og diagnostiske reagenser, hvilket forbedrer både effektivitet og tilgængelighed.
Gensplejsningsproces
Kernen i gensplejsning involverer samling af adskilte DNA-segmenter i en enkelt sammenhængende sekvens kaldet en kimær. Disse kimære gener klones typisk ind i cirkulære DNA-vektorer kaldet plasmider, som derefter introduceres i værtsceller via transformation eller transfektion. Selvom laboratorieprotokollen kan være indviklet – der kræver restriktionsenzymer, DNA-ligase og polymerasekædereaktion (PCR) – er de fleste genkonstruktioner let tilgængelige i offentlige plasmiddepoter, hvilket strømliner arbejdsgangen. Efter indsættelse bekræfter forskere integriteten, orienteringen og ekspressionspotentialet af det nye gen gennem sekventering og funktionelle assays.
Kodningsregioner
Den kodende region af et gen dikterer aminosyresekvensen af det resulterende protein. Forskere kan konstruere dette segment gennem bevidste mutationer eller ved at indsætte epitop-tags, lette sporing, oprensning eller funktionel analyse. Gensplejsning muliggør også design af helt nye proteiner med forbedrede eller nye biokemiske aktiviteter, hvilket udvider værktøjskassen til terapeutiske og industrielle anvendelser.
Ikke-kodende regioner
Ikke-kodende DNA – selvom det ikke er oversat til protein – spiller en kritisk regulerende rolle. Promotorsekvenser bestemmer hvornår, hvor og hvor stærkt et gen udtrykkes, mens forstærkere modulerer transkriptionelt output. Valget af promotor (f.eks. bakteriel, plante eller pattedyr) er afgørende, da ekspression på tværs af rige ofte mislykkes uden passende regulatoriske elementer. Yderligere ikke-kodende motiver styrer mRNA-stabilitet, lokalisering og sekretion og finjusterer derved det ultimative proteinudbytte og -funktion.
 Varme artikler
Varme artikler
-
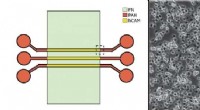 Forskere skaber 3D-cellearrays til mere realistiske eksperimentelle biologiske miljøerVed at bruge forskellige overfladebelægninger i holdets eksperimentelle mikrofluidiske miljø (til venstre) tillod levende kræftceller hurtigt at binde sig til en hCAM-belagt sektion (højre, venstre si
Forskere skaber 3D-cellearrays til mere realistiske eksperimentelle biologiske miljøerVed at bruge forskellige overfladebelægninger i holdets eksperimentelle mikrofluidiske miljø (til venstre) tillod levende kræftceller hurtigt at binde sig til en hCAM-belagt sektion (højre, venstre si -
 Vil klimaændringer øge risikoen for aflatoksin i amerikansk majs?Kredit:Pixabay/CC0 Public Domain Da klimaændringer fortsætter med at ændre vejrmønstre rundt om på planeten, inklusive Midtvesten, modellerer forskere ved Michigan State University (MSU) virkningen
Vil klimaændringer øge risikoen for aflatoksin i amerikansk majs?Kredit:Pixabay/CC0 Public Domain Da klimaændringer fortsætter med at ændre vejrmønstre rundt om på planeten, inklusive Midtvesten, modellerer forskere ved Michigan State University (MSU) virkningen -
 Tusindvis af johannesbrødtræer plantet, mens Cypern genopliver sort guldEn gruppe mænd planter et johannesbrødtræ under den første fase af et projekt i Oreites, nær Paphos den 26. november, 2017 med det formål at genoplive middelhavsøens sorte guld Næsten 6, 000 johan
Tusindvis af johannesbrødtræer plantet, mens Cypern genopliver sort guldEn gruppe mænd planter et johannesbrødtræ under den første fase af et projekt i Oreites, nær Paphos den 26. november, 2017 med det formål at genoplive middelhavsøens sorte guld Næsten 6, 000 johan -
 Bestræbelser på at redde havskildpadder er en global bevaringssucceshistorie:videnskabsmændDenne undersøgelse viser de langsigtede fordele ved havskildpadders bevaringsindsats globalt, og behovet for fortsat finansiering for at opretholde genopretningen. Kredit:Kostas Papafitsoros Ny fo
Bestræbelser på at redde havskildpadder er en global bevaringssucceshistorie:videnskabsmændDenne undersøgelse viser de langsigtede fordele ved havskildpadders bevaringsindsats globalt, og behovet for fortsat finansiering for at opretholde genopretningen. Kredit:Kostas Papafitsoros Ny fo
- En sjælden vild blomst er stjernen i Florida sump. Men kan spøgelsesorkidé overleve?
- Undersøgelse finder, at black box-metoder brugt af biologer sandsynligvis overvurderer antallet af …
- Hvordan et Hubble-billede går fra fotoner til færdig skønhed
- Undersøgelse viser, at det globale tab af skov over de sidste 35 år er blevet mere end opvejet af …
- Cuba udvider internetadgang, men under et meget forsigtigt øje
- Hvilken styrke er ansvarlig for revolution af planeter omkring solen?


