Hvorfor mikroskopisk farvning betyder noget:Forbedring af synlighed og analyse
Af Chris Deziel Opdateret 24. marts 2022
toeytoey2530/iStock/GettyImages
Farvning af en prøve før mikroskopisk undersøgelse øger primært synligheden, men dens fordele rækker langt ud over cellegrænserne.
Visse farvestoffer gennemtrænger cellevægge, oplyser indre strukturer og gør det muligt for forskere at observere metabolisk aktivitet in situ.
Desuden skelner pletter mellem levedygtige og ikke-levedygtige celler.
Derudover letter farvning præcis optælling af specifikke cellepopulationer inden for en given biomasse.
Over 20 forskellige farvningsreagenser er tilgængelige, hver skræddersyet til et bestemt diagnostisk eller forskningsmål.
TL;DR
Farvning fremhæver cellulære strukturer; valg af reagens afhænger af det analytiske mål.
Typer af pletter
Valget af farvestof afhænger af den specifikke funktion, du ønsker at visualisere. Ikke alle pletter er kompatible med levende celler, men de, der er – inklusive Bismarck-brune, toluenrøde, nilblå, nilrøde og DNA-bindende fluorescerende stoffer – bruges i vid udstrækning inden for cytologi og histologi.
Nogle pletter er rettet mod sporer, andre fremhæver lipider eller proteiner, mens nogle få skifter farve i nærvær af stivelse. For eksempel ville en praktiserende læge, der udfører en PAP-smear, påføre EosinY, et surt fluorescerende farvestof, der bliver skarpt rødt mod røde blodlegemer, cytoplasma og cellemembraner. Eosin Y bruges også rutinemæssigt til analyse af knoglemarvsaspirat.
I mange tilfælde er en enkelt plet utilstrækkelig. Hæmatoxylin, for eksempel, farver kerner blå, og når det parres med eosin, producerer det en kontrasterende rød eller lyserød baggrund, der får kernerne til at skille sig skarpt ud. Den kombinerede hæmatoxylin-eosin (H&E)-farvning er en fast bestanddel i patologien til undersøgelse af vævsarkitektur.
Gramfarve
Grams farvningsprocedure er en hjørnesten i klinisk mikrobiologi, der muliggør hurtig identifikation af bakterielle patogener. Teknikken anvender en række farvestoffer, der forskelligt farver gram-positive og gram-negative organismer.
Først påføres krystalviolet, hvorved alle celler farves til en ensartet violet. Dernæst fungerer jod som et bejdsemiddel, der låser farvestoffet fast i de tykke peptidoglycan-lag af gram-positive bakterier - typisk Staphylococcus og Streptococcus - så den violette forbliver efter affarvning. Endelig giver en modfarvning som SafranineO en rød eller lyserød nuance til gramnegative celler, hvilket skaber en klar kontrast mellem de to grupper.
Farvningsprocedure
Prøveforberedelse kan involvere tørmontering, vådmontering, sektionering eller udtværing. Til de fleste farvningsprotokoller foretrækkes en vådmontering:anbring en dråbe destilleret vand på objektglasset, placer prøven, og dæk med et dækglas. Påfør en dråbe af farvningsopløsningen til et hjørne; kapillærvirkning trækker farvestoffet hen over prøven. Ved at placere et papirhåndklæde på objektglasset modsatte side hjælper det med at suge overskydende væske ud, hvilket sikrer en jævn spredning. Når pletten er helt penetreret, er objektglasset klar til mikroskopisk evaluering.
Sidste artikelHvordan fosfolipider former cellulær struktur og funktion
Næste artikelHvilken organel danner bunden af Cilia og Flagella?
 Varme artikler
Varme artikler
-
 Yderligere 2 hvaler dør i Australien, da strandingsdødsfald når op på 200Hvaler er strandet på Ocean Beach ved Macquarie Harbour på vestkysten af Tasmanien i Australien, onsdag den 21. september 2022. Yderligere to hvaler døde fredag den 23. september 2022 i Australien
Yderligere 2 hvaler dør i Australien, da strandingsdødsfald når op på 200Hvaler er strandet på Ocean Beach ved Macquarie Harbour på vestkysten af Tasmanien i Australien, onsdag den 21. september 2022. Yderligere to hvaler døde fredag den 23. september 2022 i Australien -
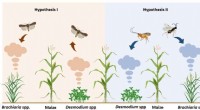 Hvordan push-pull ledsagende afgrøder hjælper med at håndtere den ødelæggende efterårshærormSkematisk repræsentation af et Push-Pull felt og forskningshypoteserne:(1) Ledsagende planteflygtige stoffer [Desmodium spp. mellemafgrøder (grønbladede desmodium, D. intortum eller sølvbladedesmodium
Hvordan push-pull ledsagende afgrøder hjælper med at håndtere den ødelæggende efterårshærormSkematisk repræsentation af et Push-Pull felt og forskningshypoteserne:(1) Ledsagende planteflygtige stoffer [Desmodium spp. mellemafgrøder (grønbladede desmodium, D. intortum eller sølvbladedesmodium -
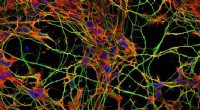 Forskere undersøger virkningerne af tau-proteiner på mikrotubuli i nervecellerNerveceller i vævskultur. Cellekerner i blåt, mikrotubuli i grønt, mikrofilamenter i rødt. Kredit:Tereza Humhalová Tau-proteinet er en vigtig faktor forbundet med udviklingen af humane neurodegen
Forskere undersøger virkningerne af tau-proteiner på mikrotubuli i nervecellerNerveceller i vævskultur. Cellekerner i blåt, mikrotubuli i grønt, mikrofilamenter i rødt. Kredit:Tereza Humhalová Tau-proteinet er en vigtig faktor forbundet med udviklingen af humane neurodegen -
 Svampe- og insektplanteædere påvirker urtediversiteten afhængigt af artstræk af urter og nabotræ…Kredit:Pixabay/CC0 Public Domain Mekanismerne for opretholdelse af biodiversitet har været et varmt emne i økologi i årtier. Svampe og insektplanteædere bidrager til mangfoldigheden af planter i
Svampe- og insektplanteædere påvirker urtediversiteten afhængigt af artstræk af urter og nabotræ…Kredit:Pixabay/CC0 Public Domain Mekanismerne for opretholdelse af biodiversitet har været et varmt emne i økologi i årtier. Svampe og insektplanteædere bidrager til mangfoldigheden af planter i
- Kan computerspil hjælpe landmænd med at tilpasse sig klimaforandringerne?
- Hvor kommer linjerne, der løber nord til syd, sammen?
- Skylning af tendenser i stofbrug tidligt i COVID-19-pandemien
- Yeti Investigation afslører ny information om Himalaya og tibetanske bjørne
- Er det rigtigt, at et område af en regnskov på størrelse med fodboldbanen bliver ødelagt hvert s…
- Hvad er nogle måder, kromatografi kan adskille kemikalier i en blanding?


