Forskere modellerer, hvordan giftige proteiner løber gennem hjernen, føre til sygdom
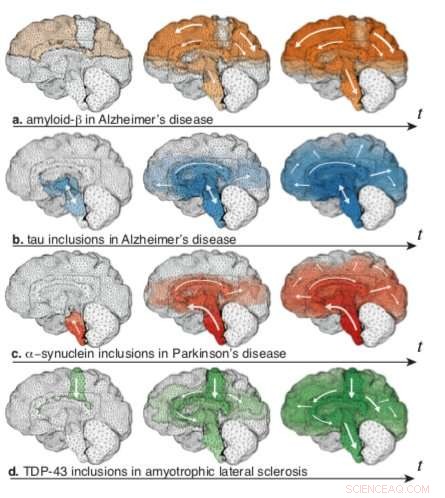
Aktiveringskort for den rumlige progression af toksisk protein for forskellige indledende såningsregioner simuleret på tværs af en 3D-hjerne Kredit:Stevens Institute of Technology
Mange neurodegenerative sygdomme spredes ved at kapre hjernens forbindelseskredsløb for at transportere giftige proteiner, som gradvist ophobes og udløser symptomer på demens. Nu, forskere ved Stevens Institute of Technology og kolleger har modelleret, hvordan disse giftige proteiner spredes gennem hjernen for at reproducere de afslørende mønstre af atrofi forbundet med Alzheimers sygdom, Parkinsons sygdom, og amyotrofisk lateral sklerose, eller ALS.
Arbejdet, offentliggøres i nummeret 12. oktober af Fysisk gennemgangsbreve , kunne åbne en ny grænse inden for computerhjernemodellering, da det fremhæver et første skridt mod at bygge bro mellem mikro- og makrotilgange – fra interaktionen af individuelle molekyler til medicinsk billedanalyse af hele hjernen. Det kan også udvide den grundlæggende forståelse af disse sygdomme, som anslås at påvirke mere end 12 millioner amerikanere inden for de næste 30 år, hvis det ikke kontrolleres.
"Dette er et første forsøg på at bygge bro mellem celleniveauet og hele organniveauet, " siger hovedforfatter Johannes Weickenmeier, en professor i maskinteknik ved Stevens. "Nøglen er at koble biokemi til hjernens biomekanik for bedre at forstå dynamikken i disse sygdomme."
Som postdoc forsker, Weickenmeier var banebrydende for en teknik til at bygge en digital hjerne ved at bruge 3-D-modelleringssoftware til at arrangere mere end 400, 000 pyramideformede virtuelle blokke, rekonstruerer blok for blok den højt foldede og buede struktur. "Det er en kunstform, " siger Weickenmeier. "At rekonstruere alle de individuelle folder er ret svært."
Han overlejrede derefter sin model med data hentet fra diffusionstensor-billeddannelse, som afslører retningerne for signaler, der passerer gennem hjernen. Nogle hjernestrukturer bærer hovedsageligt signaler i bestemte retninger, så den digitale model fanger ikke kun hjernens anatomiske træk, men også måden, hvorpå elektrokemiske signaler strømmer gennem dem.
At modellere spredningen af giftige proteiner gennem hjernen, Weickenmeier og hans team, herunder kollegerne Ellen Kuhl fra Stanford og Alain Goriely fra Oxford, brugte ligninger, der ligner dem, der beskriver, hvordan varme diffunderer gennem materialer.
De fandt ud af, at selvom forskellige neurodegenerative sygdomme ofte involverer meget forskellig biokemi - og producerer meget forskellige symptomer - kunne modellen gengive de afslørende mønstre af atrofi forbundet med Alzheimers sygdom, Parkinsons sygdom, og andre neurodegenerative sygdomme, blot ved at ændre de giftige proteiners udgangspunkt i hjernen.
"Disse mønstre af atrofi opstod i sagens natur fra vores system, " siger Weickenmeier.
Giftige proteiner "sås" forskellige steder for forskellige sygdomme, Weickenmeier forklarer, og deres spredning over hjernen - og derfor de symptomer, de producerer - er dikteret af de forbindelsesveje, der er tilgængelige for dem. Biokemi betyder stadig noget, men simuleringens effektivitet tyder på, at neuroanatomi og tilslutning også spiller en nøglerolle i at mediere progressionen af neurodegenerative sygdomme.
Mere raffinerede simuleringer kunne en dag fremskynde diagnose ved at forudsige symptomer, eller hjælpe forskere med at udvikle nye behandlinger. Imidlertid, digital hjernemodellering er i sine tidlige stadier, dels fordi der er relativt få data at bedømme modellens forudsigelser ud fra. På samme tid, hjernebilleddannelsesteknikker, der kan visualisere disse sygdomme, udvikles aktivt af neuroimaging-samfundet.
"Når vi har dem, vi vil være i stand til at kalibrere vores modeller for at lave nøjagtige patientspecifikke forudsigelser i fremtiden, " siger Weickenmeier.
Modellens potentiale strækker sig også til andre sygdomme. Lignende mekanismer understøtter dissemineret sklerose, samt kronisk traumatisk encefalopati, eller CTE, en sygdom, der sandsynligvis påvirker mennesker, der udsættes for gentagne hovedpåvirkninger, fra cheerleaders til fodboldspillere.
"Disse medicinsk relevante sygdomme, Alzheimers sygdom og andre neurodegenerative sygdomme er motivationen for vores 'in silico'-modeller, " siger Weickenmeier. "De giver os mulighed for strategisk at køre forskellige simuleringer for at teste individuelle hypoteser om sygdomsprogression og se, hvilke nye tilgange der virker lovende."
 Varme artikler
Varme artikler
-
 Ny undersøgelse af ferroelektri giver køreplan til logik med flere værdier til neuromorf computin…Et team af forskere fra Argonne, Lille Universitet for Videnskab og Teknologi og University of Picardie Jules Verne har lagt et teoretisk kort til brug af ferroelektrisk materiale (en klasse materiale
Ny undersøgelse af ferroelektri giver køreplan til logik med flere værdier til neuromorf computin…Et team af forskere fra Argonne, Lille Universitet for Videnskab og Teknologi og University of Picardie Jules Verne har lagt et teoretisk kort til brug af ferroelektrisk materiale (en klasse materiale -
 Er Mars eller Venus tættere på jorden?Svaret på, om Mars eller Venus er tættere på Jorden, er: Det afhænger. Mars og Venus er Jordens umiddelbare naboer i solsystemet. Imidlertid har alle tre planeter næsten cirkulære kredsløb rundt om
Er Mars eller Venus tættere på jorden?Svaret på, om Mars eller Venus er tættere på Jorden, er: Det afhænger. Mars og Venus er Jordens umiddelbare naboer i solsystemet. Imidlertid har alle tre planeter næsten cirkulære kredsløb rundt om -
 Fysikeren opdager mærkelige kræfter, der virker på nanopartiklerKredit:University of New Mexico Et nyt videnskabeligt papir udgivet, delvis, af et universitet i New Mexico kaster fysiker lys over en mærkelig kraft, der påvirker partikler på det mindste niveau
Fysikeren opdager mærkelige kræfter, der virker på nanopartiklerKredit:University of New Mexico Et nyt videnskabeligt papir udgivet, delvis, af et universitet i New Mexico kaster fysiker lys over en mærkelig kraft, der påvirker partikler på det mindste niveau -
 Lav strøm, højtydende optiske modtagereAlessandro Cevrero og team opnåede 60 Gb i sekundet ved hjælp af lys til at overføre data inden for cloud -datacentre. Kredit:IBM Tak til IBM -forskere udskiftning af kobbertråde med lys for at ov
Lav strøm, højtydende optiske modtagereAlessandro Cevrero og team opnåede 60 Gb i sekundet ved hjælp af lys til at overføre data inden for cloud -datacentre. Kredit:IBM Tak til IBM -forskere udskiftning af kobbertråde med lys for at ov
- Alt hvad du behøver at vide om forureningen, der dræber millioner af svin
- Afstanden til North Polar Spur
- Ny rapport anbefaler ændringer til amtslige afgrøde- og kontantlejevurderingsmetoder, der anvendes…
- Indiens stigende temperaturer er allerede dødelige, viser undersøgelse
- Stempling af billige nanoenheder
- Den berømte røde stjerne Betelgeuse snurrer hurtigere end forventet; kan have slugt en ledsager 10…


