Team simulerer, hvordan Alzheimers sygdom spredes gennem hjernen

Ellen Kuhl, professor i maskinteknik, håber, at evnen til at modellere neurodegenerative lidelser vil inspirere til bedre diagnostiske tests og behandlinger for at bremse deres virkninger. Kredit:L.A. Cicero
For første gang, Forskere har udviklet en computersimulering af, hvordan klumper af defekte proteiner i neurodegenerative sygdomme som Alzheimers spredes gennem hjernen, meget af tiden i stealth mode, over så længe som 30 år.
"Vi håber, at evnen til at modellere neurodegenerative lidelser vil inspirere til bedre diagnostiske tests og, ultimativt, behandlinger for at bremse deres virkninger, " sagde Stanfords mekaniske ingeniør Ellen Kuhl, der beskriver arbejdet i en artikel fra 12. oktober i Fysisk gennemgangsbreve medforfatter med Johannes Weickenmeier fra Stevens Institute of Technology og Alain Goriely fra Oxford University.
Simuleringerne fokuserer på Alzheimers, Parkinsons og amyotrofisk lateral sklerose (ALS, eller Lou Gehrigs sygdom), men forskerne mener, at deres teknik er generel nok til at arbejde for andre hjernesygdomme, der involverer misdannede proteiner, herunder kronisk traumatisk encefalopati.
Følg proteinerne
Gruppen vidste, at hver af de tre sygdomme, de studerede, producerede kendetegnende klumper af defekte, fejlfoldede proteiner, der opbygges i hjernen. For at se, hvordan de giftige klumper spredes over tid, Kuhl og hendes kolleger så på hjerneskiver taget fra mennesker, der døde efter at have udviklet en af de tre sygdomme. Tidligere forskere havde farvet disse hjerneskiver for at afsløre tilstedeværelsen af de forskellige proteiner af interesse.
Da Kuhls team lagde de resulterende data ind i en computer, de lavede også den matematiske modellering for at simulere, hvordan mønsteret af defekte proteiner spredes fra de relativt sparsomme klumper hos mennesker, der var tidligt i sygdommen, til meget mere udbredte klumper hos mennesker med fremskreden sygdom – en proces, der kan tage op til 30 år.
"Forestil dig en dominoeffekt, sagde Kuhl, der er en del af Stanford Neurosciences Institute og Stanford Bio-X. "Det, vores model gør, er at forbinde prikkerne mellem de statiske datapunkter, matematisk, at vise sygdomsprogression i hidtil usete detaljer."
I tilfælde af Alzheimers sygdom, forskerne modellerede udviklingen af to fejlfoldende proteiner - kendt som tau og amyloid beta - som begge ændrer form og danner giftige klumper i hjernen hos mennesker med sygdommen. Tidligere forskere havde farvet hjerneskiver for både proteiner og, med den nye model, Kuhls team var i stand til at skabe to simuleringer, der viser den forskellige måde, hver af disse varianter af sygdommen spredes på.
Spredning af defekten
Neurovidenskabsmænd ved ikke præcist, hvordan en klump af defekte proteiner påvirker sine naboer til at sprede fejlfoldningen, selvom Kuhl sagde, at der er tre fremherskende teorier. Modellens dyd, hun sagde, er, at den forudsiger sygdommens vej, uanset hvilken teori der er korrekt.
Kuhl planlægger nu at arbejde med neuroforskere for bedre at forstå mekanismerne for, hvordan proteinerne folder forkert. Disse indsigter ville forbedre deres model og måske føre til bedre måder at diagnosticere sygdommen på, mens den stadig er i stealth mode.
"Den virkelige udfordring er, at celledød fra giftige proteiner sker i årevis, hvis ikke årtier, før de første symptomer begynder at vise sig, " sagde Kuhl.
Kuhl planlægger også at gøre modelleringssoftwaren frit tilgængelig for andre forskere, gentager, hvad hun gjorde for ti år siden med lignende modeller for at studere hjertet - arbejde nu kendt som Living Heart Project. I dag, Kuhl sagde, mere end 150 akademiske og kommercielle laboratorier bruger Living Heart-softwaren til at teste kirurgiske procedurer eller designe enheder som hjerteklapper. Hjernesoftwaren bliver kendt som Living Brain Project.
"I betragtning af befolkningens aldring, ved midten af århundredet vil 135 millioner mennesker verden over have en form for demens, " sagde Kuhl. "Vi er nødt til at finde nye måder at anspore forskning i retning af diagnostik og interventioner, og computermodellering kan spille en nøglerolle i at identificere nye terapeutiske mål."
Sidste artikelNy memristor øger nøjagtigheden og effektiviteten for neurale netværk på atomskala
Næste artikelEn ny topologisk isolator
 Varme artikler
Varme artikler
-
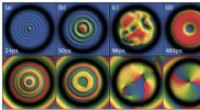 Ny mekanisme fundet til at generere gigantiske hvirvler i kvantevæsker af lysSpontan dannelse af en flerdobbelt ladet kvantehvirvel i et ringpumpet polaritonkondensat ved numerisk integration af lign. (3) og (4). Snapshots af tæthed (øverste række) og fase (nederste række) vis
Ny mekanisme fundet til at generere gigantiske hvirvler i kvantevæsker af lysSpontan dannelse af en flerdobbelt ladet kvantehvirvel i et ringpumpet polaritonkondensat ved numerisk integration af lign. (3) og (4). Snapshots af tæthed (øverste række) og fase (nederste række) vis -
 Manipulering af magnetisk domæne dynamik i ultratynde flerlagsmaterialerI den tværstangsmønstrede prøve, forskellige opførsel af perpendicualr feltdrevne ned-op DW-bevægelser uden HX kan genereres afhængigt af konfigurationen af AFM-spin. DW-udbredelse blev målt i a) vo
Manipulering af magnetisk domæne dynamik i ultratynde flerlagsmaterialerI den tværstangsmønstrede prøve, forskellige opførsel af perpendicualr feltdrevne ned-op DW-bevægelser uden HX kan genereres afhængigt af konfigurationen af AFM-spin. DW-udbredelse blev målt i a) vo -
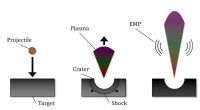 Hvorfor rumstøv udsender radiobølger, når det styrter ind i et rumfartøjHøjhastighedspåvirkningen af et stykke støv eller orbitalaffald genererer plasma og en tilhørende radiofrekvensemission. Kredit:Fletcher/Close Når rumfartøjer og satellitter rejser gennem rummet
Hvorfor rumstøv udsender radiobølger, når det styrter ind i et rumfartøjHøjhastighedspåvirkningen af et stykke støv eller orbitalaffald genererer plasma og en tilhørende radiofrekvensemission. Kredit:Fletcher/Close Når rumfartøjer og satellitter rejser gennem rummet -
 Nyt design kan gøre fiberkommunikation mere energieffektivHærens finansierede forskere udviklede et nyt design af optiske enheder, der kunne hjælpe med at gøre optisk fiberkommunikation mere energieffektiv. Kredit:University Pennsylvania Forskere siger,
Nyt design kan gøre fiberkommunikation mere energieffektivHærens finansierede forskere udviklede et nyt design af optiske enheder, der kunne hjælpe med at gøre optisk fiberkommunikation mere energieffektiv. Kredit:University Pennsylvania Forskere siger,
- Vi skal styrke miljøbeskyttelsen under tørken – eller stå over for irreversible tab
- NASA infrarøde billeder viser vindforskydning, der påvirker den tropiske storm Paulette
- Forskning udforsker en familieløs befolkning af ældre voksne i USA
- Store opgaver:Sikkerhed, planlægningsnøgle til at øge produktionsydelsen hos Spallation Neutron S…
- Sådan omdannes et akvarium til et økosystem
- Undersøgelse ser på, hvordan forbrugere reagerer på visse detailsalgskampagner


