Udlægning af retninger for fremtiden for pålidelige blodkoagulationsmolekylemodeller
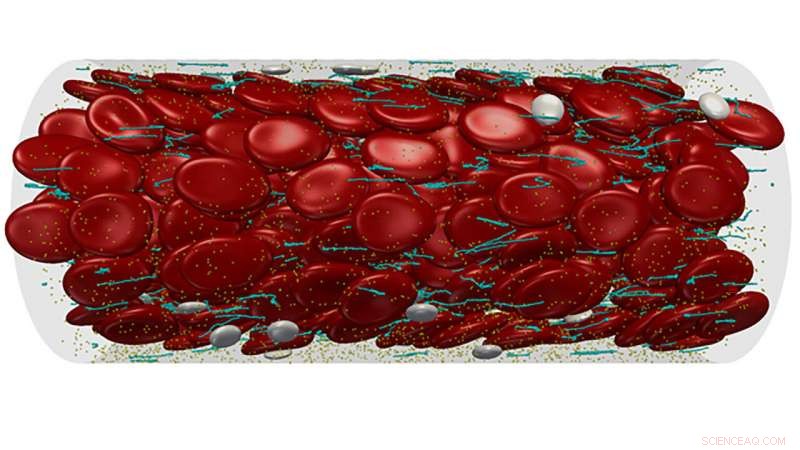
Forskere gennemgår nyligt arbejde med at forstå adfærden af con Willebrand-faktor i APL Bioengineering, male et portræt af vWF, og ved at fremhæve fremskridt på området, forfatterne fremlagde lovende veje til terapier til at kontrollere disse proteiner. Multiskala modellering af kompleks blodgennemstrømning gennem et mikrokar. Kredit:Zixiang Liu
Blodpropper har længe været involveret i hjerteanfald og slagtilfælde, tilsammen tegner sig for næsten halvdelen af dødsfaldene årligt i USA. Mens rollen som et nøgleprotein i processen, kaldet von Willebrand faktor, er blevet etableret, en pålidelig model til at forudsige, hvordan vWF samler sig i blodkar, er stadig uhåndgribelig.
Forskere ved Georgia Institute of Technology offentliggjorde en gennemgang af det seneste arbejde med at forstå vWF's adfærd i APL Bioengineering . Avisen maler et portræt af vWF, som ruller sig ud under forskydningsspændingen fra blodstrømmen for at danne net, der fanger blodplader, der passerer forbi, som så danner en blodprop, kaldes en trombe. Ved at fremhæve fremskridt på området, forfatterne fremlagde lovende veje til terapier til at kontrollere disse proteiner.
"Tromben skal blokere blodgennemstrømningen, når den lukker, som at prøve at bruge din tommelfinger for enden af en haveslange og derefter stoppe al strøm med noget mudder, "sagde David Ku, en forfatter på papiret. "Dette er ekstremt svært at opnå, så trombose kræver den hurtigste, stærkeste bånd i hele biologien."
En udfordring er, at mange af nutidens eksperimentelle modeller kun kan afbilde hændelser på mikron skala hvert sekund eller deromkring. vWF -proteiner, imidlertid, er cirka en tusindedel af den størrelse, og deres interaktioner sker på en tusindedel af den tid.
En række computermodeller er blevet foreslået for at bygge bro mellem mikroskala til nanoskala i koageldannelse, lige fra simuleringer baseret på den tid det tager for blodpropper at dannes til beregningsintensive modeller, der genskaber hvordan blodplader, vWF og celler interagerer alle i blodbanen. Artiklen opfordrer forskere på tværs af biologi, datalogi og andre områder til at samarbejde om at bygge en forbedret model.
Ud over at målrette blodpladeaggregering og miljøer med høj forskydning, der strækker vWF, en potentiel terapi er at øge aktiviteten af et andet protein, ADAMTS13, som spalter vWF og gør det ude af stand til at danne koagler. Mens forskning i musemodeller viser lovende, der kræves stadig meget arbejde for at afgøre, om ADAMTS13 -behandlinger ville være sikre eller effektive for mennesker.
Kus egen forskning pegede på negativt ladede nanopartikler, som beregningsmodellering har vist kan holde vWF i sin oprullede ureaktive tilstand. Gruppen fandt ud af, at nanopartiklerne reducerer, hvor hurtigt kar bliver tilstoppet, og undersøger, hvordan man kan forklare og optimere denne proces.
Ku sagde, at han håber, at papiret vil inspirere andre til at dykke dybere ned i nye måder at måle og forstå den koagulationsdannende vWF.
 Varme artikler
Varme artikler
-
 Forbedret modellering af nuklear struktur i francium hjælper med at søge efter ny fysikKredit:CC0 Public Domain Takket være forskere fra University of Queensland, vi kender nu med meget større sikkerhed franciumatomernes kernemagnetiske momenter. Dr. Ben Roberts, en postdocstipendi
Forbedret modellering af nuklear struktur i francium hjælper med at søge efter ny fysikKredit:CC0 Public Domain Takket være forskere fra University of Queensland, vi kender nu med meget større sikkerhed franciumatomernes kernemagnetiske momenter. Dr. Ben Roberts, en postdocstipendi -
 Brug af holografiske endoskoper til at observere fjerne objekterEn sekvens af hologrammer vist af en digital mikrospejlenhed former rumligt bølgefronterne koblet til en multimode optisk fiber på en sådan måde, at et fjernfeltsfokus scanner det distale synsfelt. Kr
Brug af holografiske endoskoper til at observere fjerne objekterEn sekvens af hologrammer vist af en digital mikrospejlenhed former rumligt bølgefronterne koblet til en multimode optisk fiber på en sådan måde, at et fjernfeltsfokus scanner det distale synsfelt. Kr -
 Fysikere forvandler en krystal til et elektrisk kredsløbKredit:Wikipedia/CC BY-SA 3.0 Washington State University fysikere har fundet en måde at skrive et elektrisk kredsløb ind i en krystal, åbner mulighed for gennemsigtighed, tredimensionel elektroni
Fysikere forvandler en krystal til et elektrisk kredsløbKredit:Wikipedia/CC BY-SA 3.0 Washington State University fysikere har fundet en måde at skrive et elektrisk kredsløb ind i en krystal, åbner mulighed for gennemsigtighed, tredimensionel elektroni -
 2-D topologisk fysik fra at ryste en 1-D-ledningKredit:CC0 Public Domain Begrænsning af kvantepartikler til at bevæge sig i en, to, eller tre dimensioner har ført til observation af mange slående fænomener. Et godt eksempel er kvantiseringen af
2-D topologisk fysik fra at ryste en 1-D-ledningKredit:CC0 Public Domain Begrænsning af kvantepartikler til at bevæge sig i en, to, eller tre dimensioner har ført til observation af mange slående fænomener. Et godt eksempel er kvantiseringen af
- Elektricitetsfri køleskab kan ændre millioner af liv
- Spiky ferrofluid thrustere kan flytte satellitter
- Sådan beregnes gennemsnitlig volumen
- Forskere afslører nye forståelser af syntetiske genkredsløb
- Hvordan transitskalering former byer
- Projektilbevægelse (fysik): Definition, ligninger, problemer (med eksempler)


