Feltopløst infrarød spektroskopi af biologiske systemer

Kredit:CC0 Public Domain
Forskere ved Laboratory for Attosecond Physics har udviklet en unik laserteknologi til analyse af molekylær sammensætning af biologiske prøver. Det er i stand til at detektere minimale variationer i den kemiske sammensætning af organiske systemer.
På det biokemiske niveau, organismer kan betragtes som komplekse samlinger af mange molekylarter. I løbet af deres stofskifte, biologiske celler syntetiserer kemiske forbindelser og modificerer dem på flere forskellige måder. Mange af disse produkter frigives til det intercellulære medium og akkumuleres i kropsvæsker, herunder blod. Et hovedformål med biomedicinsk forskning er at forstå, hvad disse uhyre komplekse blandinger af molekyler kan fortælle os om den pågældende organismes tilstand. Alle differentierede celletyper bidrager til denne 'suppe'. Men precancerøse og ondartede celler tilføjer deres egne specifikke molekylære markører - og disse giver de første indikationer på tilstedeværelsen af tumorceller i kroppen.
Indtil nu, imidlertid, meget få af disse indikatormolekyler er blevet identificeret, og dem, der kendes, vises i små mængder i biologiske prøver. Dette gør dem ekstremt vanskelige at opdage. Forskere antager, at mange af de mest informative molekylære signaturer omfatter kombinationer af forbindelser, der tilhører alle de forskellige typer molekyler, der findes i celler - proteiner, sukker, fedtstoffer og deres forskellige derivater. For at definere dem, forskere kræver en enkelt analytisk metode, der er alsidig og følsom nok til at opdage og måle deres niveauer.
Et tværfagligt team ledet af prof. Ferenc Krausz har nu bygget et nyt laserbaseret system, der er specielt designet til dette formål. Gruppen er baseret på Laboratory for Attosecond Physics (LAP), som drives i fællesskab af Ludwig-Maximilians-Universitaet (LMU) i München og Max Planck Institute for Quantum Optics (MPQ), og det omfatter fysikere, biologer og dataforskere. Dette system gør det muligt for forskere at opnå kemiske fingeraftryk i form af infrarøde spektre, der afslører molekylære sammensætninger af alle slags prøver, herunder prøver af biologisk oprindelse. Teknikken giver en hidtil uset følsomhed og kan bruges til alle kendte klasser af biomolekyler.
Det nye laserspektrometer bygger på teknologier, der oprindeligt blev udviklet i LAP til fremstilling af ultrakorte laserpulser, som bruges til at studere den ultrahurtige dynamik i subatomære systemer. Instrumentet, som blev bygget af fysikeren Ioachim Pupeza og hans kolleger, er designet til at udsende ekstremt kraftige pulser af laserlys, der dækker et bredt segment af spektret i den infrarøde bølgelængde. Hver af disse impulser varer et par femtosekunder (i videnskabelig notation 1 fs =10 -15 s, en milliontedel af en milliarddel af et sekund). Disse ekstremt korte glimt af infrarødt lys får de bindinger, der forbinder atomer til at vibrere. Effekten er analog med virkningen af at slå en stemmegaffel. Efter pulsens passage, de vibrerende molekyler udsender sammenhængende lys ved meget karakteristiske bølgelængder eller, tilsvarende, svingningsfrekvenser. Den nye teknologi gør det muligt at fange hele det udsendte bølgelængde. Da hver særskilt forbindelse i prøven vibrerer ved et bestemt sæt frekvenser, det bidrager med sit eget veldefinerede 'subspektrum' til emissionen. Ingen molekylære arter har nogen steder at skjule.
"Med denne laser, vi kan dække en lang række infrarøde bølgelængder - fra 6 til 12 mikrometer - der stimulerer vibrationer i molekyler, "siger Marinus Huber, fælles første forfatter af undersøgelsen og medlem af biolog Mihaela Zigmans gruppe, som også var involveret i forsøgene udført i LAP. "I modsætning til massespektroskopi, denne metode giver adgang til alle typer molekyler, der findes i biologiske prøver, ”forklarer hun.
Hver af de ultrakorte laserpulser, der bruges til at ophidse molekylerne, består kun af få få svingninger i det optiske felt. I øvrigt, pulsens spektrale lysstyrke (dvs. dens fotonæthed) er op til dobbelt så høj som dem, der genereres af konventionelle synkrotroner, som hidtil har fungeret som strålekilder for sammenlignelige tilgange til molekylær spektroskopi. Ud over, den infrarøde stråling er både rumligt og tidsmæssigt sammenhængende. Alle disse fysiske parametre tegner sig tilsammen for det nye lasersystems ekstremt høje følsomhed, gør det muligt at detektere molekyler til stede i meget lave koncentrationer og producere højpræcisionsmolekylære fingeraftryk.
Derudover prøver af levende væv op til 0,1 mm tykke kan nu belyses med infrarødt lys og analyseres med følsomhed uden sidestykke. I indledende forsøg, teamet på LAP anvendte teknikken på blade og andre levende celler, samt blodprøver. "Denne evne til nøjagtigt at måle variationer i kropsvæskers molekylære sammensætning åbner nye muligheder inden for biologi og medicin, og i fremtiden kunne teknikken finde anvendelse i den tidlige påvisning af lidelser, "Siger Zigman.
 Varme artikler
Varme artikler
-
 Oceanhitchhikers suttermekanisme giver potentiale for undervandsadhæsionEn remora. Kredit:NOAA CCMA Biogeography Team/Wikipedia En ny undersøgelse har afsløret, hvordan remora sukkerfisk løsner sig fra de overflader, de har klamret sig til - og hvordan mekanismen kunn
Oceanhitchhikers suttermekanisme giver potentiale for undervandsadhæsionEn remora. Kredit:NOAA CCMA Biogeography Team/Wikipedia En ny undersøgelse har afsløret, hvordan remora sukkerfisk løsner sig fra de overflader, de har klamret sig til - og hvordan mekanismen kunn -
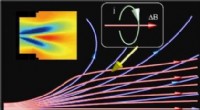 På vej til at skabe en elektrodeløs rumfartøjsfremdrivningsmotorFysisk billede af de anvendte magnetfeltlinjer (blå linjer) og magnetfeltlinjerne (røde linjer) modificeret af plasmaflowet, dvs. summen af de påførte og plasma-inducerede magnetfelter. Plasmaet red
På vej til at skabe en elektrodeløs rumfartøjsfremdrivningsmotorFysisk billede af de anvendte magnetfeltlinjer (blå linjer) og magnetfeltlinjerne (røde linjer) modificeret af plasmaflowet, dvs. summen af de påførte og plasma-inducerede magnetfelter. Plasmaet red -
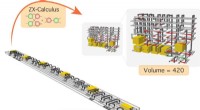 Ny tilgang til kredsløbskomprimering kunne levere kvantecomputere i den virkelige verden år før t…Kompression af et kredsløb, der har et indledende volumen på 882 ved hjælp af den foreslåede metode. Det reducerede kredsløb har et volumen på 420, mindre end halvdelen af dets oprindelige volumen.
Ny tilgang til kredsløbskomprimering kunne levere kvantecomputere i den virkelige verden år før t…Kompression af et kredsløb, der har et indledende volumen på 882 ved hjælp af den foreslåede metode. Det reducerede kredsløb har et volumen på 420, mindre end halvdelen af dets oprindelige volumen. -
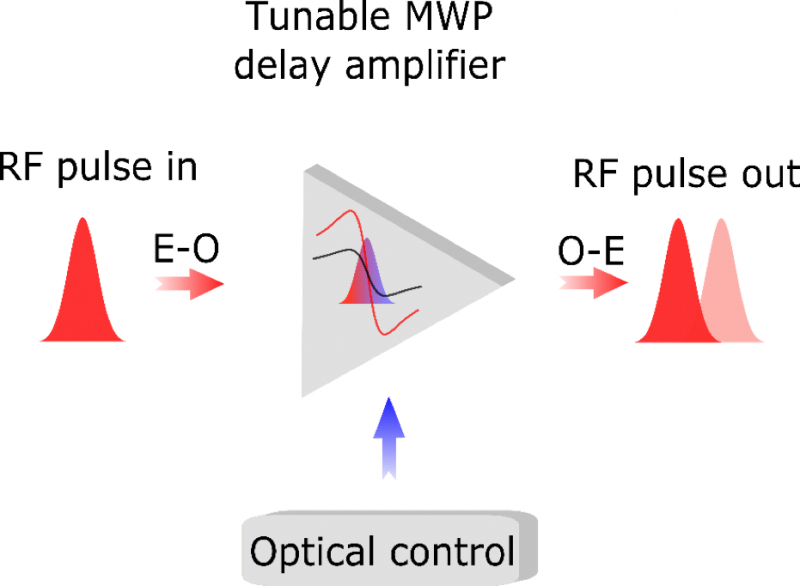 Fotonik bryder selvom baner vejen for forbedrede trådløse kommunikationssystemerEn skematisk illustration af den hurtige styring af RF -signaler. Kredit:University of Sydney Forskere fra ARC Center for Ultrahigh bandwidth Devices for Optical Systems (CUDOS) i University of Sy
Fotonik bryder selvom baner vejen for forbedrede trådløse kommunikationssystemerEn skematisk illustration af den hurtige styring af RF -signaler. Kredit:University of Sydney Forskere fra ARC Center for Ultrahigh bandwidth Devices for Optical Systems (CUDOS) i University of Sy
- Huawei beder retten om at smide forbud mod amerikanske telekommunikationsmidler tilbage
- Indien evakuerer 300, 000 fra cyklon
- Team opdager kvasar-tsunamier, der er i stand til at forhindre stjerner i at dannes
- To amerikanske rumvandrere erstatter låsende ende af robotarm
- At gifte sig er nu nemmere for mænd, forbedrer deres økonomiske velfærd, undersøgelse finder
- Brug af efterlignings- og forstærkningslæring til at tackle robotopgaver med lang horisont


