SERS med flydende grænseflade kunne se tidligere påvisning af Alzheimers sygdom
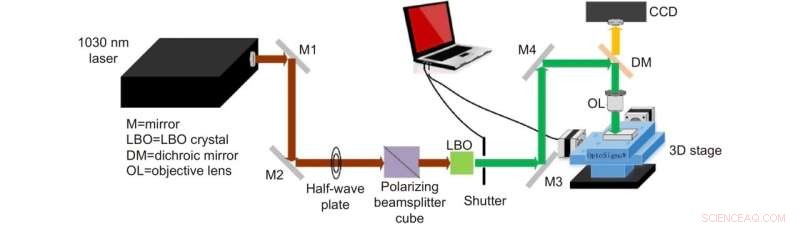
Figur 1. Skematisk af laserfremstillingssystem til mikrofluidiske SERS-chips. Kredit:Compuscript Ltd
En ny publikation fra Opto-Electronic Advances diskuterer mærkefri sporpåvisning af biomolekyler ved væskegrænsefladeassisteret overfladeforstærket Raman-spredning ved hjælp af en mikrofluidisk chip.
Surface-enhanced Raman scattering (SERS) har tiltrukket sig opmærksomhed inden for bioteknologi. Det skyldes dets høje følsomhed over for lokaliseret overfladeplasmonresonans af nanostrukturerede metaller. Sporpåvisning af biomolekyler med stor molekylvægt er fortsat udfordrende, fordi behandling af SERS-substrat ved hjælp af koblings- eller tværbindingsmidler er påkrævet. Forskerne anvendte væskegrænseflade assisteret SERS til at realisere mærkefri sporpåvisning af biomolekyler. Resultaterne tyder på, at det er lovende for tidlig diagnose af virusinfektion og Alzheimers.
Overfladeforstærket Raman-spredning (SERS), baseret på en optisk nærfeltseffekt induceret af overfladeplasmonen af ædelmetalnanopartikler eller nanostrukturer exciteret af laserstråling, forstærker Raman-signalerne op til 10 14 gange sammenlignet med almindelig Raman. På grund af dens øgede intensitet, fortsætter SERS-teknikken med at tiltrække voksende interesse for sporniveaudetektion og analyse af biomaterialer. Det har øget interessen for områder som billeddannelse af organeller i en enkelt celle, kræftcellesporing og biomarkøridentifikation.
SERS-teknikken kan anvendes i det biomedicinske område til sygdomsdiagnostik på et tidligt stadie og også i tumorterapi. Selvom forbedringsfaktoren for SERS typisk spænder fra 10 6 – 10 8 på grund af brugen af nye SERS-substrater og -metoder, er enkelt-molekyle-detektion ved mærkefri SERS upraktisk på grund af SERS-blinker, hvor oprindelsen af dette fænomen skyldes, at analytmolekyler undslipper fra hotspots. Desuden er biomolekyler, herunder deoxyribonukleinsyre (DNA) og proteiner, vanskelige at påvise direkte af SERS. Yderligere behandlinger med et SERS-substrat er nødvendige for at binde biomolekylerne.
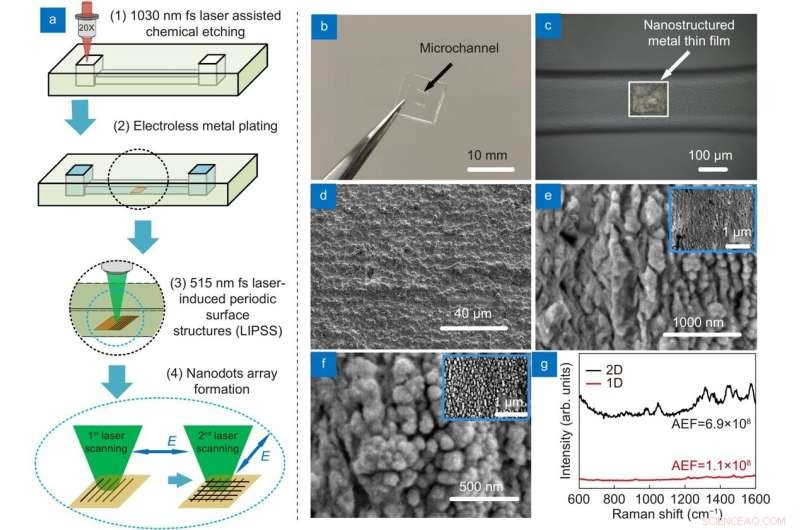
Figur 2. (a) Skematisk fremstilling (b) Fotografi af mikrofluidisk SERS-chip (c) Optisk mikroskopbillede, der viser SERS-substratet. SEM-billeder af (d) original metalfilm, (e) krusninger genereret ved 1. laserscanning og (f) nanodots genereret ved 2. laserscanning (Indsæt:lav forstørrelse af SEM-billede). (g) Raman-spektre af 10-9 M Rhodamine 6G (R6G) på 2-D (sort) og 1-D (rød) nanostrukturerede SERS-substrater. Kredit:Compuscript Ltd
Forskerholdet foreslog LI-SERS, som opnår en SERS-forbedringsfaktor på mere end 10 14 , meget højere end den almindelige SERS-metode. Den mikrofluidiske SERS-chip indeholdt et Ag-Cu SERS-substrat integreret i en indlejret glasmikrokanal. Hybrid femtosekund (fs) laserbehandling skabte græsmikrokanalen.
Den hybride fs-laserbehandling muliggør skabelsen af mere komplicerede 3D-strukturer med forbedrede funktionaliteter til biochips, sensorer og mikroelektroniske enheder. Når grænsefladen mellem analytopløsningen og luft på SERS-substratet i mikrofluidkanalen blev bestrålet af Raman-excitationslaseren, blev LI-SERS-intensiteten øget med seks størrelsesordener sammenlignet med almindelig SERS. Mekanismen for LI-SERS blev tilskrevet den synergetiske virkning af Marangoni-strømmen induceret af laserbestråling og optisk fangst. Denne laserbestråling ville lede analytmolekylerne til de varme punkter, hvor de opsamlede molekyler fanges af optisk kraft. Som følge heraf blev analytmolekylerne immobiliseret på SERS-substratet med opnåelse af stærk Raman-spredning.
Denne undersøgelse viste, at LI-SERS-metoden er anvendelig til mere praktisk brug. Det er specifikt nyttigt til sporpåvisning af mærkefri biomolekyler med store molekylmasser, herunder DNA-baser, DNA-sekvenser og β-Amyloid (Aβ). På grund af den ultrahøje følsomhed og selvimmobilisering af LI-SERS blev der opnået skelnen mellem DNA-baser og DNA-sekvenser med en detektionsgrænse på 1 fM uden at kræve yderligere behandlinger med koblings- eller tværbindingsmidler. Desuden kan LI-SERS-teknikken detektere mærkefri Aβ, en biomarkør for Alzheimers sygdom, ved niveauer under 1 pM, og med en lineær korrelation mellem Raman-signalet og Aβ-koncentrationen i området 1 nM-1 pM, der opnås. LI-SERS's etiketfri bio-sensing-evne giver et stort potentiale for tidlig diagnose af sygdomme i klinikker.
Som konklusion har forskerne givet et overblik over omfanget af LI-SERS-metoden til spordetektion af biomolekyler i mikrofluidiske SERS-chips med særlig reference til ultraspordetektion af DNA-baser og Aβ. En væskegrænseflade fik lov til at dannes i mikrokanalen. Marangoni-flowet og de optiske fangsteffekter induceret af LI-SERS demonstrerede en detektionsgrænse på 1 fM for mærkefrie DNA-baser. Bemærkelsesværdige træk ved LI-SERS-metoden, herunder den ultrahøje følsomhed og alsidighed forbundet med opsamling og selv-immobiliserende analytmolekyler på hot spots, vil være gavnlige for tidlige sygdomsdiagnoser såsom virusinfektioner og Alzheimers sygdom. + Udforsk yderligere
Ny SERS-metode udviklet til at fange målmolekyler
 Varme artikler
Varme artikler
-
 Fokuserede røntgenstråler afslører, hvordan sten under højt tryk omdannes til forskellige materi…Det eksperimentelle kammer ved Matter in Extreme Conditions -stationen ved SLACs Linac kohærente lyskilde. Dette kammer blev brugt til et eksperiment, der studerede transformationen af smeltet silic
Fokuserede røntgenstråler afslører, hvordan sten under højt tryk omdannes til forskellige materi…Det eksperimentelle kammer ved Matter in Extreme Conditions -stationen ved SLACs Linac kohærente lyskilde. Dette kammer blev brugt til et eksperiment, der studerede transformationen af smeltet silic -
 Når kerner indhenter elektronerI AttoCOLTRIMS -apparatet, den tredimensionelle bevægelse af elektroner (blå elliptiske pil) og ioner (H2+ og H+, grå pile) kan detekteres tilfældigt. Kombinationen af en ekstrem-ultraviolet (XUV, b
Når kerner indhenter elektronerI AttoCOLTRIMS -apparatet, den tredimensionelle bevægelse af elektroner (blå elliptiske pil) og ioner (H2+ og H+, grå pile) kan detekteres tilfældigt. Kombinationen af en ekstrem-ultraviolet (XUV, b -
 At bide på aluminiumsfolie kan være smertefuldt. Hvorfor?Bidende aluminiumsfolie kan være en smertefuld oplevelse. Getty Images At bide på aluminiumsfolie kan være smertefuldt og bliver normalt bemærket, hvis du har metal i munden fra tandlægearbejde (f.ek
At bide på aluminiumsfolie kan være smertefuldt. Hvorfor?Bidende aluminiumsfolie kan være en smertefuld oplevelse. Getty Images At bide på aluminiumsfolie kan være smertefuldt og bliver normalt bemærket, hvis du har metal i munden fra tandlægearbejde (f.ek -
 Sådan konverteres centimeter til centimeter SquaredEn centimeter er en enhed, der bruges til at måle et objekts længde. For eksempel er en blyant ca. 15 centimeter lang. Forkortelsen for centimeter er “cm.” En kvadratcentimeter er en enhed, der bruges
Sådan konverteres centimeter til centimeter SquaredEn centimeter er en enhed, der bruges til at måle et objekts længde. For eksempel er en blyant ca. 15 centimeter lang. Forkortelsen for centimeter er “cm.” En kvadratcentimeter er en enhed, der bruges
- En teori om fysik forklarer fragmenteringen af tropiske skove
- Koboltforsyning kan imødekomme efterspørgslen efter elektriske køretøjer og elektronikbatterier:…
- Sådan beregnes PH af pufferløsninger
- Multinationale selskaber handler på havtilstoppende plastik
- Præcisionslandbrug via satellitbilleddannelse
- Har blockchain fundet en anvendelse ud over kryptohandel?


