Hvorfor er radius af en negativ ion altid større end neutralt atom?
1. Øget elektron-elektron frastødning: Tilføjelsen af ekstra elektroner til den elektroniske sky fører til en stigning i elektron-elektron frastødning. Når antallet af elektroner stiger, bliver de frastødende kræfter mellem dem stærkere, hvilket får elektronerne til at sprede sig og optage større orbitaler. Denne udvidelse af elektronskyen resulterer i en samlet stigning i den ioniske radius sammenlignet med det neutrale atom.
2. Svagere nuklear tiltrækning: Den negative ladning af de ekstra elektroner i en anion skaber en stærkere elektrostatisk kraft mellem elektronerne og den positivt ladede kerne. Denne øgede nukleare tiltrækning er imidlertid ikke tilstrækkelig til at overvinde den øgede elektron-elektron frastødning. Som et resultat holdes elektronerne mindre tæt til kernen i anionen sammenlignet med det neutrale atom, hvilket bidrager til den større ionradius.
3. Afskærmningseffekt: De yderste elektroner (valenselektroner) i et atom oplever en reduceret effektiv kerneladning på grund af tilstedeværelsen af indre elektroner. Denne afskærmningseffekt bliver mere udtalt i en anion på grund af det øgede antal elektroner. Den øgede afskærmning reducerer tiltrækningen mellem valenselektronerne og kernen, hvilket tillader valenselektronerne at optage større orbitaler og øger den ioniske radius yderligere.
Det er værd at bemærke, at den specifikke størrelse af stigningen i ionradius afhænger af elementet og dets elektroniske konfiguration, men generelt er radius af en negativ ion altid større end radius for det tilsvarende neutrale atom.
 Varme artikler
Varme artikler
-
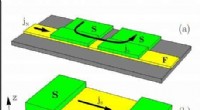 Bevægelige domænevægge inducerer tab i superleder/ferromagnet hybridsystemerJosephson Junction. Kredit:Universitetet i Jyväskylä/ Mihail Silaev Fysikere har vist, at bevægelsen af domænevægge kan detekteres ved at overvåge spænding genereret i superledende enheder. Denn
Bevægelige domænevægge inducerer tab i superleder/ferromagnet hybridsystemerJosephson Junction. Kredit:Universitetet i Jyväskylä/ Mihail Silaev Fysikere har vist, at bevægelsen af domænevægge kan detekteres ved at overvåge spænding genereret i superledende enheder. Denn -
 Big Bangs hemmeligheder og mørkt stofDet nye partikelacceleratorforsøg Belle II søger efter universets oprindelse. Kredit:Felix Metzner, KIT På det japanske forskningscenter for partikelfysik KEK, det nye partikelacceleratorforsøg Be
Big Bangs hemmeligheder og mørkt stofDet nye partikelacceleratorforsøg Belle II søger efter universets oprindelse. Kredit:Felix Metzner, KIT På det japanske forskningscenter for partikelfysik KEK, det nye partikelacceleratorforsøg Be -
 At finde de manglende brikker i puslespillet om en antineutrinos energiMINERvA-detektoren hos Fermilab hjælper videnskabsmænd med at analysere neutrino-interaktioner med atomkerner. Kredit:Reidar Hahn ladede partikler, som protoner og elektroner, kan karakteriseres v
At finde de manglende brikker i puslespillet om en antineutrinos energiMINERvA-detektoren hos Fermilab hjælper videnskabsmænd med at analysere neutrino-interaktioner med atomkerner. Kredit:Reidar Hahn ladede partikler, som protoner og elektroner, kan karakteriseres v -
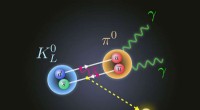 Forskere foreslår ny fysik for at forklare henfald af subatomære partiklerFSU-fysikere foreslog en ny partikel (gul) for at forklare nyligt rapporterede sjældne kaon (blå) henfald til neutrale pioner (orange). Kredit:Florida State University Florida State University-fys
Forskere foreslår ny fysik for at forklare henfald af subatomære partiklerFSU-fysikere foreslog en ny partikel (gul) for at forklare nyligt rapporterede sjældne kaon (blå) henfald til neutrale pioner (orange). Kredit:Florida State University Florida State University-fys
- Hvad er en halvleder? En elektrisk ingeniør forklarer, hvordan disse kritiske elektroniske komponen…
- Undersøgelse analyserede skatteaftaler for at vurdere effekten af offshoring på indenlandsk besk…
- Genetiske stregkoder bruges til at kvantificere afgørende populationer i et koralrevøkosystem
- Et nærmere kig på de forbindelser og molekyler, der er involveret i at give cannabis sin unikke du…
- Sådan forebygger du svindel med økologiske fødevarer
- Første globale kort over Pluto og Charon fra NASAs New Horizons -mission offentliggjort


