Hvad er ladningen på ion, hvis atomnummer 16 og masse 33 18 elektroner?
Givet atomnummer =16 (repræsenterer antallet af protoner)
Antal elektroner =18
Massetal =33 (summen af protoner og neutroner)
Massetallet kan udtrykkes som:
Massetal =Antal protoner + Antal neutroner
Ved at omarrangere formlen:
Antal neutroner =Masseantal - Antal protoner
Antal neutroner =33 - 16 =17
Lad os nu beregne ladningen på ionen:
Ionens ladning =Antal protoner - Antal elektroner
Ionens ladning =16 - 18
Ionens ladning =-2
Ionen har en ladning på -2, hvilket indikerer, at den har fået to ekstra elektroner i forhold til antallet af protoner. Dette resulterer i en netto negativ ladning.
 Varme artikler
Varme artikler
-
 Nye former for laserstråler smutter gennem uigennemsigtige medierVed at forme sin rumlige bølgefront, en laserstråle kan forplante sig gennem et stærkt spredt medium uden lateral diffusion. Ud over, lysets tilbagespredning undertrykkes. Kredit:Yale University F
Nye former for laserstråler smutter gennem uigennemsigtige medierVed at forme sin rumlige bølgefront, en laserstråle kan forplante sig gennem et stærkt spredt medium uden lateral diffusion. Ud over, lysets tilbagespredning undertrykkes. Kredit:Yale University F -
 Ny kvantehukommelse gemmer information i timevisNogle steder i krystalgitteret, et kulstofatom (hvidt) mangler, og på nabostedet er der et nitrogenatom (gult). Kredit:Vienna University of Technology Lagring af information i et kvantehukommelses
Ny kvantehukommelse gemmer information i timevisNogle steder i krystalgitteret, et kulstofatom (hvidt) mangler, og på nabostedet er der et nitrogenatom (gult). Kredit:Vienna University of Technology Lagring af information i et kvantehukommelses -
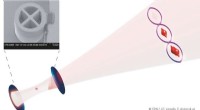 Generering af lys i en kvantesuperposition med et fotonantalSkematisk fremstilling af eksperimentet. En kvantepunkt koblet til en optisk mikrohulrum (i indsat et ægte billede af enheden) udsender lys i en tilstand, der samtidig er en enkelt foton, to fotoner,
Generering af lys i en kvantesuperposition med et fotonantalSkematisk fremstilling af eksperimentet. En kvantepunkt koblet til en optisk mikrohulrum (i indsat et ægte billede af enheden) udsender lys i en tilstand, der samtidig er en enkelt foton, to fotoner, -
 Tæt adskilte hydrogenatomer kunne lette superledning i omgivelsesbetingelserIllustration af en atomstruktur i zirkoniumvanadiumhydrid ved nær omgivende forhold som bestemt ved hjælp af neutronvibrationsspektroskopi og Titan -supercomputeren ved Oak Ridge National Laboratory.
Tæt adskilte hydrogenatomer kunne lette superledning i omgivelsesbetingelserIllustration af en atomstruktur i zirkoniumvanadiumhydrid ved nær omgivende forhold som bestemt ved hjælp af neutronvibrationsspektroskopi og Titan -supercomputeren ved Oak Ridge National Laboratory.
- Gravitationsbølger giver et indblik i fortiden - men vil vi nogensinde fange krusninger fra Big Ban…
- Japan har opgivet årtiers pacifisme som reaktion på Ukraines invasion og øget kinesisk pres på T…
- Anvendelse af fysik til at forstå bevidsthedens mysterium
- Geologer viser en hidtil uset opvarmning i Tanganyika-søen
- Når kolde atomer møder nano:En kablet kvanteknude
- Udtalelse:Canadas tilgang til måneudforskning skal være strategisk eller godt blive efterladt


