Hvorfor kaldes gasmolekylers bevægelse også termisk bevægelse?
Den tilfældige bevægelse af gasmolekyler er det, der forårsager trykket af en gas. Når gasmolekyler kolliderer med væggene i deres beholder, udøver de en kraft på væggene. Jo større antal kollisioner pr. arealenhed, jo større er gastrykket. Da antallet af kollisioner pr. arealenhed stiger med temperaturen, stiger trykket af en gas også med temperaturen.
Termisk bevægelse er også ansvarlig for diffusionen af gasser. Diffusion er den proces, hvorved gasmolekyler spredes fra et område med høj koncentration til et område med lav koncentration. Dette sker, fordi gasmolekyler konstant bevæger sig og kolliderer med hinanden, og disse kollisioner får dem til at ændre retning og sprede sig.
Forståelse af termisk bevægelse er afgørende for at forstå gassers adfærd. Det er et grundlæggende koncept inden for termodynamik og fluidmekanik, og det har anvendelser inden for mange områder inden for videnskab og teknik.
 Varme artikler
Varme artikler
-
 Forskere skaber kvantemikroskop, der kan se det umuligeKunstnerens indtryk af UQs nye kvantemikroskop i aktion. Kredit:University of Queensland I et stort videnskabeligt spring, University of Queensland forskere har skabt et kvantemikroskop, der kan a
Forskere skaber kvantemikroskop, der kan se det umuligeKunstnerens indtryk af UQs nye kvantemikroskop i aktion. Kredit:University of Queensland I et stort videnskabeligt spring, University of Queensland forskere har skabt et kvantemikroskop, der kan a -
 Fysikere opdager, at nogle plasma-ustabiliteter kan slukke sig selvPPPL-fysiker Fatima Ebrahimi. Kredit:Elle Starkman Fysiker Fatima Ebrahimi ved det amerikanske energiministeriums (DOE) Princeton Plasma Physics Laboratory (PPPL) har for første gang brugt avancer
Fysikere opdager, at nogle plasma-ustabiliteter kan slukke sig selvPPPL-fysiker Fatima Ebrahimi. Kredit:Elle Starkman Fysiker Fatima Ebrahimi ved det amerikanske energiministeriums (DOE) Princeton Plasma Physics Laboratory (PPPL) har for første gang brugt avancer -
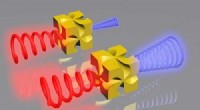 Metamateriale forbedrer signifikant chirale nanopartikelsignalerGrafisk abstrakt. Kredit:ACS Photonics (2022). DOI:10.1021/acsphotonics.1c00882 Venstre hånd ligner højre hånd i spejlet, men venstrehåndshandsken passer ikke på højre hånd. Kiralitet refererer til
Metamateriale forbedrer signifikant chirale nanopartikelsignalerGrafisk abstrakt. Kredit:ACS Photonics (2022). DOI:10.1021/acsphotonics.1c00882 Venstre hånd ligner højre hånd i spejlet, men venstrehåndshandsken passer ikke på højre hånd. Kiralitet refererer til -
 Hvordan dampmaskinen fra det 18. århundrede hjalp fysikere med at lave et kvantegennembrudHvem vidste, at dampmaskinen ville vise sig at være så nyttig? Kredit:Jorge Royan/wikimedia, CC BY-SA Den hvæsende lyd, du hører i baggrunden, når du skruer op for lyden på din musikafspiller, kal
Hvordan dampmaskinen fra det 18. århundrede hjalp fysikere med at lave et kvantegennembrudHvem vidste, at dampmaskinen ville vise sig at være så nyttig? Kredit:Jorge Royan/wikimedia, CC BY-SA Den hvæsende lyd, du hører i baggrunden, når du skruer op for lyden på din musikafspiller, kal
- Respiratoriske virale patogener som SARS-CoV-2 er nemme at teste på stedet med ny nanofilm
- Jeg har brugt årtier på at føre tilsyn med nødhjælpsoperationer rundt om i verden, og her er hv…
- Sådan finder du domænet for en kvadratrødfunktion
- Ny kystovertopningsprognose gjort tilgængelig for offentligheden
- Hvordan former vand Jorden?
- At hjælpe lærere med at praktisere det, de underviser i, kunne hjælpe dem med at blive undervisen…


